近日,日本札幌北海道大学神经外科在”JAMA Neurology“期刊杂志发表了一篇“同种异体干细胞治疗急性缺血性中风:2/3期随机临床试验。
干细胞治疗急性缺血性中风:第2/3期临床试验

结果:发现在这项有206名参与者参加的随机临床试验中,与安慰剂相比,在缺血性中风发作后18至36小时内静脉注射MultiStem疗法是安全的,但在90天时并没有改善短期结果。没有出现3级或4级过敏反应,包括老年患者。
意义:这项研究的结果支持异体干细胞治疗中风的安全性,但需要进一步研究来确定异体干细胞治疗缺血性中风是否对符合特定标准的患者具有有益作用。
什么是中风
中风是全球第二大死亡原因,也是导致残疾的主要原因,2019年有 660万人死于中风。循证再灌注治疗,包括静脉溶栓和机械血栓切除术(MT),广泛用于中风治疗。尽管这些治疗的结果各不相同,但大约50%的患者在中风后3个月仍会出现残疾,强调了围绕这种治疗方法的复杂性和持续的争论。这种动态的景观凸显了对新的治疗选择和扩大治疗窗口的需求。

细胞疗法显示出希望通过调节免疫反应来增强功能恢复,提供神经保护,并恢复受伤大脑的神经回路。各种细胞类型(间充质干细胞、骨髓单核细胞、神经干细胞,和诱导多能干细胞)和给药途径(静脉内、动脉内和脑内)在不同的时间窗口(几小时到几个月)进行了探索。
先前针对亚急性和慢性中风的自体细胞疗法的随机临床试验(RCT)表明,与残疾和日常生活活动有关的结果有所改善。然而,这些试验并不关注急性中风,样本量小,并且使用了耗时的干细胞制备和给药程序。
与自体干细胞相比,同种异体干细胞在治疗方面具有明显的优势,因为它们具有现成的特性,并且可以在病程早期使用。MultiStem是一种批量生产的干细胞产品,通过多种机制提供益处。例如,MultiStem可以减少炎症、调节免疫失调、保护受损细胞并促进血管生成、组织修复和愈合。
目前,很少有随机对照试验研究了同种异体干细胞(例如MultiStem)在中风治疗中的应用。MultiStem急性中风治疗促进康复 (MASTERS) 试验使用同种异体、骨髓来源、临床级、多能成体祖细胞系,并提供了宝贵的见解,尽管是在中风后24至48小时内进行的。
干细胞治疗急性缺血性中风:第2/3期临床试验
本研究报告了使用再生细胞对急性中风进行2/3期治疗评估(TREASURE) 试验的结果,该试验探讨了MultiStem对缺血性中风发作后18至36小时内接受治疗的患者的安全性和有效性。
设计、地点和参与者:2017年11月15日至2022年3月29日期间,日本44家学术和临床中心开展了 “使用再生细胞治疗急性脑卒中评估(TREASURE)”多中心、双盲、平行组、安慰剂对照2/3期随机临床试验。纳入标准为年龄在20岁或以上、患有急性缺血性脑卒中(基线时美国国立卫生研究院脑卒中量表[NIHSS]评分为8-20分)、确诊急性脑梗死累及大脑皮层且主轴超过2厘米(通过弥散加权磁共振成像确定)、脑卒中发病前改良Rankin量表(mRS)评分为0或1分。数据分析在2022年5月9日至8月15日期间进行。
功效评估:主要疗效结果是第90天时具有优异结果的患者比例。这被定义为满足以下综合评分标准:mRS评分为1或更低(范围,0-6),NIHSS总分为1或更低(范围,0-42),巴塞尔指数(BI)得分为95或更高(范围,0-100)。
关键的次要终点是第365天具有优异结果的患者比例、第90天和第 365天的mRS评分分布以及第90天mRS评分为0至1和0至2的患者比例。
安全评估:安全评估包括几个主要安全终点。这些反应如下:3级或4级输注相关反应(不良事件通用术语标准,4.0版),包括输注后24小时内发生的心血管和呼吸功能异常或过敏反应;治疗后7天内发生严重不良事件;神经系统症状恶化,定义为与研究产品相关的治疗后7天评估的NIHSS评分与基线相比增加4分或更多;90天以内死亡或危及生命的不良事件;和继发感染直至第90天。
结果
这项研究包括206名患者(104人接受MultiStem治疗,102人接受安慰剂治疗)。他们的平均年龄为76.5岁(35-95岁),半数以上的患者为男性(112人[54.4%])。
主要和次要终点在组间没有差异。
MultiStem组和安慰剂组在第90天的优良率无显著差异(12[11.5%] vs10[9.8%];调整后风险差异为0.5% [95%CI,-7.3%to8.3%])。此外,任何次要终点的组间差异均无统计学意义(表2)。第90天和第365天的mRS评分分布见图2。
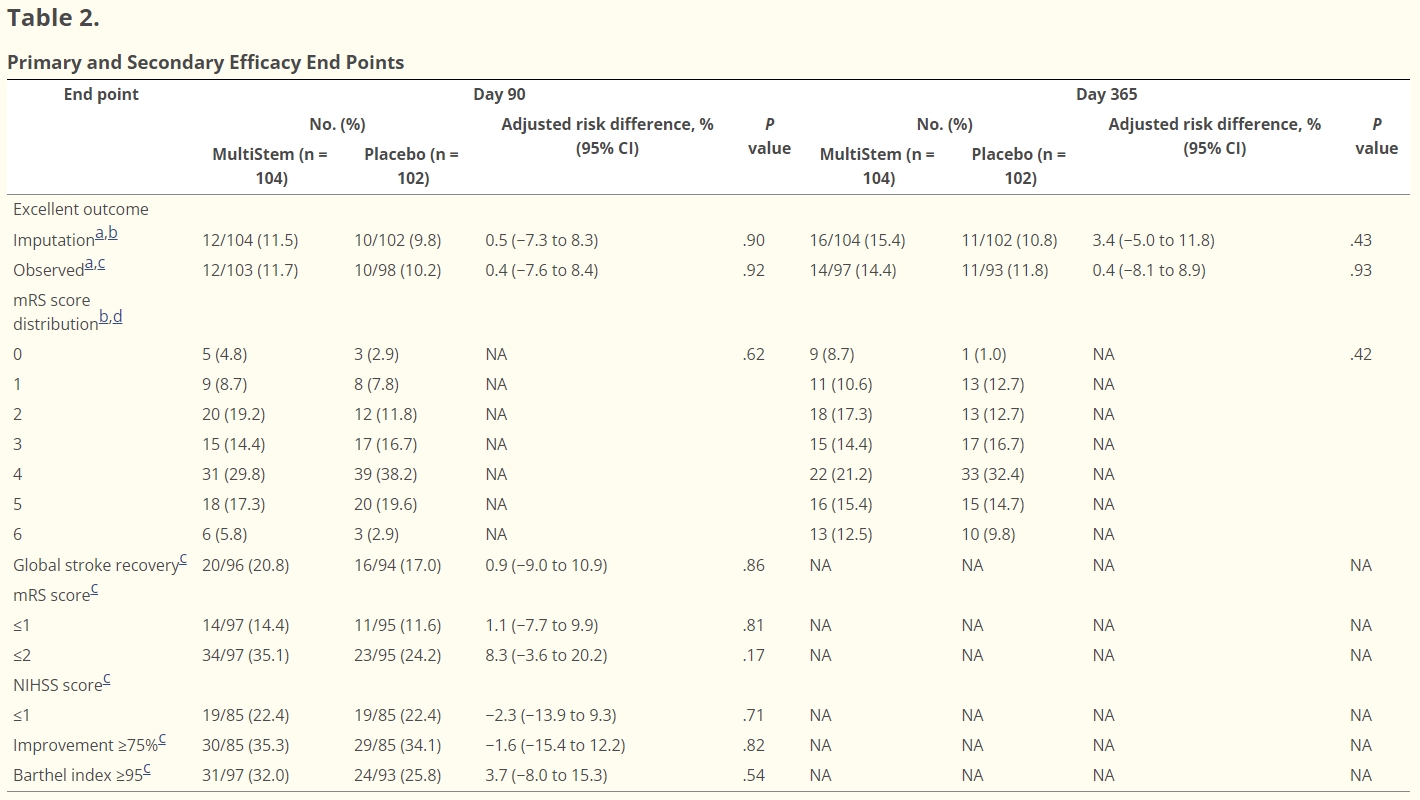
缩写:CMH,Cochran-Mantel-Haenszel;mRS,修正的 Rankin 量表;NA,不适用;NIHSS,美国国立卫生研究院卒中量表。
a:采用CMH检验对基线NIHSS评分(≤12分或≥13分)、同时接受再灌注治疗(是或否)和年龄(20-74岁或≥75岁)进行调整后比较治疗方法。MultiStem组与安慰剂组之间的风险差异及相应的双侧95%CI值根据CMH检验中应用的相同因素进行了调整,并采用Sato T的Mantel-Haenszel方法进行了计算。
b:根据随机化后的最后一次疗效评估结果(优秀结果)和mRS评分进行推算。
c:观察病例。关于优良预后,将死亡病例作为最差病例,并纳入优良预后综合评分标准的部分缺失病例(即优良预后综合评分标准的3项中至少有1项符合的病例)。
d:P值使用CMH检验计算,并根据基线NIHSS评分(≤12或≥13)、同时接受再灌注治疗(是或否)和年龄(20-74或≥75岁)进行调整,使用修正的ridit评分。
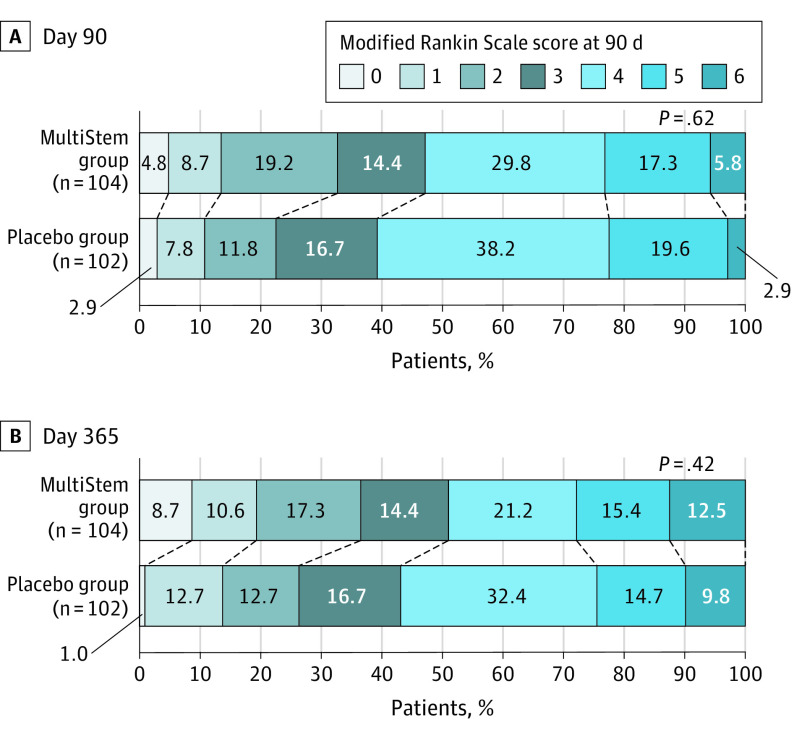
A和B,第90天 (A) 和第365天 (B) 的改良Rankin量表分数。分数范围为0至6,其中0表示没有症状;1、无临床残疾症状;2、轻微残疾;3、中度残疾;4、中重度残疾;5、严重残疾;6、死亡。
对年龄和缺血核心体积亚组进行了探索性亚组分析,在第90天时mRS评分为2或更低,且未进行多重比较校正。缺血核心体积为50mL或更少的患者在MultiStem组中的预后明显优于安慰剂组(27名患者中的8名[29.6%] vs37名患者中的3名[8.1%],P=0.04;调整后的风险差异为20.4%[95%CI,1.0%至39.9%])。与安慰剂组相比,64岁或以下的患者在MultiStem组中也往往有更好的结果,尽管组间差异不具有统计学显着性(10人中的8人[80.0%] vs12人中的5人[41.7%],P=0.08;调整后的风险差异,37.2%[95%CI,-0.4%至74.8%];图3)。
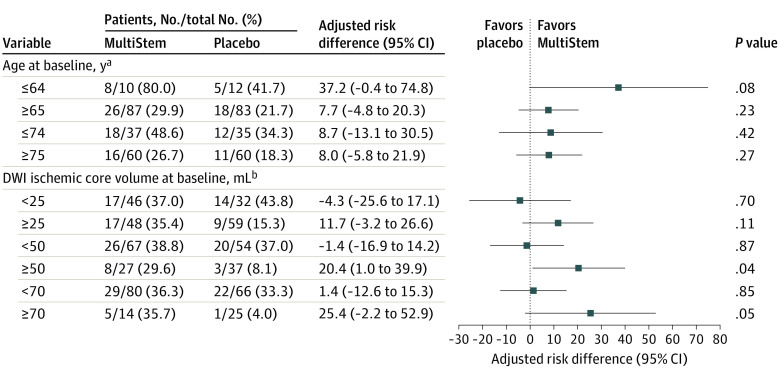
a:使用根据美国国立卫生研究院卒中量表 (NIHSS) 基线评分(≤12或≥13)调整基线的 CMH测试和接受伴随再灌注治疗(是或否),按基线年龄对患者进行分类后,对治疗进行比较。MultiStem组有97名患者,安慰剂组有95名患者。
b:使用根据基线NIHSS评分(≤12或≥13)、接受伴随再灌注治疗(是或否)和年龄调整的CMH测试,根据基线时的弥散加权成像 (DWI) 缺血核心体积对患者进行分层后比较治疗(20-74岁或≥75岁)MultiStem组有94名患者,安慰剂组有91名患者。
讨论
据我们所知,这是首个评估干细胞疗法治疗急性缺血性中风的双盲2/3期临床试验。之前的干细胞治疗中风的临床试验使用的是自体干细胞,因此双盲研究具有挑战性。由于异体细胞治疗急性中风的多中心临床试验有限,这项研究对缺血性中风的新疗法具有重大影响。
虽然在这项研究中,MultiStem组和安慰剂组在主要终点和次要终点上没有明显差异,但对第90天时mRS评分为0到2分的患者进行的探索性亚组分析(未进行多重比较校正)似乎显示,MultiStem组的治疗效果更好,尤其是缺血核心容积大于等于50毫升的患者和年龄在64岁或以下的患者。不进行多重比较校正的探索性事后分析表明,MultiStem组与安慰剂组相比,中风全面恢复且第365天BI达到或超过95分的患者比例明显更高。各组的不良事件发生率相当。
在这项研究中,MultiStem的安全性也是可以接受的。我们的研究结果与Rasmusson等人的观察结果一致,因为我们没有遇到与MultiStem输注相关的3级或4级过敏反应。此外,MultiStem的作用机制包括免疫调节,用药后7天内未出现疑似严重不良反应,进一步证实了这种细胞疗法的安全性。
研究结论
在这项临床试验中,缺血性中风发病18至36小时内的静脉注射异体细胞疗法未能显示出短期治疗效果。不过,根据未进行多重比较校正的探索性亚组分析,大面积梗死患者和年轻患者可能有疗效。我们将对TREASURE试验和正在进行的MASTERS-2试验进行综合分析,以确认MultiStem治疗的有效性和安全性。
参考资料:Houkin K, Osanai T, Uchiyama S, et al. Allogeneic Stem Cell Therapy for Acute Ischemic Stroke: The Phase 2/3 TREASURE Randomized Clinical Trial. JAMA Neurology. 2024 Jan. DOI: 10.1001/jamaneurol.2023.5200. PMID: 38227308; PMCID: PMC10792497.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信