脊髓损伤 (SCI) 是一种破坏性病症,具有复杂的病理机制,可导致损伤部位以下的感觉、运动和自主神经功能障碍。迄今为止,尚无有效的疗法可用于治疗SCI。最近,骨髓间充质干细胞(BMMSC)被认为是SCI后最有希望的细胞治疗来源。
间充质干细胞治疗脊髓损伤的七大作用机制
本综述的目的是总结使用骨髓间充质干细胞治疗脊髓损伤的细胞和分子机制的最新见解。
本工作主要从神经保护、轴突萌发和/或再生、髓磷脂再生、抑制性微环境、胶质疤痕形成、免疫调节和血管生成等七个方面综述了骨髓间充质干细胞在脊髓损伤修复中的具体机制。
介绍
脊髓损伤(SCI)是一种严重的神经系统疾病,通常会导致育龄期瘫痪,导致正常运动、感觉和自主功能暂时或永久性改变,对个人、家庭和社会经济系统产生重大影响。
据报道,全球有超过2700万患者因SCI而遭受长期残疾,每10万人中有541例。复杂的病理生理学和时间敏感性尤其限制了SCI的治疗效果。不完全性SCI,伤后3h灰质出血较少,白质无变化;伤后6~10h,出血灶逐渐扩大,神经组织水肿,24~48h后逐渐消退。由于轻伤和重伤的不完全性SCI程度不同,轻伤仅在中心出现小面积坏死灶,大部分神经纤维得以保留。
严重损伤的脊髓中央可能出现坏死和软化灶,并被神经胶质增生或疤痕所取代,仅保留一小部分神经纤维。大多数创伤后组织变性是由多种继发性损伤引起的,包括血脊髓屏障(BSCB)破坏、自由基形成、离子失衡、细胞凋亡、脱髓鞘。自发恢复发生在有限的时间窗口内,因为SCI的亚急性期被认为不利于轴突再生和功能恢复。
目前,临床治疗包括手术减压、稳定脊髓、缓解痉挛和康复治疗,其中主要包括支持治疗和损伤管理。令人沮丧的是,这些治疗的效果有限,因为它们不能有效刺激受损脊髓的修复。
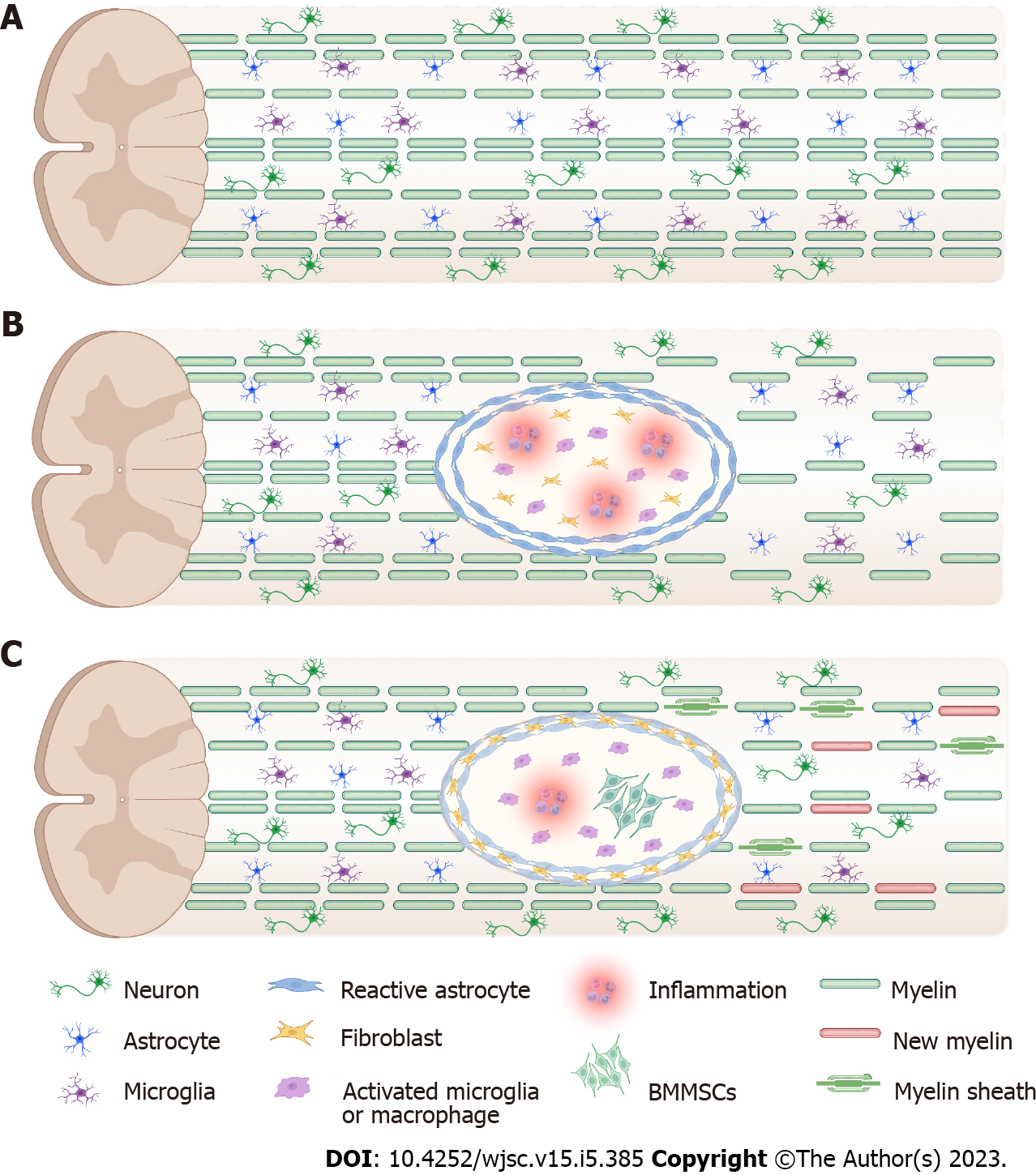
答:正常脊髓含有髓鞘包裹的轴突、神经元体、小胶质细胞、成纤维细胞和星形胶质细胞;B:原发性损伤后的继发性损伤包括胶质细胞和神经元凋亡、轴突断裂、炎症反应、缺血、脊髓缺血再灌注损伤、血管功能障碍、水肿、抑制性微环境、兴奋性毒性和自由基形成;C:骨髓间充质干细胞促进脊髓损伤修复的机制,包括神经保护、轴突生长、髓鞘形成、免疫调节、微环境调节、抑制疤痕形成、促进血管生成。BMMSC:骨髓来源的间充质干细胞。
干细胞治疗脊髓损伤的7大作用机制
由于其潜在的神经保护作用,细胞移植已成为SCI再生策略的前沿。许多细胞类型在SCI治疗中已得到广泛研究,包括少突胶质细胞前体细胞、雪旺细胞、嗅鞘细胞、神经干细胞和间充质干细胞 (MSC)。MSCs具有自我更新能力和多向分化潜能,可以分化为成骨细胞、脂肪细胞和软骨细胞。
间充质干细胞主要存在于骨髓中,也可以从其他组织和器官中分离,如脐带、脂肪组织和肌肉。其中,骨髓间充质干细胞(BMMSCs)因其免疫原性低、易于分离、伦理问题少、肿瘤发生风险低等特点,成为SCI应用中研究最广泛的细胞类型。根据目前国内外的研究进展,基于BMMSC的治疗在SCI领域具有非凡的前景。
1、骨髓间充质干细胞的神经保护作用
神经元是有丝分裂后的,没有增殖能力,开发促进神经元保护和再生的策略具有长期益处。神经保护措施不仅对于保留进一步损伤以实现最佳神经元生存能力至关重要,而且对于病理进展期间受损神经细胞的恢复也至关重要。
BMMSC在SCI中通过神经保护、神经再生和髓鞘再生来重建受损的脊髓。间充质干细胞可以释放生长因子和神经营养因子,包括脑源性神经营养因子(BDNF)、血管内皮生长因子(VEGF)、胶质细胞源性神经营养因子(GDNF)、神经生长因子(NGF)、成纤维细胞生长因子(FGF)、神经营养蛋白-3和表皮生长因子,可以增强受损组织的再生和修复。
2、轴突生长
轴突是维持神经元之间通信的独特细胞结构。SCI后持续功能障碍的一个重要原因是轴突破坏,因此促进轴突再生和可塑性非常有希望。然而,先前的研究表明,注射的MSC在CNS中聚集的百分比为0.75%-18.5%和6.7%,因此可以想象只有一小部分细胞到达SCI部位。
3、髓鞘再生
创伤性SCI中的脱髓鞘可导致功能丧失,而保留的神经纤维的髓鞘形成不良可能会导致永久性功能障碍。髓磷脂损失伴随着少突胶质细胞凋亡,丢失的少突胶质细胞和髓磷脂的替代可提高传导性并保护轴突免于退化。移植细胞在失去髓鞘的轴突周围产生髓磷脂的过程是一种促进SCI后恢复的机制。
4、免疫调节
许多研究表明,SCI后的BMMSC移植可以通过减轻有害炎症或增强有益炎症来发挥治疗作用。
BMMSC移植在SCI后发挥免疫调节作用主要是通过诱导抗炎免疫细胞的形成、调节TLRs的表达水平、抑制损伤脊髓的炎症反应,从而促进功能恢复。SCI后,机体因休克和压力立即进入免疫抑制状态。在受伤部位首先动员的细胞是先天免疫系统的骨髓细胞,例如中性粒细胞和巨噬细胞,它们吞噬碎片。然后,适应性免疫细胞(例如B淋巴细胞和T淋巴细胞)被募集到受伤的脊髓。
5、改善抑制性微环境
移植BMMSCs的SCI中心发现少突胶质细胞标志物表达很少,而轴突数量显着增加,表明移植的细胞为内源性神经干细胞的再生和神经分化提供了合适的环境。过度表达的BMMSC中的BDNF通过影响少突胶质细胞进一步促进轴突髓鞘再生。
6、抑制胶质疤痕形成
大量SCI动物模型实验研究表明,BMMSC移植可以抑制胶质疤痕形成。综上所述,BMMSC移植可以抑制胶质疤痕形成,为SCI后轴突再生提供良好的环境。
7、预防血管损失并改善血管生成
越来越多的证据表明,BMMSC植入可以促进血管生成和血管稳定性,以治疗不同疾病,特别是缺血性疾病,如心肌梗塞和脑梗塞。同样,在动物SCI后,植入的BMMSC可以增强血管生成。此外,体外研究也证实BMMSC移植可促进血管形成和血管保护作用。
BMMSCs对SCI患者的临床试验在过去的几十年里,细胞移植被认为是脊髓损伤后一种有前途的治疗方法。不仅有大量的动物和临床前研究,还有相当数量的临床研究,多项系统评价/荟萃分析已经证明了细胞移植对SCI患者的作用。其中,间充质干细胞移植是治疗脊髓损伤最广泛、最有前景的治疗方法。
干细胞治疗脊髓损伤的临床应用
在评估相关文献后,我们发现了38项包含1090名受试者的临床研究,提供了骨髓间充质干细胞移植治疗脊髓损伤患者的安全性和有效性的整体证据,主要表现为至少一个节段的ASIA评分改善,以及感觉和运动方面的改善根据之前的不同研究,观察到了改善。有研究表明,高达70%的完全颈段SCI患者和33%的胸段SCI患者在受伤后1年内可通过自然恢复恢复至少一级脊髓水平。
结论
从以往的研究结果来看,单一骨髓间充质干细胞治疗脊髓损伤所能达到的效果有限,联合治疗是未来重要的发展方向。
使用各种分子或因子(包括基因调节等)的联合治疗。)可以增强细胞治疗的效果,达到多效叠加的效果。
此外,大多数临床前研究目前设计的观察期为4周和8周,更长的观察期对于干细胞疗法的临床转化非常重要,以便在可能的情况下探索和解决某些不良反应。
最后,鉴于目前令人鼓舞的临床前试验结果,一些治疗方法已转化为临床实践。BMMSC移植已被证明在SCI患者中是安全的,并且在某些病例中看到了部分疗效,但大多数临床研究仍处于I期和II期,III期试验的结果对于干细胞的临床转化具有非凡的意义。 SCI的细胞疗法。总而言之,尽管仍然存在许多问题和挑战。
参考资料:
引文:黄丽云、孙翔、潘慧霞、王琳、何成庆、魏庆。以骨髓间充质干细胞为重点的脊髓损伤细胞移植治疗:进展与挑战。 世界干细胞杂志 2023;15(5):385-399
Huang LY, Sun X, Pan HX, Wang L, He CQ, Wei Q. Cell transplantation therapies for spinal cord injury focusing on bone marrow mesenchymal stem cells: Advances and challenges. World J Stem Cells 2023; 15(5): 385-399 [PMID: 37342219 DOI: 10.4252/wjsc.v15.i5.385]
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信