间充质干细胞 (MSC) 一直是无数临床研究的主题,涉及从克罗恩病到移植物抗宿主病 (GVHD) 等各种病理学。
基于间充质干细胞的疗法已经可用于治疗一系列疾病或医疗状况。从自身或捐赠者获得的自体或同种异体间充质干细胞在医疗实践中各有优点和缺点。
目前,人们正在研究干细胞在治疗许多无法治疗的疾病中的潜在广泛用途。如今,现代治疗策略愿意使用不同来源的间充质干细胞(MSC)。研究人员越来越意识到间充质干细胞的性质及其使用的新可能性。
由于其特性,特别是其自我再生、分化成多种细胞谱系和参与免疫调节的能力,间充质干细胞已成为开发现代有效的未来治疗策略的有前途的工具。间充质干细胞的巨大潜力和可用性使其在治疗许多疑难杂症方面具有多种临床应用。除了其许多优点和好处外,间充质干细胞的使用仍然存在问题。
间充质干细胞的作用机制是什么?他们如何到达目的地?间充质干细胞临床应用安全吗?这些是当间充质干细胞被视为治疗工具时出现的主要问题。
一文梳理丨间充质干细胞-来源-安全性-优缺点
间充质干细胞的多样性、其不同的临床应用以及尚未彻底研究的许多特征是关于这些细胞的讨论和争议观点的来源。在这里,我们回顾了目前关于间充质干细胞的治疗潜力、临床效果和临床应用安全性的知识。
什么是间充质干细胞?
20世纪60年代,弗里登斯坦等人发现了一种在体外形成克隆集落的成纤维细胞(CFU-F,Colony Forming Unit-Fibroblast)。弗里登斯坦的观察发现了一种特殊类型的细胞,目前被称为间充质干细胞(MSCs)。间充质干细胞是原生的、非特化的、非造血的可塑性粘附细胞,具有巨大的增殖潜力和自我更新及分化能力。
2006年,国际细胞治疗学会(ISCT)提出了定义人类多能间充质基质细胞的基本标准,间充质干细胞的名称由此演变而来。
间充质干细胞在标准培养条件下具有可塑性粘附特性,并具有向成骨细胞、软骨细胞和脂肪细胞三系分化的能力,此外,95%以上的间充质干细胞对三种特异性表面标志物–CD73(SH3/4)、CD90(Thy-1)和CD105(SH2)–呈阳性,不表达CD45、CD34、CD14、CD11b、CD79a、CD19或主要组织相容性复合体(MHC)II类。
间充质干细胞还表达其他标记物,包括 CD9、CD10、CD13、CD29、CD44、CD49、CD51、CD54(ICAM-1)、CD117(c-kit)、CD146(MCAM)、CD166(ALCAM)和 Stro-1,但这些标记物的特定组合表达似乎取决于宿主组织。尽管已经发现了多种描述间充质干细胞的阳性标记物,但还没有一种标记物被认为是间充质干细胞的特异性标记物。
还应注意的是,不同来源的间充质干细胞在分化和增殖方面的潜力可能有很大差异。有研究认为,这些差异是间充质干细胞所处的特定微环境直接影响的结果。
尽管描述间充质干细胞的报道越来越多,但关于间充质干细胞的正确鉴定却出现了许多争议。ISCT提出的标准似乎并不充分,因为从不同组织中分离出来的间充质干细胞在分化、增殖能力和细胞表面表达等方面都代表了一个相对异质的细胞群体。
间充质干细胞的来源
目前,间充质干细胞可以从多种来源中分离出来 (图1)。
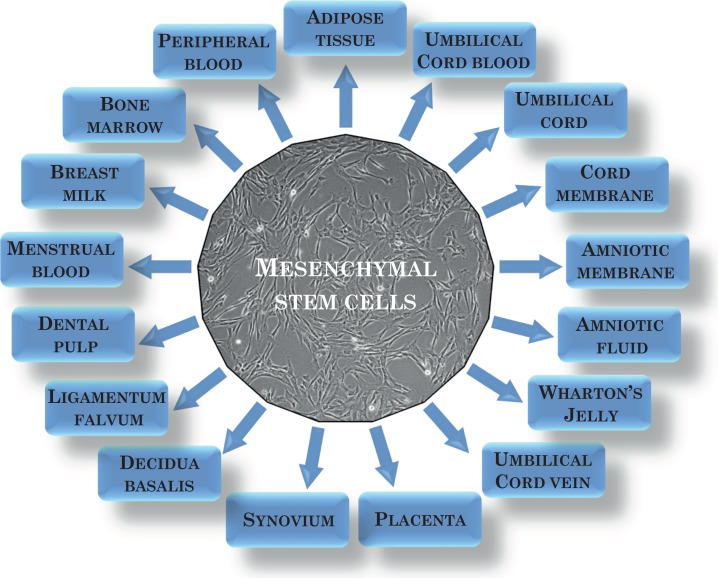
截至近日,已提出新的间充质干细胞来源。间充质干细胞存在于牙髓、牙周膜、肌腱、皮肤、肌肉和其他组织中(图1)。然而,分离效率存在差异,这与供体组织的可用性、状况和年龄有关。一个非常重要的问题是供体细胞的年龄。从年轻供体获得的细胞不易受到氧化损伤和变化的影响,它们在培养物中的老化速度要慢得多,并且增殖率更高。
目前,许多研究集中在间充质干细胞在细胞治疗中的应用。间充质干细胞被用作治疗关节退行性变化以及重建骨骼和软骨的工具,并用于整形外科、美容医学、心血管疾病、内分泌和神经系统疾病、细胞移植以及受损肌肉骨骼组织的修复。由于这些细胞的特殊性质,例如快速增殖、高分化能力以及迁移到损伤部位的能力,新的临床应用正在接受测试。
干细胞治疗的新方法是使用细胞外囊泡 (EV),它可以用作MSC的替代品。EVs作为治疗载体具有旁分泌作用,无需细胞直接参与。它们从干细胞中释放出来,并向靶位点提供许多成分,例如mRNA、DNA 和蛋白质。最近的许多研究都描述了这种方法但仍然需要对干细胞外泌体的作用机制有透彻的了解。
间充质干细胞的迁移和归巢
间充质干细胞的治疗效果取决于其到达损伤部位的能力,而这种能力是由于间充质干细胞能够迁移、粘附和移植到目标组织中。影响间充质干细胞归巢治疗效果的因素有很多。其中,培养条件、传代次数、供体年龄、输送方法和宿主的接受能力起着重要作用。
细胞疗法的功效很大程度上取决于递送方法。最常见的MSC给药方法是静脉输注。然而,在细胞到达目标之前,大多数细胞被困在各个器官的毛细血管内,尤其是肺部。这种损耗可以用以下事实来解释:MSC是相对较大的细胞并表达各种粘附分子。尽管间充质干细胞可能被困在肺部,但大量证据表明它们能够归巢于受损组织。
有趣的是,最近的数据还表明,尽管存在与静脉输注相关的问题,但这种途径与其他 MSC 输送方式具有相似的功效。在某些情况下,动脉内注射似乎是更有效的途径。研究表明,与通过静脉给药相比,通过颈内动脉输送MSC可以更有效地促进其迁移和归巢到受伤的大脑中。与该递送途径相关的风险包括可能在微血管中出现的闭塞。当间充质干细胞直接输送到心脏受损区域附近时,到达梗塞周围区域的细胞数量要高得多。
如前所述,有效的间充质干细胞疗法的必要条件是细胞能够到达损伤部位并归巢到受影响的组织。毫无疑问,特定的受体和粘附分子以及与内皮细胞的相互作用在这种迁移和归巢过程中起着至关重要的作用。细胞粘附蛋白在质膜中表达,如整合素,参与细胞与细胞外基质蛋白(EMC)(如胶原蛋白、纤连蛋白和层粘连蛋白)的粘附。
体内研究表明,间充质干细胞具有趋化特性,静脉注射后能够附着在内皮细胞上,并在炎症条件下上调的因子作用下在内皮细胞之间向损伤组织迁移。然而,它们的跨内皮迁移(TEM)、透射以及向损伤和炎症部位归巢的详细机制尚未得到详细解释。据推测,这种机制可能与白细胞的机制类似(图2),但有不同的粘附分子参与。
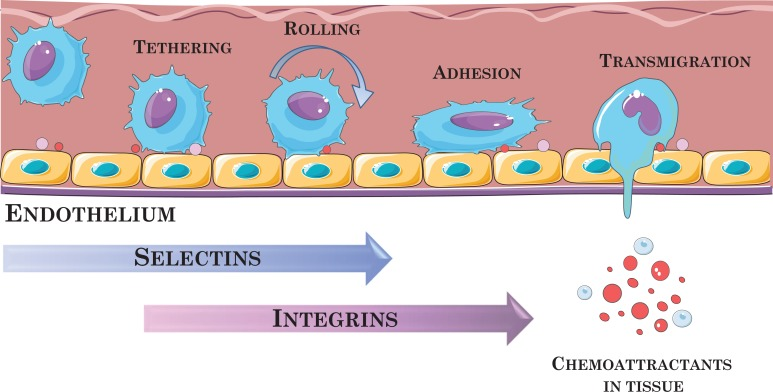
间充质干细胞的免疫学特性
一般认为,间充质干细胞不具有免疫原性,因此无需免疫抑制即可移植到异基因宿主体内。间充质干细胞的作用机制基于其免疫调节特性和免疫抑制活性。它们能够抑制免疫系统不同细胞的增殖和活化。这些相互作用可能直接发生(即细胞-细胞相互作用),也可能间接发生(通过可溶性因子),而且这种抑制途径与间充质干细胞和T细胞之间的MHC匹配无关。间充质干细胞的免疫调节作用体现在许多T细胞特性上,如活化和增殖,从而有效抑制免疫反应。
一般认为,间充质干细胞不具有免疫原性,因此无需免疫抑制即可移植到异基因宿主体内。间充质干细胞的作用机制基于其免疫调节特性和免疫抑制活性。它们能够抑制免疫系统不同细胞的增殖和活化。这些相互作用可能直接发生(即细胞-细胞相互作用),也可能间接发生(通过可溶性因子),而且这种抑制途径与间充质干细胞和T细胞之间的MHC匹配无关。间充质干细胞的免疫调节作用体现在许多T细胞特性上,如活化和增殖,从而有效抑制免疫反应。
间充质干细胞疗法的安全性
迄今为止,已经进行了许多研究来调查基于MSC的疗法的安全性。临床试验表明,体外培养的人类间充质干细胞不易受到不良变化的影响。
加拿大的一个小组分析了使用BM-MSC的临床试验。在对36项研究进行彻底分析后,他们发现MSC的使用与致瘤潜力之间没有关系,并且没有报道该疗法的严重副作用。
Karussis等人还研究了MSC治疗的安全性和影响。多发性硬化症和肌萎缩侧索硬化症患者。在一项持续25个月的研究中,在34名接受检查的患者中,没有观察到治疗造成的严重不良反应。此外,20名患者在移植后1年接受了检查,MRI结果没有显示任何令人不安的变化。然而,需要对使用间充质干细胞疗法的安全性进行更长期的研究和观察。
间充质干细胞生物学的缺点
间充质干细胞(MSCs)作为一种治疗工具,虽然在许多疾病治疗中展现出潜力,但也存在一些明显的缺点和潜在风险:
- 治疗效果的不确定性
- MSCs的治疗效果可能因个体差异而有所不同。不同的患者在接受相同MSC治疗时,可能观察到不同的疗效,这需要进一步的研究和临床试验来验证。
- 高昂的治疗成本
- MSCs疗法的成本较高,包括干细胞的采集、分离、培养和处理等步骤,这些过程需要高技术和设备支持,导致治疗费用昂贵。对于普通患者而言,经济负担较大。
- 潜在的副作用
- 尽管MSCs疗法相对安全,但仍存在一些潜在的副作用和风险。例如,干细胞移植可能引发感染、排异反应或系统性过敏等问题。此外,干细胞在体内的行为尚未完全掌握,存在一定的未知风险。
- 技术与法规的挑战
- MSCs疗法的推广和应用面临技术和法规方面的挑战。干细胞的培养和扩增技术需要不断优化,同时,干细胞疗法的安全性和有效性需要得到充分验证。此外,相关法规和监管政策也需进一步完善,以确保干细胞疗法的规范应用。
这些缺点和潜在风险提示在临床应用中需要谨慎考虑MSCs的使用,并可能需要进一步的研究和临床试验来克服这些挑战。
间充质干细胞生物学的优点
间充质干细胞(MSCs)是一种多功能干细胞,具有多种潜在的治疗应用,以下是间充质干细胞的一些主要优点:
- 免疫调节能力:MSCs能够调节免疫系统,降低移植排斥反应的风险,这使得它们在同种异体移植中特别有用。
- 组织修复和再生:MSCs能够迁移到损伤部位,并分化成多种类型的细胞,有助于组织和器官的再生。这种能力使得MSCs在治疗关节退行性疾病、骨折愈合和心肌修复等方面具有潜力。
- 易于获取和培养:MSCs可以从多种组织中分离出来,如骨髓、脂肪组织、脐带等,且这些细胞在体外培养中相对容易维持。
- 低免疫原性:与其他类型的干细胞相比,MSCs的免疫原性较低,这意味着它们在治疗过程中不太可能引起强烈的免疫反应。
- 广泛的应用范围:MSCs在临床试验中已被用于治疗多种疾病,包括心血管疾病、神经系统疾病、糖尿病等,显示出了良好的安全性和疗效。
- 伦理优势:与胚胎干细胞相比,MSCs的获取不需要涉及胚胎,因此在伦理上更为可接受。
这些优点使得MSCs成为再生医学和细胞治疗领域的重要研究方向。
结束语
干细胞无疑是治疗多种疾病的巨大希望。由于它们存在于许多成体组织中并且不会引起伦理问题,因此它们比胚胎干细胞具有巨大的优势。由于其独特的功能,例如易于分离和培养、在许多组织中的可用性、免疫调节特性以及其使用不存在伦理问题,我们相信它们可用于自体和同种异体移植。
根据我们的数据,间充质干细胞的同种异体临床应用似乎是再生医学中有前途的工具。
参考资料:Musiał-Wysocka A, Kot M, Majka M. The Pros and Cons of Mesenchymal Stem Cell-Based Therapies. Cell Transplant. 2019 Jul;28(7):801-812. doi: 10.1177/0963689719837897. Epub 2019 Apr 24. PMID: 31018669; PMCID: PMC6719501.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 扫码添加官方微信
扫码添加官方微信