概述:尽管有最佳的医疗实践,糖尿病 (DM) 仍常常导致慢性肾脏损伤。糖尿病肾病(DKD)是由肾脏和全身因素复杂的相互作用引起的。使用药物针对特定的致病因子并不能有效治疗糖尿病肾病。然而,干细胞疗法通过解决多种疾病途径和促进肾脏再生提供了一种有前途的替代方案。间充质干细胞(MSC)因其在成体组织中的优越可及性和卓越的作用模式(例如产生旁分泌抗炎和细胞保护物质)而具有巨大的前景。
间充质干细胞疗法对糖尿病肾病的治疗作用
随着间充质干细胞治疗糖尿病肾病越来越接近临床应用,这篇综述对它的发展进行了批判性评估。动物模型的结果表明,全身MSC输注可能对糖尿病肾病进展产生积极影响。本文回顾了有关在糖尿病肾病临床前和临床试验中使用间充质干细胞治疗的最新文献。还强调了与糖尿病肾病相关的有效生物标志物,这可能有助于更好地了解MSC在这种疾病进展中的作用。
关键信息
- 间充质干细胞在糖尿病肾病中具有抗炎和旁分泌作用。
- 间充质干细胞在患有糖尿病肾病的动物模型中缓解。
- 间充质干细胞有望治疗糖尿病肾病。
介绍
糖尿病和慢性肾脏病 (CKD) 患者是糖尿病肾病 (DKD) 患者的一个独特亚群,可以通过尿液中白蛋白排泄增多或肾小球滤过率 (GFR) 降低或两者兼而有之来识别。它最终会扰乱从人体排出不需要的产物和液体的正常过程,并侵犯肾功能。国际糖尿病联盟 (IDF) 声称,40%的糖尿病患者在最晚期会出现肾衰竭。此外,糖尿病和高血压是关键指标,有时占80%的终末期肾衰竭病例 (ESRF) 。
临床体征和症状
蛋白尿,或尿液中白蛋白被去除,体重增加以及腿部和脚踝发炎;夜尿反复、晨起头晕恶心、贫血;血压升高都是人类DKD的征兆。2型糖尿病 (T2DM) 患者患DKD的可能性比1型糖尿病患者高40%。 DKD是导致终末期肾病即CKD和ESRD的主要因素。中低社会经济国家的不均衡增长和对全球疾病负担的低估导致DKD 患病率持续上升。
此外,DKD与高死亡率有关。患有肾脏疾病的糖尿病患者的死亡风险高出31.1%,并且随着病情的严重程度而增加。早期DKD患者也有较大的死亡风险。DKD还带来了巨大的财务和社会压力。 DKD通常很晚才被发现,直到出现明显的困难为止。信息缺乏和筛查不一致是早期诊断的主要障碍。早期诊断是减轻DKD经济负担的实用方法。
造成糖尿病肾病(DKD)的危险因素有哪些?
蛋白尿增多
肾脏疾病的进展是由尿液中白蛋白的大量排放引起的。尿液中微量白蛋白尿(30-300mg)或大量白蛋白尿(>300mgg-1)通过白蛋白肌酐排放增加来描述。微量白蛋白尿和大量白蛋白尿都是肾功能损伤的标志物,通常用作肾功能障碍的诊断指标。尿液中白蛋白的过度分泌及其与肾小球的关系如图1所示。
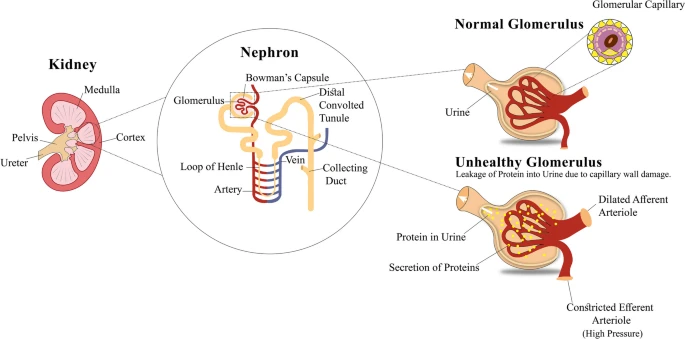
糖尿病肾病,受糖尿病影响的肾病。肾小球的全面解剖表明,在健康的肾小球中,毛细血管将蛋白质分子保留在血液中,常规尿液将排出体外。同时,在不健康的肾小球中,肾小球毛细血管壁受损,导致蛋白质分子溢出到尿液中。不健康的肾小球会导致尿液中白蛋白的排出量增加,导致糖尿病肾病(DKD)
高血糖
DKD的另一个主要且独立的危险因素是高血糖。抗氧化系统的改变和晚期糖基化终产物(AGE)的产生增加导致肾功能持续恶化。 DKD的病理生理学同样被认为涉及由高血糖通量和几个相关的微血管问题引起的多元醇途径的刺激。糖化血红蛋白 (HbA1c) 变异与糖尿病(T1DM和T2DM)患者相关。糖尿病肾病的发病和进展很大程度上依赖于HbA1c。意大利的一项多中心试验肾功能不全和心血管事件(RIACE)报告了相关发现。在T2DM患者中,强有力的血糖控制在推迟蛋白尿的发生和阻止其进展方面显示出积极的作用。
高血压
DKD的一个重要危险因素是高血压。最近的一项荟萃分析显示,高血压与糖尿病肾病的发病存在着不祥的联系。与非高血压患者相比,高血压患者更容易患糖尿病肾病,95%置信区间(CI,13.1-2.14)。来自中国的一项基于人群角度的研究发现,控制高血压可以使终末期肾衰竭的风险降低23%,进一步支持了这一观点。
血脂异常
糖尿病患者血脂异常的特点是高密度脂蛋白降低以及甘油三酯和低密度脂蛋白升高。通过特化上皮细胞(即覆盖肾小球毛细血管表面的足细胞)的死亡、死亡脂肪细胞的清除(巨噬细胞浸润)以及细胞外基质形成的增加,血脂异常导致DKD的进展。由于高血糖和胰岛素抵抗,DKD患者的血脂异常水平可能会升高。
肥胖
根据证据,肥胖和糖尿病引起的肾脏疾病(DKD)似乎密切相关。然而,肥胖导致DKD的分子机制尚不明确。据认为,这一危险因素会导致蛋白尿和肾小球肾炎(即肾小球损伤和肾肥大)。
抽烟
它的特点是作为一个离散的关键角色来增强DKD的进展。吸烟在DKD的扩展中发挥多方面的致病作用,包括氧化应激、脂肪、胆固醇、甘油三酯增加、蛋白质糖化、AGEs增加和蛋白质流失到尿液中(肾小球硬化)。研究发现,吸烟会增加患糖尿病肾病的可能性。最近的一项荟萃分析进一步支持了这一点,该分析发现吸烟的T2DM患者患糖尿病肾病的几率更高。它是通过结合九组研究的数据获得的。
糖尿病肾病的病理生理学
良好的血糖控制与糖尿病患者更好的肾功能和更有限的DKD进展有关。持续的高血糖或高血糖水平会对肾脏造成多种有害影响。AGEs的形成和氧化损伤会对肾脏的结构和功能造成损害。缺氧或缺氧也可能是由于肾脏血流不畅而导致的。代谢和能量紊乱会进一步导致肾脏损伤。糖尿病肾病(DKD)的简明病理生理学如图2所示。
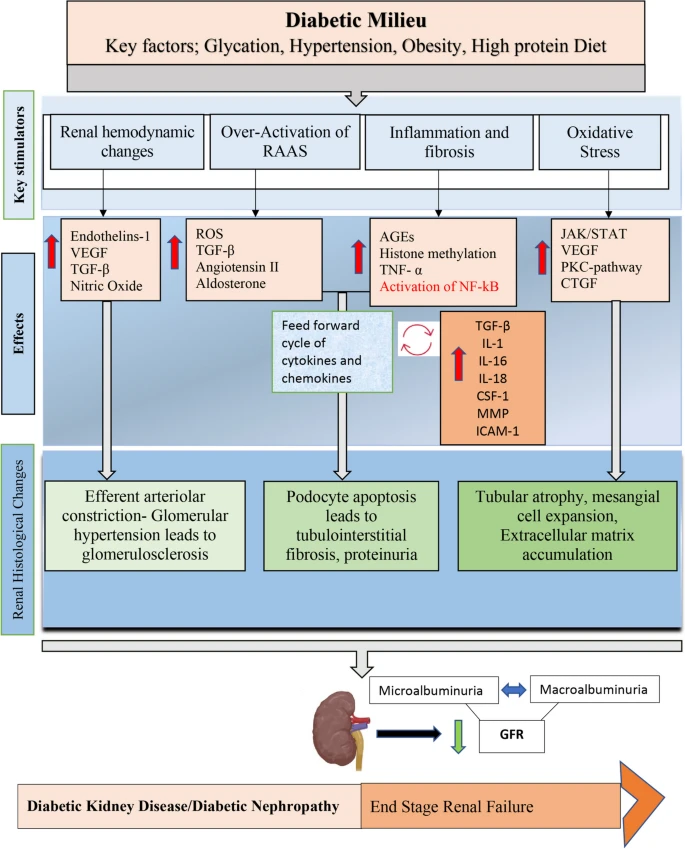
目前治疗糖尿病肾病标准是什么?
DKD是糖尿病的常见并发症,可导致血压、血脂和血糖水平异常,从而进一步损害肾脏并增加患心血管疾病的风险。对于糖尿病患者来说,密切监测和管理血糖水平并与医疗保健提供者合作管理任何其他风险因素非常重要。生活方式的改变对于糖尿病及其相关后果的诊断、控制和治疗至关重要。
控制血糖水平
据估计,无论血糖水平控制得如何,约有20%的DM患者会患上DKD。某些临床研究表明,强化血糖控制可以延缓糖尿病肾病的进展并保护肾功能,例如糖尿病患者微量白蛋白尿的发生和eGFR降低。根据美国糖尿病协会 (ADA)/欧洲糖尿病研究协会 (EASD) 的规定,为了减缓DKD的进展,初始DM患者必须加强血糖控制,将HbA1c水平降至7.0%或更低和肾脏疾病结果质量倡议 (KDOQI) 。然而,一些研究发现HbA1c水平低于6.0%或高于9.0%与死亡风险增加相关。因此,当前的国际指南建议根据患者的特征和危险因素采取个体化的治疗强度方法。这意味着虽然7%的HbA1c目标是一般建议,但将考虑治疗强度的个体化方法,这意味着目标可能因不同患者而异。
血糖控制的重要性怎么强调都不为过。它直接影响各种治疗方法的有效性,包括干细胞疗法,例如基于 MSC的糖尿病治疗方法。
控制体重
体重过重会导致胰岛素抵抗、全身炎症和代谢失调,进而对肾功能产生有害影响。因此,通过生活方式调整、饮食调节和日常体育锻炼实现的成功体重管理不仅是加强血糖控制的重要手段,也是减少DKD风险和进展的重要手段。当我们深入研究DKD治疗的多方面方法时,重要的是要考虑创新方法,例如间充质干细胞 (MSC) 在肥胖、糖尿病及其相关并发症中的治疗潜力。在大量研究中,向饮食诱导肥胖 (DIO) 小鼠施用人类MSC或MSC衍生的条件培养基可导致体重和脂肪量显着减少。更重要的是,间充质干细胞治疗显示出肥胖小鼠代谢参数的显着改善,包括增强胰岛素敏感性以及降低血糖和甘油三酯水平。因此,多次给予 MSC可以保护肥胖小鼠免受与肥胖相关的代谢综合征的影响,包括糖尿病、脂肪肝疾病和心血管损伤。
血压控制
DKD患者严格的血压监测可以显着降低蛋白尿,延缓肾功能丧失,并最大限度地降低心脏病风险。美国糖尿病协会 (ADA) 建议糖尿病患者将血压控制在140/90mmHg (1mmHg=0.133 kPa) 以下。对于患有心血管疾病或肾功能衰竭的患者,建议将血压目标降低到130/80mmHg。所有其他患者将血压控制在 130/80mmHg的目标。
控制血脂
DKD患者严重血管问题,可能导致高脂血症。它会破坏内皮细胞的屏障功能,同时还会危及血液供应。 KDOQI指南建议采用他汀类药物治疗来降低低密度脂蛋白胆固醇 (LDL-C) 水平,以降低DKD患者发生动脉粥样硬化并发症的风险。
根据胆固醇治疗的荟萃分析,LDL-C每降低mmol/L,重大心血管事件的发生率就会降低23%。与EASD合作发布的《2019ESC糖尿病、糖尿病前期和心血管疾病发展指南》建议,患有动脉硬化性心血管疾病和糖尿病或3-4期CKD的患者,LDL-C应控制在低于低于1.4mmol/L(或55mg/dL)可降低心血管疾病的风险。与一般人群的目标低于2.5mmol/L相比,这是一个更严格的目标。
低蛋白饮食
蛋白尿(尿液中蛋白质含量)的减少已被证明是T2DM患者肾脏和心血管事件风险降低的综合指标。不管怎样,针对DKD的低蛋白饮食计划引起了一些讨论。美国糖尿病协会 (ADA) 建议DKD患者应控制蛋白质摄入量,每天摄入约0.8g/kg体重。这与较高水平的蛋白质摄入量形成鲜明对比,较高水平的蛋白质摄入量被发现会加速肾功能的衰退(通过肾小球滤过率来衡量)。这是因为较高水平的蛋白质摄入量会导致肾脏必须过滤的代谢废物增加,从而导致进一步的损害。然而,摄入较少的蛋白质会对血糖、肾小球滤过率或心血管问题产生有益的影响。
新型降糖药物的使用
RAAS(ACE抑制剂和 ARB)和二甲双胍(控制血糖水平的抗糖尿病药物)可以帮助减轻肾脏的负担。这些药物可以一起使用或作为单一疗法,以帮助减缓DKD的进展并保护肾功能。
治疗DKD的传统方法,如常规处方药物、物理疗法和饮食治疗,并不总是有效。为了减少大量患者数量和医疗服务负担,需要细胞疗法等创新治疗模式。这些技术可能会阻碍DKD的发展,并有助于修复缺陷器官而不引起任何严重的副作用。间充质干细胞(MSC),即成体干细胞治疗,可能是再生医学领域最有利的细胞疗法。由于它们具有自我更新和分化潜力,因此可以全身或局部用于治疗许多疾病。
间充质干细胞治疗糖尿病肾病
自我更新和产生不同谱系细胞的能力是干细胞的两个优良品质。间充质干细胞与多种人类疾病(如糖尿病、恶性生长(癌症)以及神经退行性疾病(如帕金森病和阿尔茨海默病))的相互作用已得到广泛研究。
间充质干细胞通常可以在骨髓、产道、脐带血、内脏脂肪、脑组织和其他一些组织中观察到。研究强调,间充质干细胞具有高度可变性,在不同来源之间甚至同一来源内表现出显着的异质性,这强调了彻底表征和质量控制措施的必要性。考虑到这一点,国际细胞治疗协会(ISCT)对各种来源分离的所有间充质干细胞制定了具体标准。 2019年,ISCT推出了更新的指南,旨在解决间充质干细胞 (MSC) 固有的异质性问题。这些指南涵盖了多种分析方法,旨在说明MSC的各种功能特性。这些特性包括营养因子的分泌、免疫细胞的调节及其在血管生成中的作用。
间充质干细胞治疗糖尿病肾病的分子机制
实验研究显示使用间充质干细胞缓解糖尿病肾病具有良好的效果。间充质干细胞是多能细胞,在适当的刺激下可以分化成各种细胞类型,包括肾小球内皮细胞。 MSC归巢至受损肾脏的过程涉及多种分子,包括趋化因子受体、粘附蛋白和基质金属蛋白酶 (MMP) 家族,其中基质细胞衍生因子1 (SDF-1) 及其受体CXCR4在MSC迁移至肾脏损伤部位。
研究发现间充质干细胞对肾脏具有积极作用,可减少各种负面过程,如肾小球大小、足细胞凋亡、肾小球基质扩张/硬化、肾小管周围间质纤维化、肾小管上皮细胞死亡和去分化、肾小管间质纤维化和微血管稀疏。因此,这些影响与白蛋白尿减少(肾脏损伤的迹象)和肾小球滤过率(GFR)的稳定有关,肾小球滤过率是肾功能的关键指标。
间充质干细胞衍生的外泌体及其在糖尿病肾病中的作用
间充质干细胞可以分泌大量包装在细胞外囊泡(外泌体)中的RNA、脂质和多种可溶性因子,并通过其旁分泌功能发挥作用,外泌体具有生物相容性、稳定性、低毒性和有效的生物学能力。分子货物的运输,使它们成为细胞治疗的合适候选者。研究表明,MSCs-Exos可能对神经、呼吸、软骨、肾脏、心脏、肝脏疾病、骨再生和癌症的治疗具有有益作用。与单独的MSC相比,MSC外泌体已表现出优越的治疗和再生效果。
间充质干细胞在糖尿病肾病动物模型中的应用
干细胞治疗的使用作为治疗疾病或替代/治愈受损组织的潜在策略而受到广泛关注。使用链脲佐菌素 (STZ) 诱导的糖尿病 (DM) 的研究表明,间充质干细胞可成功逆转糖尿病小鼠的高血糖并预防肾病。在肾血管性高血压模型中,间充质干细胞治疗通过抑制肾素-血管紧张素系统(RAS)和减少交感神经过度活跃,显着减少血管张力的进行性增加。这是与DKD进展相关的两个过程。
间充质干细胞有潜力解决与DKD相关并导致DKD进展的多种合并症。由于MSC能够改变与DKD相关的风险因素,因此MSC被广泛用于这些可能性。根据美国国立卫生研究院 ( https://clinicaltrials.gov/ )的专家开始招募信息,近十年来,涉及间充质干细胞的细胞治疗在临床前期取得了快速进展。
近年来,基于间充质干细胞的临床试验数量成倍增加。截至2021年7月,Clinical Trials.gov上已完成或正在进行的 1014项基于间充质干细胞的初步临床研究。同样,截至2022年7月,我们搜索关键词“间充质干细胞”来查找综合研究计数。共有1119项研究。在应用“尚未招募”的过滤器后,它显示了69项研究;招聘215名;通过邀请函报名14;主动不招募53;停职16名;终止37;撤回38;状态未知317;和分别完成“343”。 “间充质干细胞”和“糖尿病肾病”的过滤器显示8项研究计数,“招募状态:5项研究”和“未知研究:3项”。截至2023年3月,关键词“间充质干细胞”和“糖尿病肾病”显示,有8项研究计数为“招募状态:3项研究”、“邀请注册:1项研究”和“未知研究:4项”。
截至到2022年只有一项人体临床试验。一项新的人体临床试验(NEPHROSTROM)已经进行,并作为第二次人体临床试验公布了其结果(表4)。根据MSC的类别/来源,过去几年估计的临床前和临床研究数量也如图3所示,这表明迫切需要对人类进行广泛的研究,以预测MSC在这种糖尿病引起的疾病中的作用。并发症,即DKD。考虑到肾谱系中MSC的免疫特权性质,该饼图显示了同种异体/同基因类别中较多的研究。
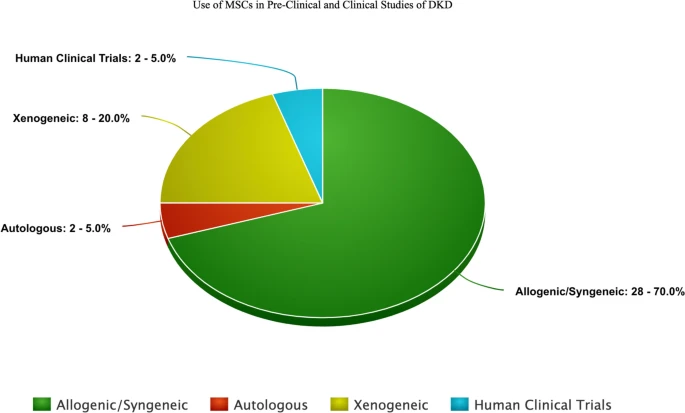
在本概述中,我们对过去基于MSC来源进行的临床前和临床试验进行了总体概述。这凸显了将间充质干细胞转化为DKD人体临床试验的迫切需要。这些动物模型提供了足够的疗效结果,并为研究MSC在DKD人类受试者中的作用奠定了基础。此外,最近有6项临床试验被国家医学图书馆 (NLM) 列为“正在进行中”,如表2所示。
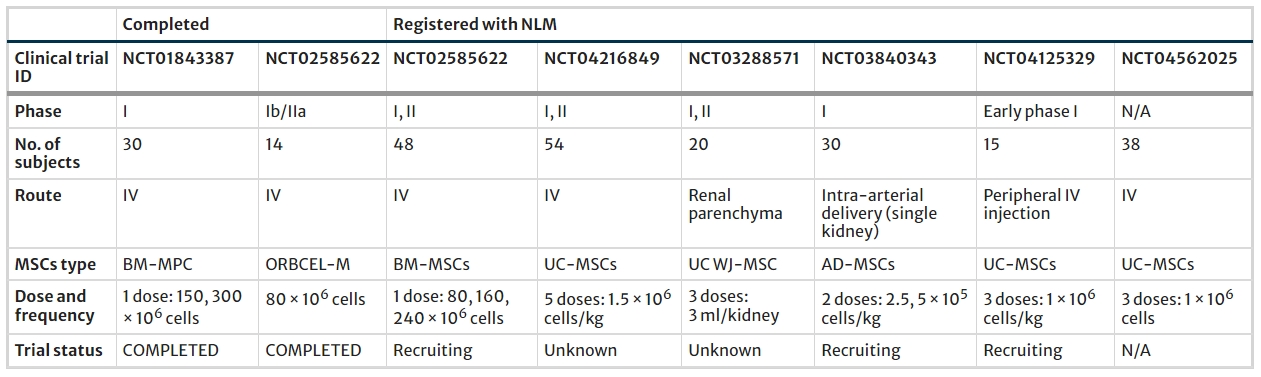
NLM国家医学图书馆、MSC间充质干细胞、BM-MPC骨髓间充质前体细胞、UC脐带、WJ沃顿胶、AD-MSC脂肪源性间充质干细胞
用于监测间充质干细胞在糖尿病肾病进展中的作用的潜在生物标志物
间充质干细胞等细胞疗法在人类受试者中有效转化为糖尿病及其并发症,需要鉴定可测量的生物标志物或因子,作为有利治疗反应的预测因子或早期指标。尿白蛋白排泄增加是进行性DKD风险的关键标志,但其在临床试验中作为未来CKD/ESRD风险替代指标的效用尚不确定。因此,确定潜在的生物标志物来监测 MSC对DKD进展的影响对于成功的治疗结果至关重要。
研究人员一直在研究与DKD病理生理学不断发展的理解相关的个体生物标志物或生物标志物组。促炎细胞因子,包括TNF-α、IL-6、IL-1β和MCP-1,已成为DKD风险和严重程度的可能指标。多项研究报告称,与健康对照相比,糖尿病患者的血清和尿液TNF-α水平升高,这可能与蛋白尿状态和肾功能相关。检查MSC疗法对DKD大鼠肾功能影响的体内模型显示TNF-α水平下降。可溶形式的TNF-α受体sTNFR1和sTNFR2也可能是DKD严重程度的潜在指标。虽然这些生物标志物作为DKD进展和并发症预测因子的临床意义尚未明确确定,但它们有可能作为MSC抗炎作用的生物标志物。需要进一步的研究来验证它们在预测DKD进展和 MSC治疗反应方面的临床有效性。
表3列出了DKD中的新兴生物标志物,这些标志物可以为了解MSC在该疾病的动物和人类模型中的作用机制提供见解。
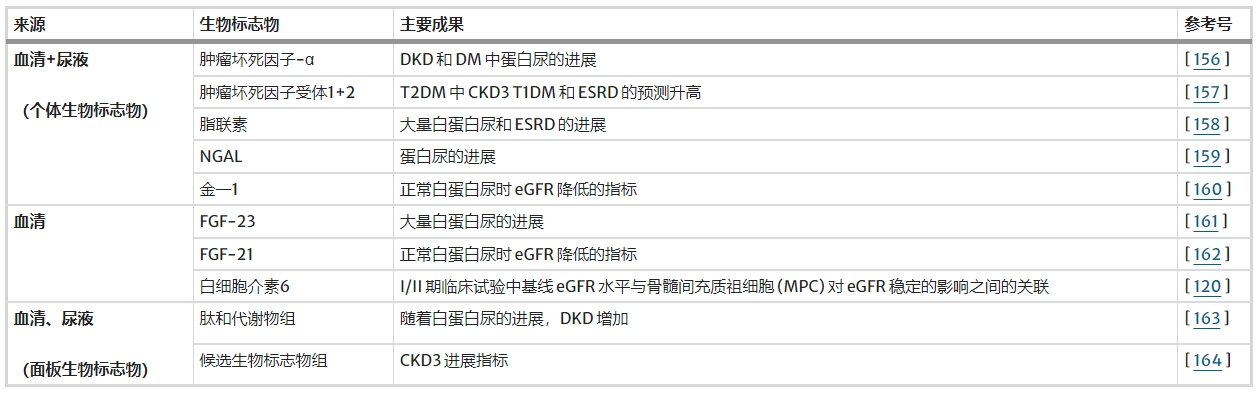
使用间充质干细胞治疗糖尿病肾病的人体临床试验
针对DKD或其他原因引起的间充质干细胞疗法治疗慢性肾病最近才开始进行临床试验,研究仍处于起步阶段。检索三大临床试验注册中心后,仅发现了少数间充质干细胞治疗慢性肾病的临床试验和另外4项非糖尿病CKD的临床试验:WHO国际临床试验注册中心(www.who.int/ictrp/en/)、欧盟临床试验注册中心( www.clinicaltrialsregister.eu/ ) 和美国国立卫生研究院 ClinicalTrials.gov ( www.clinicaltrials.gov )。
临床研究人员目前正在研究间充质干细胞在这种疾病中的再生和临床作用。大量动物和体外研究表明,基于MSC的疗法在治疗DKD方面具有巨大潜力。这些临床试验的结果提供了重要信息,表2列出了后续临床研究(已完成的和正在进行的试验)的研究基础。
2016年完成的一项双盲、剂量递增、序贯的前瞻性随机对照实验 (NCT01843387) 是第一个临床试验。研究人员对30名随机分配的接受间充质前体细胞 (MPC) 或安慰剂治疗的个体的有效性和不良事件进行了追踪。
第二项临床试验,即糖尿病肾病新型基质细胞疗法 (NEPHSTROM),是一项1b/2a期试验,已在三个欧洲站点进行 (NCT02585622)。本研究的简要总结如下。表4显示了两项临床试验的主要特征。
| MSC来源 | 年龄 | DM型 | 样本 | 样本分布 | 注射次数 | 注射方式 | 结果 | 阶段 | 不良事件 (n) | 跟进(米) | 参考号 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 骨髓MPC | 安慰剂:74:8±7:9y,较低剂量MSC:70:5±7:4年 更高剂量MSC:64:8±10:1年 | T2DM | 30 | 150×106/kg(较低剂量)或300×106/kg(较高剂量) | 单剂量 | 四号 | ↔eGFR、蛋白尿↔血脂分析↔血压↔血清C反应蛋白、TNF-α↓血清IL-6 | 一/二 | 没有任何 | 12 | [ 152 ] |
| 骨髓间充质干细胞 | 安慰剂:54–66岁,ORBCEL-M:66–73 岁 | T2DM | 16 | ORBCEL-M(80 ×106细胞) | 单剂量 | 四号 | ↔肾小球滤过率, ↓各组年度mGFR下降↔UACR, ↔安全,=血糖;糖化血红蛋白;血清总胆固醇;血清甘油三酯;和血清C反应蛋白,↑sTNFR1、1NGAL、sVCAM-1、Treg | 1b/IIa | 没有任何 | 18 | [ 153 ] |
↔ 表示任一方向均无重大变化或影响
↓ 表示下降或减少的影响
= 表示稳定性,因为值或参数随时间保持不变或稳定
↑ 表示等级增加
第一项使用间充质干细胞治疗糖尿病肾病的临床研究
这是第一个在T2DM肾功能障碍患者中使用同种异体BM-MSC进行的双盲对照组(安慰剂)试验。从术前诊断后的第二天开始,静脉注射 (IV) 给予指定的治疗剂量。
该研究测量了HbA1c、空腹血糖和胰岛素水平随时间的变化。结果表明,一段时间后这些水平没有显着变化。研究人群的高血糖水平各不相同,HbA1c范围为5.1%至11.2%。研究人群中糖尿病药物的使用情况也存在差异:20%的人服用胰岛素,20%的人服用不同的口服溶液,20%的人同时服用口服溶液和胰岛素,17%的人仅通过饮食来控制糖尿病。此外,23.3%的研究人群仅服用口服药物,通常是磺酰脲类或双胍类药物。研究还提到,专家们被允许在研究期间根据认为适当的情况修改每个受试者的2型糖尿病治疗方案。研究发现,注射(治疗的输注)具有积极的结果,并且每个治疗组的安全性相似。
总体而言,该研究表明 rexlemestrocel-L具有“免疫耐受特性”,这意味着它不太可能引发免疫反应。然而,需要注意的是,这项研究只是一个证据,还需要进一步的研究来全面评估 rexlemestrocel-L 和其他同种异体细胞疗法的安全性和有效性。
第二次临床试验(NEPHROSTROM)
在NEPHSTROM研究的第一个队列中,一项1b/2a期临床试验,探讨了单次静脉输注ORBCEL-M在2型糖尿病和进行性糖尿病肾病 (DKD) 患者中的安全性和耐受性。该干预措施的耐受性良好,只有一名接受安慰剂治疗的患者出现输注反应迅速缓解。重要的是,两名ORBCEL-M接受者在随访期间的死亡被确定与试验研究产品无关,强调了其可接受的安全性。
该研究的临床疗效结果显示,与安慰剂组相比,ORBCEL-M组的估计肾小球滤过率 (eGFR) 下降率显着降低,特别是在使用CKD-EPI和MDRD方程进行评估时。然而,测量的GFR (mGFR) 在各组之间没有表现出显着差异。这些结果表明ORBCEL-M具有潜在的肾脏保护作用。该研究还深入研究了间充质干细胞的免疫调节作用,强调了它们在调节治疗效果方面的作用。ORBCEL-M的接受者表现出持续的免疫调节和抗炎作用,导致细胞特征发生特定变化。这些观察结果表明,ORBCEL-M可以通过影响免疫和炎症反应来调节进行性DKD。
用于其他肾脏病变的自体和同种异体间充质干细胞治疗
截至2023年3月,在“ClinicalTrials.gov”上使用关键词“肾脏”和“间充质干细胞”进行了搜索。 “已完成”的研究过滤器向我们展示了八项研究。
在这些研究中,我们发现了一项利用MSC治疗CKD和狼疮性肾炎的自体研究和同种异体研究。 I期(NCT02195323) 自体试验旨在测量CKD受试者中BM-MSC治疗的耐受性和安全性。这项试验是在一个中心以单臂形式进行的。对符合条件的CKD受试者(n=7)进行18个月的随访期评估。研究药物,即自体骨髓来源的间充质干细胞,通过静脉内途径施用(2×106个细胞/kg)。这项调查的主要结果指标是安全性,通过计数和不良反应进行分析。
第二个焦点是降低eGFR的比率。将随访期间受试者的肾脏组织学与基线、1、3、6、12和18个月进行比较。在实验阶段没有观察到与治疗相关的不良事件。此外,在18个月的随访后, 与基线相比,eGFR ( p=0.10) 和SCr ( p=0.24) 没有观察到统计学显着性。总之,CKD受试者在单剂自体BM-MSC给药中表现出安全性和耐受性。
另一项I期同种异体、介入、非随机平行分配试验 (NCT04318600) 旨在评估hA-MSC的安全性、耐受性和有效性。主要试验终点是在狼疮性肾炎患者中研究的。通过外周静脉注射将hA-MSC给予11名II、III或IV型狼疮性肾炎 (LN) 受试者。输注剂量为1×106个细胞/kg,每月一次,连续输注3次。
同样,五名LN受试者接受了安慰剂(对照组)。所有受试者均未接受静脉注射皮质类固醇脉冲治疗,但允许他们摄入口服皮质类固醇和静脉注射环磷酰胺、饮食吗替麦考酚酯、他克莫司和来氟米特。通过不良反应的数量和严重程度来分析安全性。还观察了基线和治疗后60周的eGFR、24小时蛋白尿偏差和SLEDAI评分。
结论——优点和局限性
该研究探讨了间充质干细胞在治疗糖尿病肾病方面的潜在益处,糖尿病肾病是一个重大的全球健康问题。该综述考虑了调节不同疾病发病机制的各种动物模型和协调干预措施。该研究强调了MSC的旁分泌机制及其减缓或逆转关键致病途径的能力。
作者认为,DKD中的MSC输注可能被视为对糖尿病中发生的慢性肾毒性过程的广泛重新编程,可能会“重新调整反应性患者肾脏病理的时钟”。该研究还表明,间充质干细胞治疗可能会改善血糖控制并促进其他糖尿病终末器官问题。该审查强调了间充质干细胞治疗与生活方式和基于药物的药物相结合治疗DKD的潜力。
参考资料:Habiba, U.E., Khan, N., Greene, D.L. et al. The therapeutic effect of mesenchymal stem cells in diabetic kidney disease. J Mol Med 102, 537–570 (2024). https://doi.org/10.1007/s00109-024-02432-w
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信