
获得细胞治疗产品的定价
瑞士制药巨头诺华公司创造了历史,成为第一家在美国获得FDA批准的CAR-T疗法的公司。诺华公司宣布其转基因自体(“自衍生”)免疫细胞疗法Kymriah的每个疗程费用为475,000美元。此后不久,Kite Pharma宣布其CAR-T疗法Yescarta在美国获得批准,标价为373,000美元。虽然这些价格昂贵,但远非引领潮流。
细胞疗法定价和产品
在本文中:
- 全球获批的干细胞治疗产品有哪些?
- 细胞治疗费用
- 获批细胞治疗产品的定价
- 伤口护理疗法
- 基于软骨的细胞疗法
- 静脉细胞疗法
- 基于细胞的基因治疗
- 干细胞治疗的费用
- 自体与同种异体干细胞移植
- 细胞疗法定价
- 中国干细胞临床治疗进展
全球获批的干细胞治疗产品有哪些?
全球获批上市的干细胞治疗产品:21种
诺贝尔生理学或医学奖获得者Thomas C. Sudhof教授曾表示, “我们可以把疾病进行控制,干细胞是一个非常好的治疗方法”。在传统医学治疗无法解决的问题上,干细胞研究将带来新的希望。”
截至目前,全球共有21种干细胞产品已在全球获得批准,其中12种获得美国FDA或欧洲EMA的批准。其余9种产品主要在亚洲获得批准。值得注意的是,获批产品主要是由造血干细胞或间充质干细胞组成。另外,还有一个角膜缘干细胞产品。
造血干细胞产品:10种
目前全球批准的造血干细胞疗法共有 10 种。其中美国FDA批准8种脐血产品,均用于造血干细胞移植的治疗。欧盟EMA 批准 2 种基于自体造血干细胞的基因疗法,Strimvelis用于腺苷脱氨酶缺乏症,Zynteglo用于治疗输血依赖性地中海贫血症。
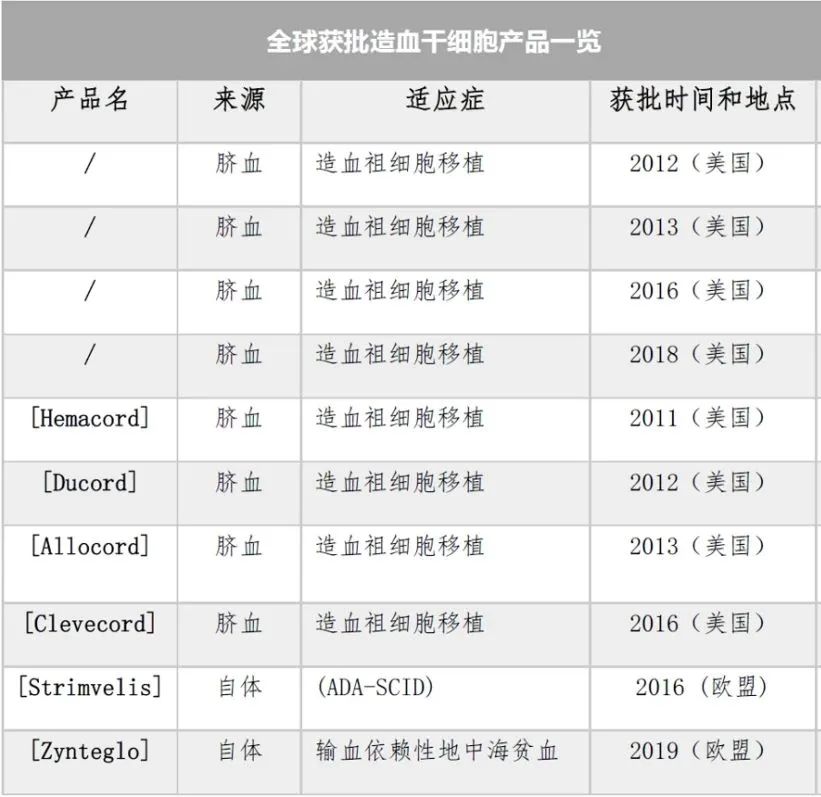
脐血造血干细胞比其他来源的异体造血干细胞更有优势。因为脐血获得更容易,对人类白细胞抗原的耐受性更高,风险较低。
此外,Strimvelis和Zynteglo均是EMA批准的基于自体造血干细胞的基因疗法。
•2016年,EMA批准Strimveli,适用于腺苷脱氨酶缺乏症,一种由腺苷脱氨酶基因编码突变引起的免疫缺陷疾病。
•2019年,EMA批准Zyntegl, 适用于治疗输血依赖性地中海贫血,这是一种由β-珠蛋白基因突变引起的遗传性疾病,导致成人血红蛋白显著减少或缺失。
间充质干细胞产品:10种
目前全球批准的间充质干细胞产品共有 10 种,但没有一款获得美国FDA 的批准。根据作用机制和批准的适应症,MSCs产品可分为两大类:组织修复和免疫调节。
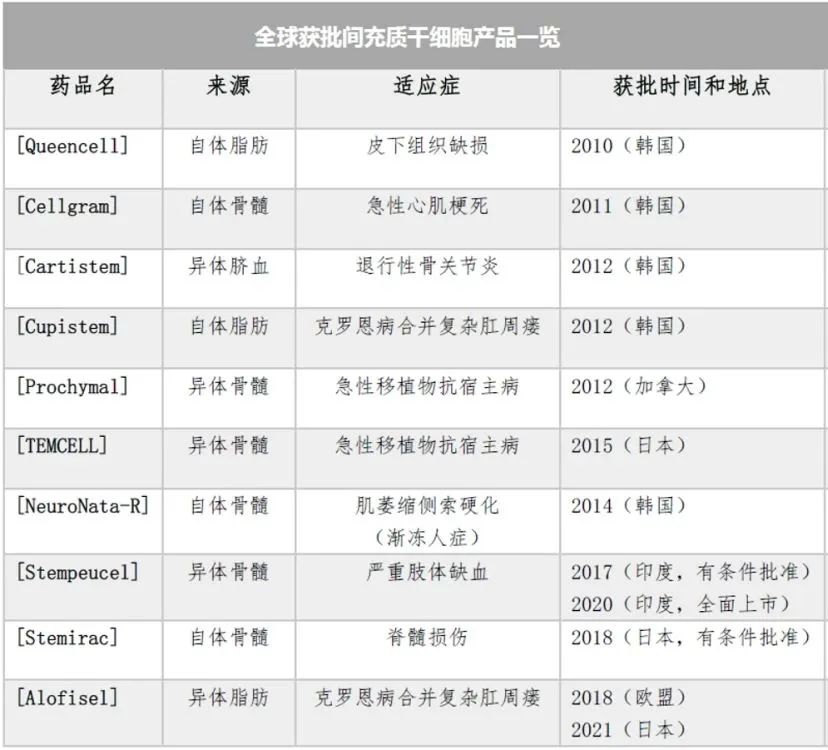
除了已经批准的造血干细胞和MSCs产品外,此外,还有角膜缘干细胞:EMA 2015 年批准的 Holoclar是一种将自体角膜缘干细胞种植于纤维蛋白胶支架上的组织工程干细胞产品,用于治疗眼部灼伤引起的 LSC 缺乏症。
细胞治疗费用
细胞疗法的定价存在争议,因为大多数细胞疗法产品的价格都比传统药物高出数倍。不幸的是,大多数药物都可以大量制造和储存以供现成使用,而细胞疗法涉及活细胞,需要采用不同的方法进行商业规模的制造、运输、储存和患者使用。
迄今为止,价格最高的治疗方法不是细胞疗法,而是基因疗法 (Glybera)。在推出时,Glybera是西方世界批准的第一个基因疗法,在德国上市销售,每次治疗的成本接近100万美元。[1]破纪录的价格标签于2014年 11月公布,当时Uniqure及其营销合作伙伴Chiesi向德国当局提交了一份定价档案,以推出Glybera。不幸的是,Glybera后来因销量不佳而退出欧洲市场。
在Glybera、Kymriah、Yescarta和其他十几种细胞疗法获得批准后,围绕定价和报销的对话已成为细胞疗法行业的焦点。
获批细胞治疗产品的定价
与药物相比,细胞疗法需要不同的定价分析。下面显示了已上市的获批细胞疗法产品的价格标签(以美元为单位的价格),并且有标准化的市场定价。
获批细胞治疗产品的定价:
美国Organogenesis & Novartis AG 的Apligraf =每次使用1,500-2,500美元[2]
美国Genzyme的Carticel=15,000至35,000美元[3]
韩国MEDIPOST的Cartistem=19,000-21,000美元[4] , [5]Anterogen的Cupistem在韩国=每次治疗3,000-5,000 美元[6]。
Tigenix的ChondroCelect在欧盟=~24,000美元(20,000欧元)[7]
美国AdvancedTissue Science的Dermagraft=每次治疗1,700美元[8],
[9]Vericel的Epicel在美国=6,000-10,000 美元/全身表面积的1%[10]HearticellgramFCB-Pharmicell 在韩国=19,000 美元[11]
日本Terumo的HeartSheet=HeartSheetA套件为56,000美元(6,360,000日元);
HeartSheetB试剂盒15,000美元(1,680,000日元)(*每次给药使用一个A试剂盒和 5个 B试剂盒)[12]
欧盟Chiesi Framaceutici的Holoclar=未知(患者人数非常少) 美国诺华公司的Kymriah=每次治疗425,000 美元[13]
美国NuVasive的Osteocel=600美元/cc[14],[15]Osiris Therapeutics 和 Mesoblast 在加拿大的Prochymal = ~ 200,000 美元[16]
美国Dendreon和Valeant Pharma的Provenge=93,000美元[17] ,
[18]CO.DONAG在欧盟的Spherox=9,500 –12,000美元(8,000–10,000欧元)每次治疗[19]GSK在欧盟的
Strimvelis=665,000美元(世界上最昂贵的疗法之一)[20], [21]日本JCRPharmaceuticalsCo. Ltd.的Temcell = 115,000-170,000美元[22]。
*TEMCELL的定价为7,600美元(每袋868,680日元),一袋72m细胞每周给药两次,2m细胞/kg体重每次给药所需[23]。
美国Kite Pharma的Yescarta=373,000美元[24]
伤口护理疗法
如上表所示,伤口护理产品往往具有最低的细胞疗法定价,通常每次使用成本为1,500至2,500美元。例如,Apligraf®由健康人体皮肤中的细胞制成,用于治愈3-4周后仍未痊愈的溃疡(每次使用1,500-2,500美元),而Dermagraft是一种“皮肤替代品”,放置在您的皮肤上溃疡来覆盖它并帮助它愈合(每次应用1,700 美元)。
有趣的是,Epicel是一种治疗全身表面积大于或等于30%的深层真皮或全层烧伤的药物。它的定价更高,为每1%的全身表面积6,000-10,000美元,因为它不是用于治疗单个伤口部位,而是用于治疗患者身体的大面积表面积。
基于软骨的细胞疗法
接下来,基于软骨的细胞疗法产品的中档定价往往在10,000美元到35,000美元之间。例如,Carticel是一种由自体软骨细胞组成的产品(定价15,000至35,000美元),CARTISTEM是一种膝关节软骨再生疗法(定价 19,000至21,000美元),而ChondroCelect 是一种含有软骨细胞的植入悬浮液(定价24,000美元)。2017 年7月,欧洲EMA还批准Spherox作为治疗膝关节软骨缺损的产品,每次治疗的定价为9,500美元至 12,000 美元(8,000欧元至10,000欧元)。
静脉细胞疗法
下一个最昂贵的细胞治疗产品是静脉内给药的产品,价格从大约90,000美元到200,000美元不等。例如,Prochymal是一种静脉内给药的同种异体MSC疗法,来自成人捐赠者的骨髓(定价200,000美元),Provenge是一种静脉内给药的前列腺癌癌症免疫疗法(93,000美元),而Temcell是一种静脉内给药的自体 MSC 产品,用于同种异体骨髓移植后急性GVHD的治疗(定价115,000-170,000美元)。
基于细胞的基因治疗
最后,世界上许多最昂贵的细胞疗法都是基因疗法,价格从500,000美元到1,000,000美元不等。
例如,Kymriah是第一个在美国获得FDA批准的CAR-T细胞疗法(每个疗程定价为475,00美元)。Strimvelis是一种体外干细胞基因疗法,用于治疗患有非常罕见疾病ADA-SCID的患者(定价665,000美元)。
细胞疗法的费用
尽管这些概括并不适用于所有细胞疗法产品,但它们解释了大部分细胞疗法定价,并为估算细胞疗法定价和报销提供了一个有价值的模型。下表总结了此信息。
获批细胞疗法的定价表
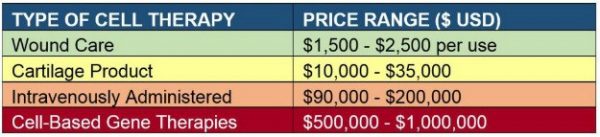
自体与同种异体干细胞移植
另一个参考点也很有价值。RIKEN研究所于2014年将自体iPSC衍生的RPE细胞移植到人类患者体内,启动了世界上第一个涉及iPSC衍生产品的临床试验。虽然该试验后来因安全问题而暂停,但它于2016年恢复,这次使用同种异体iPSC衍生细胞产品。
研究小组表示,通过使用储存的iPS细胞,准备移植所需的时间可以从11个月减少到短短一个月,而目前约1亿日元(889,100 美元)的成本可以减少到1 个月。 -五分之一或更少。[25]
影响细胞疗法定价的因素
虽然影响细胞疗法定价的因素很多,但可用于预测市场定价的关键变量包括:
- 细胞疗法是否涉及基因操作
- 细胞治疗产品类型
- 是自体还是同种异体治疗
另一个复合因素是市场规模,因为伤口愈合和软骨替代疗法有大量的患者群体,而一些更昂贵的疗法只针对较小的患者群体。[26]
中国干细胞治疗临床进展
总体来看,细胞治疗从早期对细胞疗法的质疑,到现在变成一个充满活力的新兴行业,细胞正如雨后春笋般兴起,为诸多难治性疾病提供了一条有效治疗途径。
在免疫细胞临床应用方面,我国已批准两款CAR-T细胞疗法上市,分别是:2021年6月获批上市的阿基仑赛注射液(复星凯特产品)和2021年9月上市的瑞基奥仑赛注射液(药明巨诺产品)。
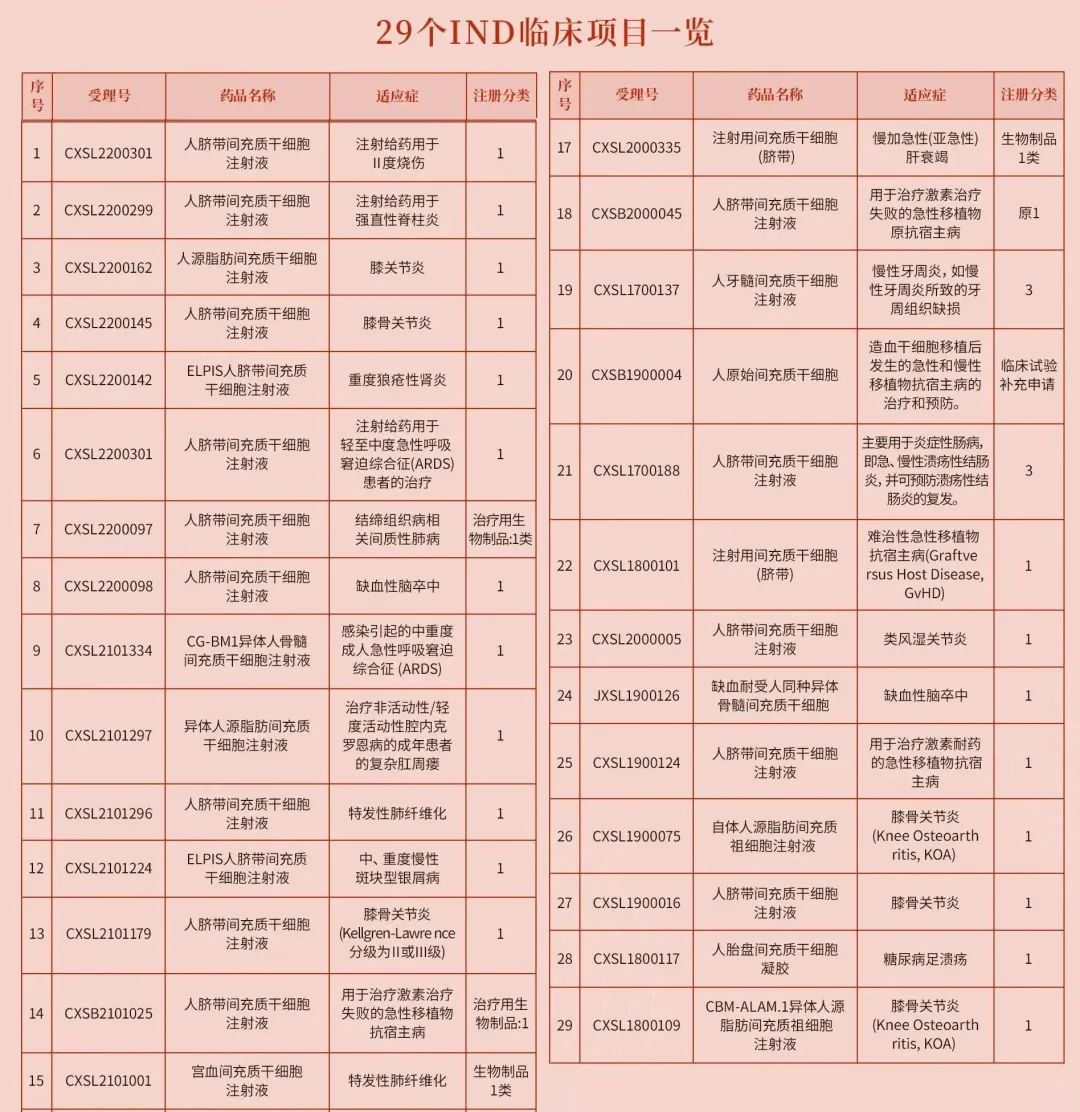
然而,在干细胞临床应用方面根据国家药品监督管理局药品审评中心公示信息显示,截止2022年10月31日,共有29个干细胞新药项目获得国家临床默示许可。分别是胎盘、脐带、牙髓、宫血、异体/自体脂肪来源的间充质干细胞,适应症包括膝骨关节炎、类风湿关节炎、糖尿病足溃疡、银屑病、肺纤维化、肝衰竭、卒中、急性呼吸窘迫综合征、牙周炎、克罗恩病和 GvHD。
我国的细胞治疗拥有广阔的应用市场和较为深厚的科研积淀,加上中央和地方不断出台的利好政策支持,我国的细胞行业已经形成了庞大的市场规模,随着临床转化以及市场的发展,细胞治疗在国内造福患者的时代也将到来。
参考资料:
[1] $1-Million Price Tag For Glybera Gene Therapy: Trade Secrets”. Available at http://blogs.nature.com/tradesecrets/2015/03/03/1-million-price-tag-set-for-glybera-gene-therapy. Web. 21 Aug. 2017.
[2] 2017 Apligraf ® Medicare Product and Related Procedure Payment, Organogenesis. Available at: http://www.apligraf.com/professional/pdf/PaymentRateSheetHospitalOutpatient.pdf. Web. 3 Mar. 2017.
[3] “CARTICEL® (Autologous Chondrocyte Implantation, Or ACI)”. Available at: https://www.painscience.com/articles/cartilage-repair-with-carticel-review.php. Web. 3 Aug. 2017.
[4] Cartistem?, What. “What Is The Cost Of Cartistem?” Available at: http://www.stemcellsfreak.com/2015/01/cartistem-price.html. N.p., 2017. Web. 3 Mar. 2017.
[5] “Cartistem”. Kneeguru.co.uk. Available at: http://www.kneeguru.co.uk/KNEEtalk/index.php?topic=59438.0. Web. 3 Aug. 2017.
[6] Stem Art, Stem Cell Therapy Pricing. Available at: http://www.stem-art.com/Library/Miscellaneous/SCT%20products%20%20Sheet%201.pdf. Web. 3 Mar. 2017.
[7] Are Biosimilar Cell Therapy Products Possible? Presentation by Christopher A Bravery [PDF]. Available at: http://advbiols.com/documents/Bravery-AreBiosimilarCellTherapiesPossible.pdf. Web. 3 Aug. 2017.
[8] Artificial Skin, Presentation by Nouaying Kue (BME 281). Available at: www.ele.uri.edu/Courses/bme281/F12/NouayingK_1.ppt. Web. 3 Mar. 2017.
[9] Allenet, et al. “Cost-effectiveness modeling of Dermagraft for the treatment of diabetic foot ulcers in the french context.” Diabetic Metab. 2000 Apr;26(2):125-32.
[10] Epicel Skin Grafts, Sarah Schlatter, Biomedical Engineering, University of Rhode Island. Available at: http://www.ele.uri.edu/Courses/bme281/F08/Sarah_1.pdf. Web. 31 July. 2017.
[11] Nature. (2011). South Korea’s stem cell approval. [online] Available at: http://www.nature.com/nbt/journal/v29/n10/full/nbt1011-857b.html. Web. 3 Sept. 2017.
[12] Novick, Coline Lee. Translated version of the first two pages of Terumo’s Conditionally Approved HeartSheet NHI Reimbursement Price. [Twitter Post] Available at: goo.gl/YGCh6z. Web. 21 Sep. 2017.
[13] Fortune.com. (2017). Is $475,000 Too High a Price for Novartis’s ‘Historic’ Cancer Gene Therapy? [online] Available at: http://fortune.com/2017/08/31/novartis-kymriah-car-t-cms-price/ Web. 8 Sept. 2017.
[14] Skovrlj, Branko et al. “Cellular Bone Matrices: Viable Stem Cell-Containing Bone Graft Substitutes”. The Spine Journal 14.11 (2014): 2763-2772. Available at: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4402977/. Web. April 12, 2017.
[15] Hiltzik, Michael. “Sky-High Price Of New Stem Cell Therapies Is A Growing Concern”. Available at: http://www.latimes.com/business/hiltzik/la-fi-hiltzik-20151010-column.html. Web. 1 Sept. 2017.
[16] “Counting Coup: Is Osiris Losing Faith In Prochymal?, Busa Consulting LLC. Available at: http://busaconsultingllc.com/scsi/organelles/counting_coup_prochymal.php. Web. 3 Aug. 2017.
[17] “Dendreon Sets Provenge Price At $93,000, Says Only 2,000 People Will Get It In First Year | Xconomy”. Available at: http://www.xconomy.com/seattle/2010/04/29/dendreon-sets-provenge-price-at-93000-says-only-2000-people-will-get-it-in-first-year/. Web. 3 Mar. 2017.
[18] “Dendreon: Provenge To Cost $93K For Full Course Of Treatment | Fiercebiotech”. Available at: http://www.fiercebiotech.com/biotech/dendreon-provenge-to-cost-93k-for-full-course-of-treatment. Web. 3 Mar. 2017.
[19] Warberg Research. CO.DON (CDAX, Health Care). Available at: http://www.codon.de/fileadmin/assets/pdf/03_Investor/Research_Report/2017_07_24_CO.DON_Note_Warburg_Research_englisch.pdf. Web. 21 Sept. 2017.
[20] “GSK Inks Money-Back Guarantee On $665K Strimvelis, Blazing A Trail For Gene-Therapy Pricing | Fiercepharma”. Available at: http://www.fiercepharma.com/pharma/gsk-inks-money-back-guarantee-665k-strimvelis-blazing-a-trail-for-gene-therapy-pricing. Web. 3 Mar. 2017.
[21] Strimvelis”. Wikipedia.org. Available at: https://en.wikipedia.org/wiki/Strimvelis. Web. 13 Aug. 2017.
[22] “Mesoblast’S Japan Licensee Receives Pricing For TEMCELL® HS Inj. For Treatment Of Acute Graft Versus Host Disease”. Mesoblast Limited, GlobeNewswire News Room. Available at: https://globenewswire.com/news-release/2015/11/27/790909/0/en/Mesoblast-s-Japan-Licensee-Receives-Pricing-for-TEMCELL-HS-Inj-for-Treatment-of-Acute-Graft-Versus-Host-Disease.html. Web. 3 Mar. 2017.
[23] “TEMCELL® HS Inj. Receives NHI Reimbursement Price Listing,” JCR Pharmaceuticals Co., Ltd. News Release, November 26, 2015. Available at: http://www.jcrpharm.co.jp/wp2/wp-content/uploads/2016/01/ir_news_20151126.pdf. Web. 3 Mar. 2017.
[24] “Kite’s Yescarta™ (Axicabtagene Ciloleucel) Becomes First CAR T Therapy Approved by the FDA for the Treatment of Adult Patients With Relapsed or Refractory Large B-Cell Lymphoma After Two or More Lines of Systemic Therapy”. Business Wire. Web. 19 Oct. 2017.
[25] “Riken-Linked Team Set To Test Transplanting Eye Cells Using Ips From Donor | The Japan Times”. The Japan Times. N.p., 2017. Web. 23 July. 2017.
[26] LinkedIn Comment, by David Caron. Available at: https://www.linkedin.com/feed/update/urn:li:activity:6316277496551665664/. Web. 21 Sept. 2017.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞不保证信息的准确性和完整性。所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信