间充质干细胞(MSCs)在移植时可以从多种来源获取,主要包括:
进行间充质干细胞移植时,间充质干细胞的来源于哪里?
- 骨髓:骨髓是最常用的间充质干细胞来源之一。这些细胞可以通过骨髓抽吸术收集,这是一种相对简单且安全的手术。
- 脂肪组织:间充质干细胞也可以从脂肪组织中分离,脂肪组织是体内储存脂肪的组织。这些细胞可以通过抽脂手术获取,即使用中空的不锈钢管从体内去除脂肪。
- 脐带组织:间充质干细胞可以从脐带组织中获得,脐带是连接胎儿和胎盘的组织。这些细胞可以在出生时收集并储存以备将来使用。
- 外周血:间充质干细胞在健康成年人的外周血中以少量存在。这些细胞可以通过一种称为单采术的程序收集,类似于献血。
- 胎盘组织:间充质干细胞也可以从胎盘组织中获得。这些细胞可以在出生时收集并储存以备将来使用。
这些来源提供了间充质干细胞的多样性,使得它们在不同的医疗场景中都有可能被使用。
从哪里可以获得间充质干细胞?
间充质干细胞 (MSC) 是具有自我更新能力并表现出多向分化能力的基质细胞。MSCs可分离自多种组织,如脐带、子宫内膜息肉、经血、骨髓、脂肪组织等。
间充质干细胞 (MSC) 是具有自我更新能力并表现出多向分化能力的基质细胞。MSCs可从多种组织中分离得到,如脐带、子宫内膜息肉、经血、骨髓、脂肪组织等。这是因为易于收获和获得的数量使这些来源对于实验和可能的临床应用最实用。
最近,在新的来源中发现了间充质干细胞,例如经血和子宫内膜。可能有更多的MSCs来源等待被发现,MSCs可能是未来实验或临床应用的一个很好的候选者。
间充质干细胞简介
MSC是具有自我更新能力并表现出多向分化能力的基质细胞。MSCs可分离自多种组织,如脐带、子宫内膜息肉、经血、骨髓、脂肪组织等( 图1)。这是因为易于收获和获得的数量使这些来源对于实验和可能的临床应用最实用。最近,许多间充质干细胞来源于新的来源,如经血和子宫内膜。
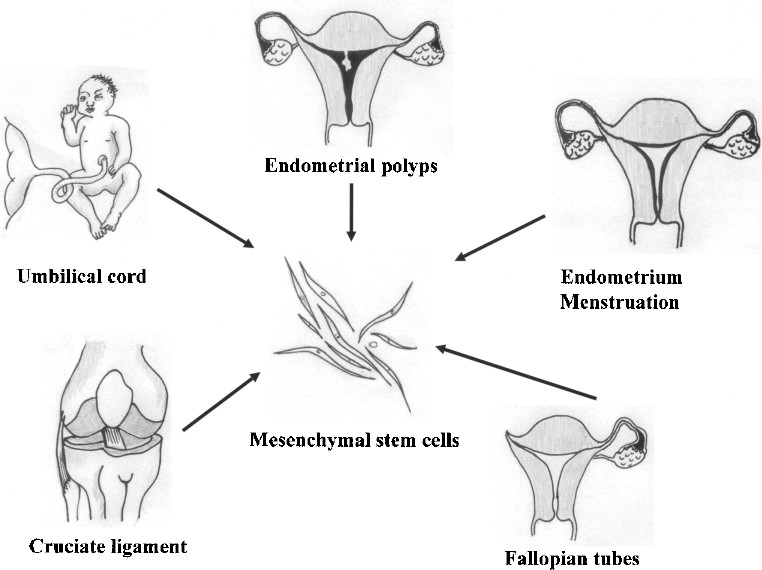
来自月经的MSC
大约400次月经周期发生在女性的育龄期。通常,月经血被丢弃。最近,从月经血中发现了MSCs。这代表了一种新的、无创的、有效的人类MSCs来源,可用于再生医学。大多数来自月经血的MSC具有分化成肌肉的能力,尤其是心肌细胞。这些细胞已被证明具有显着的生肌能力,能够挽救杜氏肌营养不良症或心肌梗死模型的营养不良肌细胞。
因此,来自月经血的间充质干细胞有可能成为一种新的、易于获取的材料来源,用于基于肌源性干细胞的治疗。最近,桑伯格等人显示月经血来源的干细胞可用于大脑修复。
月经来源的 MSCs 可以在体外分化为神经元。这些细胞被用于治疗中风动物模型,并观察到通过似乎不涉及细胞替代的机制的改善。这一发现带来了希望,即月经来源的干细胞不仅是肌源性的,而且是神经源性的,并且可能在未来用于治疗中风。
来自子宫内膜的间充质干细胞
来自人类子宫的子宫内膜是一种高度再生的组织,在女性的生育期经历了400多个脱落、生长和分化周期。干细胞或祖细胞可能在子宫内膜再生中发挥重要作用。Gargett及其同事发现人类子宫内膜含有少量MSC样细胞,这可能是其周期性生长的原因。他们发现CD146是识别这些细胞的良好标记,这可能为组织工程应用提供新的MSC来源。
来自子宫内膜息肉的间充质干细胞
子宫内膜息肉是子宫内膜腺体和间质在血管核心周围的局部增生过度生长,从子宫内膜表面形成无蒂或有蒂的突起。子宫内膜息肉引起月经间期出血、不规则出血和月经过多,可以通过宫腔镜检查发现。由于子宫内膜息肉是子宫内膜组织的良性过度生长,它们可能是MSCs的丰富来源。
我们从子宫内膜息肉中提取了MSC(图2A),显示了传统的MSC表面标记(图2B)。MSC还可以分化成脂肪细胞、成骨细胞和神经源细胞谱系(图2C、D)。它们的增殖速度也快于子宫内膜基质细胞和骨髓基质细胞。我们的研究结果表明,子宫内膜息肉可能具有作为MSCs新来源的潜力。
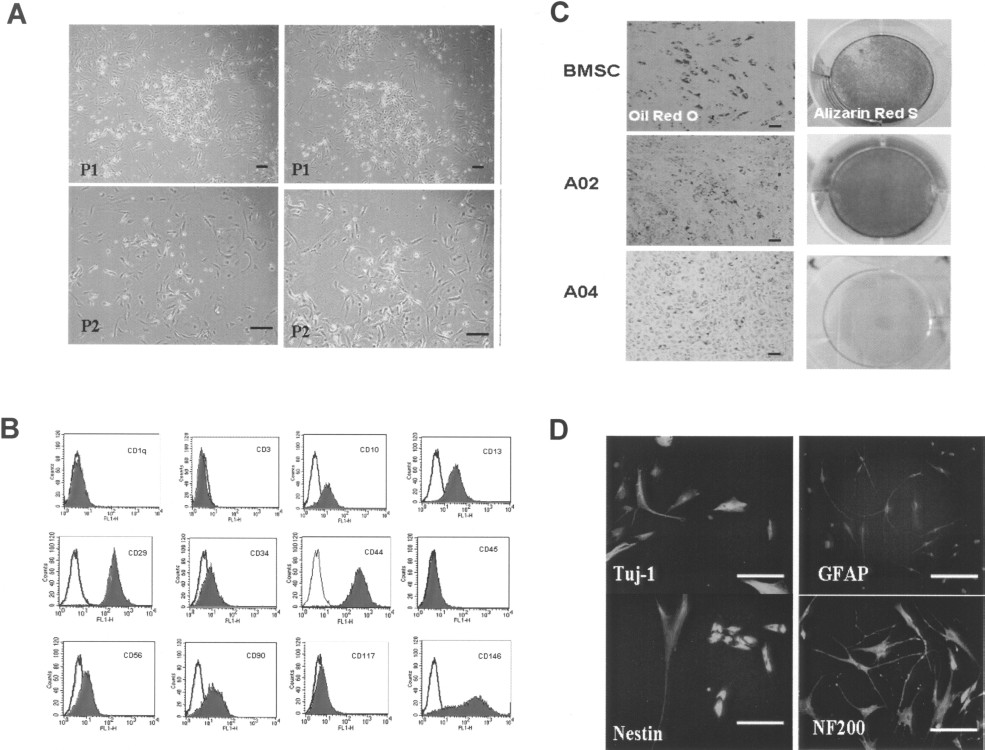
(A) 在增殖培养基中生长的子宫内膜息肉干细胞的代表性照片。
(B) 表达CD13、CD29、CD44 和 CD90 的子宫内膜息肉干细胞的流式细胞术。
(C) 成脂分化显示中性脂泡形成的形态变化,几乎所有细胞都含有大量油红 O 阳性脂滴。成骨分化显示出许多含有矿化基质的分化细胞,这些细胞被茜素红S强烈染色。
(D)在神经胶质细胞分化中,具有扩展的神经突样结构的折射细胞体的形态排列成网络。通过针对巢蛋白、Tuj-1、GFAP和NF200的免疫染色鉴定EPMSCs衍生的神经胶质细胞。
来自输卵管的间充质干细胞
人类输卵管与子宫具有相同的胚胎逻辑起源。它们有能力在月经周期中经历动态内分泌引起的变化,包括细胞生长和再生,以提供维持雄性和雌性配子活力、受精、早期胚胎发育和运输所需的独特环境到子宫。
Jazedje等人最近发现了源自人类输卵管的MSCs。这些细胞可以分化成脂肪形成的、软骨形成的、成骨的和成肌的谱系。他们得出结论,人输卵管间充质干细胞可以很容易地分离和扩增。此外,它们呈现间充质特征并且能够分化。
来自人类十字韧带的间充质干细胞
程等和Ge等人从人类前后交叉韧带 (ACL, PCL) 中发现了MSCs,并发现这些细胞可以分化成软骨细胞、脂肪细胞和骨细胞。这些韧带可以很容易地从全膝关节或十字韧带重建手术后的患者身上获得。他们得出结论,人类 MSCs 可以从 ACL 和 PCL 中分离和扩展,并且可以成为再生医学中使用的可行替代来源。
来自脐带基质的间充质干细胞
最近,干细胞也来源于脐带基质。米切尔等人证明沃顿氏胶 (WJC) 的间充质干细胞可以在体外分化为神经元和神经胶质细胞,并证明脐带沃顿氏胶可能是原始细胞的丰富来源。与BMSCs相比,WJCs具有更大的扩张能力、更快的体外生长,并且可以合成不同的细胞因子,并在神经退行性疾病、癌症、心脏病等多种临床前模型中作为治疗细胞。WJC被认为是MSC的替代来源,值得在长期临床试验中进行检验。
间充质干细胞的分化途径
间充质干细胞分化途径
在特定的体外条件下,MSC可以分化为中胚层、外胚层和内胚层的各种谱系,例如骨骼、脂肪、软骨细胞、肌肉、神经元、胰岛细胞和肝细胞。分化也受遗传事件的调节,涉及转录因子。向特定表型途径的分化(图3)可由一些调节基因控制,这些基因可诱导祖细胞向特定谱系分化。除了生长因子和诱导化学品,用生物材料支架构建的微环境也可以为MSC提供适当的增殖和分化条件。
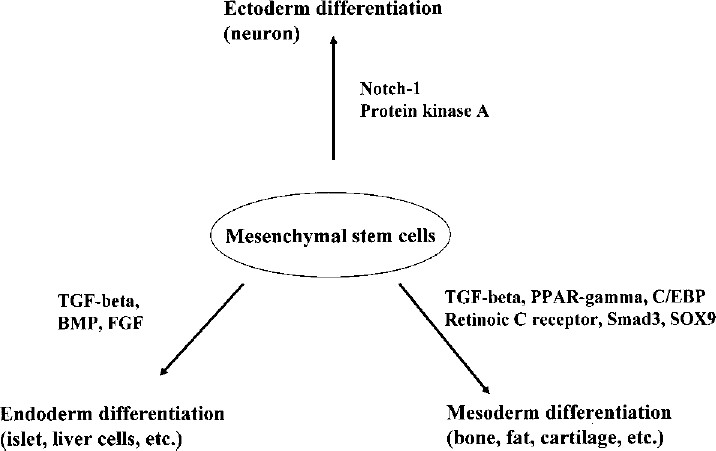
- 中胚层分化
- 外胚层分化
- 内胚层分化
间充质干细胞的动员
已发现几种生长因子、细胞因子和趋化因子可介导MSC的动员。在动物和人体研究中,生长因子VEGF、基质衍生因子1 (SDF-1)、粒细胞集落刺激因子 (GCSF)、粒细胞集落刺激因子 (G-CSF)、粒细胞巨噬细胞集落刺激因子 ( GM-CSF)、促红细胞生成素(EPO)、血管生成素-2、成纤维细胞生长因子、胎盘生长因子(PlGF)、血小板衍生生长因子-CC、干细胞因子(SCF)、白细胞介素(IL)-2、IL-3 、IL-6、IL-8和IL-1β 均已知可刺激和动员MSC。在血管生成和血管生成过程中,由于协同相互作用的生理需要,来自骨髓的造血干细胞 (HSC) 和内皮祖细胞 (EPC) 可能会同时动员。
间充质干细胞的归巢
最近的研究表明,干细胞具有高度迁移性,并且似乎被吸引到大脑病理区域,例如缺血区域,。移植到羊胎中的人类MSC将被植入各种组织(骨髓、脾脏、胸腺、肝脏)。循环造血细胞会主动穿过不同器官的内皮血管系统并进入它们的骨髓壁龛。归巢也是宿主防御和修复的一部分。生长因子、趋化因子和粘附分子是直接归巢效应的信号。MSC可以迁移并归巢于组织和器官。
间充质干细胞的免疫调节
除了多向分化,MSC还具有强大的免疫调节作用,包括抑制T细胞、B细胞和自然杀伤细胞的增殖和功能。了解这些机制和所涉及分子的确切作用将对未来临床应用的发展有巨大帮助,例如干细胞移植或实验应用。
间充质干细胞的前景
寻找新的间充质干细胞来源
除了骨髓,MSCs还可以从人体的各种组织中分离出来。脂肪干细胞可能是一种很有前途的MSC来源,因为它存在于整个人体中。然而,来自胎儿的MSCs,如脐带和血液,将是一个不涉及伦理考虑的良好来源,因为它们在婴儿分娩后被丢弃。月经血和子宫内膜干细胞是其他有希望的MSC来源,因为它们通常在月经或手术后被丢弃。人体中有多种组织可以作为MSCs的潜在来源进行探索。
分化途径和免疫调节的研究
一旦发现了新的 MSC 来源,接下来的挑战就是确定如何区分它们,以便将它们用于临床应用。影响差异化的因素对于确保它们对人类使用是安全的特别重要。对通路了解得越好,MSCs 被操纵成所需类型细胞的可能性就越大。免疫调节是MSC移植中的另一个重要问题。由于机制尚不清楚,因此有必要阐明分子在免疫反应中的作用,这可能决定植入是否成功。
间充质干细胞动员和归巢的未来研究
目前,没有来自检查药物介导的内源性干细胞动员和功能修饰的长期临床研究的可用数据。未来研究的重点之一应该是阐明调节干细胞水平的分子途径以及干细胞的功能和基因修饰,从而提高功能能力。将来有必要开发靶向内皮祖细胞的药理学和遗传学策略。
结论
可能有许多人类MSC来源等待发现。它们可能是未来实验或临床应用的良好候选者。MSCs的分化、动员和归巢机制是复杂的。间充质干细胞的多能性使其成为临床应用的有吸引力的选择。未来的研究应该探索 MSCs在分化、移植和各种疾病的免疫反应中的作用。
参考资料:
1.丁 DC,Shyu WC,Lin SZ。间充质干细胞。细胞移植。2011;20(1):5-14。doi: 10.3727/096368910X
提示:本文内容来自网络用户投稿,仅供参考,不做为诊断依据,任何关于疾病的建议都不能替代执业医师的面对面诊断。最终以医生诊断为准,不代表本站同意其说法,请谨慎参阅,本站不承担由此引起的任何法律责任。




 扫码添加官方微信
扫码添加官方微信