近期,国际期刊杂志“Stem Cell Research & Therapy”发表了一篇“干细胞疗法治疗1型糖尿病的现状:评论与前瞻性思考”的文献综述。在这篇文章中,批判性评价仅限于关键实验结果和相关临床试验。目的是找出在干细胞治疗糖尿病变得可靠和可重复之前必须克服的局限性。作为细胞疗法的替代方案,干细胞衍生细胞外囊泡(EVs)的使用被视为未来的一种可能性。
干细胞治疗1型糖尿病的现状:未来我们期盼什么?

什么是1型糖尿病
糖尿病(DM)是一种代谢性疾病,是一个主要的健康问题。1型糖尿病(T1DM)患者体内胰岛素分泌不足,而2型糖尿病(T2D)患者则无法利用胰岛素。与1980年的1.08亿人相比,2014年全球有超过4亿人患有糖尿病。如果这一趋势持续下去,预计到2045年,这一数字将增至6亿多。其中,T1DM约占10%。

1型糖尿病的发病机制涉及自身免疫介导的对胰岛中产生胰岛素的β细胞的破坏。支持T1DM发病的自身免疫基础的证据包括胰岛周围和胰岛内出现淋巴细胞浸润,以及出现针对多种胰岛自身抗原的自身抗体。随着β细胞数量的减少,胰岛素分泌也随之减少,直到可用的胰岛素不足以维持正常的血糖水平。外源性胰岛素是治疗T1DM患者的主要方法。虽然胰岛素治疗可以维持适当的血糖控制,但在许多患者中却无法预防微血管并发症。
此外,胰岛素输送不准确会导致血糖控制不佳和/或低血糖。胰岛移植可以有效治疗T1DM患者。尽管效果良好,但胰岛移植的主要问题是需要免疫抑制和供体稀缺。另外,干细胞衍生的胰岛素分泌细胞可以提供无限的供应。
为此,胚胎细胞、新生儿细胞、诱导多能细胞和间质/基质细胞治疗1型糖尿病的临床应用已有报道,并成为多篇系统综述的主题。
多能干细胞与1型糖尿病
人类多能干细胞(hPSCs)包括胚胎干细胞(hESCs)和人类诱导多能干细胞(hiPSCs)。胚胎干细胞(hESCs)来源于胚胎内部细胞团,而人类诱导多能干细胞(hiPSCs)则是通过体细胞重编程产生的。然而,与hESCs相比,使用hiPSCs需要考虑的伦理问题更少。此外,hiPSCs还提供了使用自体细胞的机会,因此可以避免异源免疫反应。一些研究报道了hESCs和hiPSCs之间的一些差异。这些差异包括基因表达谱、DNA甲基化等表观遗传修饰和遗传稳定性。
人类多能干细胞分化产品的临床移植
hESC衍生的IPC移植面临两大挑战:免疫原性和致畸性。因此,这些细胞的移植需要将它们封装在免疫隔离装置内和/或使用免疫抑制剂。为此,ViaCyte开发了一种免疫保护装置。该装置装载有源自hESC的PEC。数据表明,皮下移植这种组合[VC-01TM]可以控制啮齿类动物化学诱导的糖尿病。
完全分化的IPC由Vertex Pharmaceutical Incorporated(美国马萨诸塞州波士顿)从同种异体多能干细胞开发而来。在I/II期开放标签临床试验(NCT04786262)中,纳入了两名低血糖意识受损的1型糖尿病患者。IPC被移植到门户系统中。还必须给予免疫抑制剂。
Vertex公布了第一名患者的早期令人印象深刻的数据。第270天,患者实现胰岛素独立,HbA1c水平为5.2%。第二位患者的结果则没有那么好。到第150天,外源胰岛素需求仅减少了30%,HbA1c变为7.1%。不过,结果尚未公布。目前,Vertex计划再招募17名患者。这种治疗的缺点是必须进行免疫抑制。实际上,频繁施用胰岛素与使用免疫抑制剂之间存在权衡。
相关阅读:
- 新数据显示新型干细胞细胞疗法(VX-880)对1型糖尿病胰岛素、血糖管理有希望治疗1型糖尿病!
- Vertex干细胞疗法获FDA批准临床
- 哥伦比亚大学报道最新干细胞治疗1型糖尿病的临床试验结果:能够帮助控制血糖
间充质干细胞治疗1型糖尿病
间充质干细胞可以通过多种机制发挥其治疗作用。它们可以定位损伤部位并支持胰岛的修复。间充质干细胞还增强胰岛移植物血管化。通过其免疫调节功能,它们可以为早发T1DM提供治疗手段。受这些有前景的特性的推动,多项临床试验对MSC治疗DM的用途进行了评估。
- 胡等人将29名患者随机分组如下:15名接受沃顿胶衍生间充质干细胞静脉注射,14名接受常规治疗并作为对照。作者报告称,接受间充质干细胞治疗的患者的平均C肽水平有所增加,胰岛素需求量有所下降。
- Carlsson及其同事在10名患者中使用了自体骨髓来源的间充质干细胞。研究人员报告称,在1年的随访中,混合膳食耐受性测试中的C肽反应有所增加。
- 在Araujo及其同事的一项试验中,13名患者被随机分配如下:8名接受同种异体AT衍生的MSC和维生素D,5名作为对照。干预三个月后,MSC治疗组的胰岛素需求量和HbA1c水平较低。
- 伊扎迪等人用自体骨髓来源的间充质干细胞治疗了11名患者。他们报告说,早期诊断的T1DM中的间充质干细胞治疗改善了HbA1c和C肽水平。还观察到促炎细胞因子向抗炎细胞因子的转变。
- 卡尔森等人使用脐带间充质干细胞治疗10名早发性T1DM患者。他们报告说,治疗组的胰岛素需求量没有变化,而对照组的胰岛素需求量中位数增加了10单位/天。他和同事最近报告了对随机对照试验进行彻底系统回顾和荟萃分析的结果,这些试验测试了MSC在糖尿病患者中的临床疗效和安全性。
这些作者确定了176篇全文论文。然而,169项研究被排除在外,因为它们涉及非人类实验或没有随机化和对照。据报道,间充质干细胞输注改善了HbA1c水平,但空腹血糖或C肽水平没有显着差异。尽管这些研究证明全身性间充质干细胞给药对于治疗早发性1型糖尿病具有潜在益处,但仍存在大量不确定性,无法得出最终结论。间充质干细胞来源不均匀,细胞剂量可变且患者数量有限。鉴于这些局限性,需要进行大量高质量、大规模随机研究才能提供明确的结论。
为了利用其免疫调节功能,最近的一些报告将间充质干细胞与胰岛联合移植。王等人。从三名计划接受胰岛自体移植的慢性胰腺炎患者身上采集骨髓来源的间充质干细胞。通过门静脉将胰岛与间充质干细胞共同移植。作者报告说该过程是安全的。与对照组相比,患者的12个月空腹血糖水平较低,生活质量较好。
干细胞疗法治疗1型糖尿病的挑战和局限性
多能干细胞衍生的IPC面临两个重要问题:异体免疫反应及其肿瘤发生的可能性。
将其封装在免疫隔离装置中或使用免疫抑制是必要的。封装有其固有的缺点。需要进一步改进现有的封装系统。必须避免细胞缺氧,并确保有足够的血管。还必须尽量减少异物组织反应引起的囊周纤维化。如果这些问题得不到解决,在封装装置内进行细胞移植将很难取得令人满意和有意义的结果。终生需要使用免疫抑制剂会产生严重的副作用。此外,一些已使用的免疫抑制剂会导致糖尿病。表1概述了干细胞衍生的IPC。
| 起源细胞 | 分化实验方案 | 分化所需时间(天) | 差异化产品 | 临床试验 | 移植部位 | 封装 | 免疫抑制 |
|---|---|---|---|---|---|---|---|
| 胚胎干细胞 | [ 11 , 12 ] | 14 | 胰腺祖细胞 | 是 [ 19 ] NTC:02239354 | 皮下 | 是(VC-01) | 不 |
| 多能干细胞 | [ 13 , 15 , 16 , 17 ] | 14 | 胰腺祖细胞 | 是 [ 21 , 22 ] | 皮下 | 是(VC-02) | 是的 |
| 多能干细胞 | [ 8 , 98 ] | 30–36 | 胰岛素产生细胞 (VX-880) | 是的* | 门户内 | 不 | 是的 |
| 间充质基质/干细胞 | [ 61 , 63 , 64 , 65 , 66 ] | 10–21 | 产生胰岛素的细胞 | 不仅仅在啮齿动物中进行实验 [ 61 , 65 ] | 肾被膜下 | 不 | 不 |
最后,无论干细胞来源的IPC的来源如何,都必须解决其他问题。必须量化实现胰岛素独立所需的细胞数量,并且还应确定它们的功能寿命。
前景:间充质干细胞衍生的外泌体?
细胞外囊泡(EVs)是细胞(包括间充质干细胞)自然释放的膜囊泡。它们被包裹在脂质双分子层中,由于不含功能性细胞核,因此无法复制。大小在30-100nm范围内的EV被称为外泌体(exosomes),该术语由Trams等人提出。外泌体是唯一一类已知由内泌体通过内泌体膜内陷形成多泡体(MVBs)而衍生的EVs。外泌体通过多囊体与质膜的融合释放出来。
相关阅读:
众所周知,外泌体是细胞物质从分泌细胞到受体细胞的单向输送器,可调节受体细胞的功能。这可以通过接触信号、外泌体在靠近信号源的地方释放或内分泌信号来实现,外泌体随后通过血液进行系统运输,向远端发挥作用。因此,间充质干细胞衍生的外泌体已作为一种无细胞疗法用于治疗各种病症。
间充质干细胞衍生的外泌体与糖尿病
作为细胞疗法的替代方案,MSC衍生的外泌体在治疗DM中的潜在作用已在多项实验研究中得到探索。
He等人从人脐带干细胞中制备外泌体。他们通过使用高脂肪饮食并随后给予链脲佐菌素(STZ)在大鼠中建立了T2DM模型。通过尾静脉静脉注射外泌体,剂量为10mg/kg,溶于200μlPBS,每3天一次,持续2个月。施用外泌体或植入人MSC后血糖水平显着降低。腹膜内葡萄糖耐量试验(IPGTT)和腹膜内胰岛素耐量试验(ITT)显示,外泌体给药改善了葡萄糖代谢并增加了胰岛素敏感性。此外,外泌体处理后自噬相关蛋白增加。作者认为外泌体通过促进自噬改善葡萄糖和脂质代谢。
EV作为细胞疗法的替代品
关于利用EVs诊断和治疗糖尿病或其并发症的临床前研究已成为多篇综述的主题。
2014年,ClinicalTrials.gov仅发布了一项临床试验(NCT0213833)。自那以后,没有公布或报告任何结果。
与此同时,干细胞疗法的经验很普遍,并在不断优化。然而,使用外泌体可避免细胞疗法的几个相关问题,特别是坏死和免疫排斥反应。由于外泌体没有细胞核,因此不会致畸。外泌体可以储存,并可作为现成的治疗工具及时提供。外泌体通过静脉注射给药,无需侵入性程序即可重复使用。此外,外泌体具有自主靶向能力,可被设计为特定分子的载体。然而,由于缺乏制备或表征EVs的标准化方法,EVs的治疗应用具有挑战性。此外,作为外泌体生产来源的间充质干细胞是异质性的。
因此,制备的样本可能包含多种EV亚型的混合物。Witwer等人强调,有必要将国际细胞治疗学会提出的鉴定间充质干细胞的最低标准和国际细胞外囊泡学会的建议(2018年更新)结合起来。通过这种方式,可以确定制备和表征EVs的框架。由于间充质干细胞衍生的EVs尚未实现全球标准化,因此应使用可重复的检测方法,通过物理、生化和功能属性来定义最终产品。
总结
过去十年,干细胞治疗糖尿病取得了重大进展。然而,在可靠地利用细胞疗法治疗糖尿病之前,仍有一些障碍和挑战需要克服。
我们的目标是在没有封装、免疫抑制或基因操作的情况下成功进行细胞移植。为实现这一目标,使用间充质干细胞衍生的IPC带来了一线希望。与ESCs和iPSCs相比,间充质干细胞的致畸风险微乎其微。实验证据表明,异基因移植这些细胞不会引起免疫反应,这可能是基于未分化群体的免疫调节功能。间充质干细胞衍生的IPC可进一步增强免疫调节功能,以克服T1DM患者的自身免疫反应。间充质干细胞临床应用的缺点是其异质性,这取决于其获取来源以及供体之间的差异。
目前正在尝试将其标准化。皮下组织是细胞移植的最佳部位。但必须解决血管通透性差的问题。目前,我们的实验室正在测试间充质干细胞衍生的IPC皮下移植模型。细胞被移植到纤维蛋白基质中。此外,我们还同时移植了一个小型支架用于药物输送(图1)。
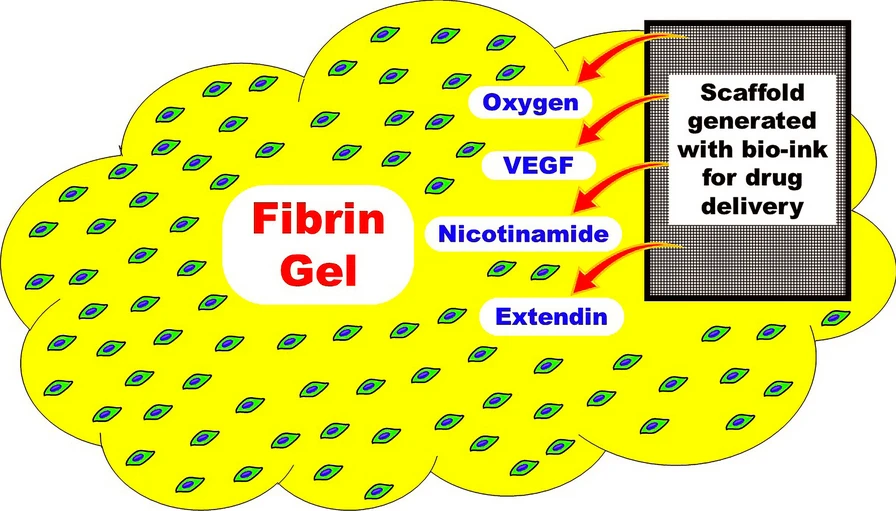
细胞被移植到生物基质内。共同移植一个小支架用于药物输送。氧气满足即时需求,VEGF诱导早期血管形成,烟酰胺保持胰岛活力,Exendin促进体内进一步分化
外泌体是一种令人兴奋的治疗选择。我们认为,与源自未分化MSC的外泌体相比,源自IPC的受过改造的外泌体可能提供更好的治疗效果。我们的实验室正在进行探索这一概念的实验(图2)。
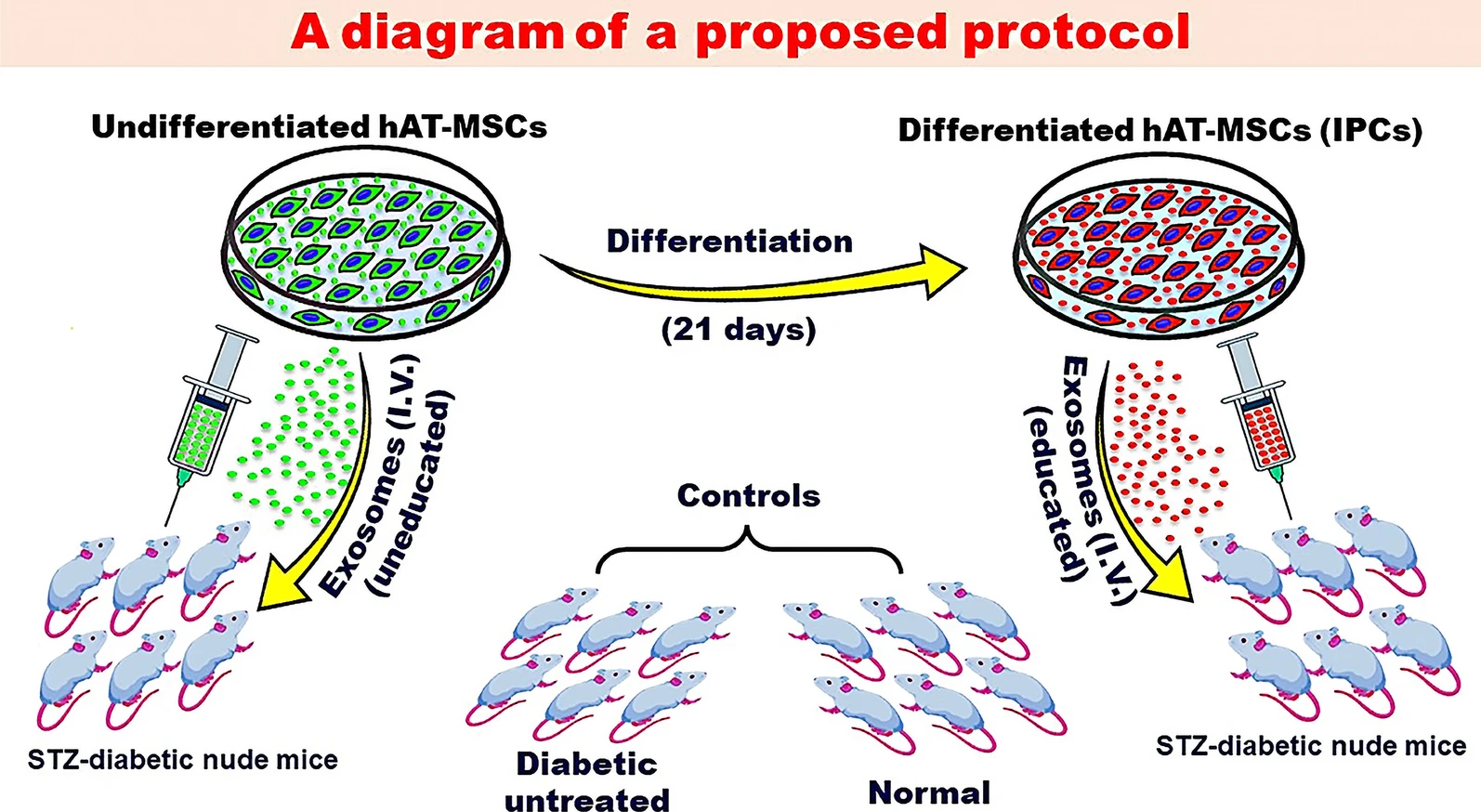
外泌体从幼稚MSC(未受改造的外泌体)或分化的IPC(受教育的外泌体)的条件培养基中回收,并静脉注射到STZ糖尿病小鼠中。结果与肾被膜下细胞移植进行比较
最后,必须强调的是,只有当功能结果优于新发现的药物或不断改进的闭环胰岛素泵时,细胞或外泌体疗法对胰岛素依赖型糖尿病患者才有意义且具有临床合理性。
参考资料:Ghoneim, M.A., Gabr, M.M., El-Halawani, S.M. et al. Current status of stem cell therapy for type 1 diabetes: a critique and a prospective consideration. Stem Cell Res Ther 15, 23 (2024). https://doi.org/10.1186/s13287-024-03636-0
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 扫码添加官方微信
扫码添加官方微信