激素疗法、辅助生殖技术和再生医学已被用于治疗卵巢功能不全 (POI) 引起的不孕症,但收效甚微。现在是时候通过概述POI患者进化干细胞 (SC) 疗法的争议和前景来对该领域进行调查了。
我们首先讨论组织源性SC治疗和诱导/工程SC治疗的几种策略,然后列举机制,包括在生殖组织中诱导的细胞再生能力和由各种趋化因子诱导的旁分泌作用。接下来,我们评估了基于SC的组织工程在逆转卵巢衰老方面的潜在益处。最后,我们讨论了干细胞疗法和广义再生医学治疗卵巢功能不全的临床可行性。
总之,干细胞疗法和干细胞衍生的外泌体,诱导多能干细胞、工程干细胞和组织工程可以为卵巢功能不全患者的生育康复开启新篇章。揭示潜在的分子机制和生物学功效不仅可以通过动物实验来促进,还可以通过安全筛选和临床试验来验证干细胞治疗卵巢早衰的可行性。
介绍
女性自然绝经的平均年龄约为48-51岁。卵巢功能不全 (POI) 也称为卵巢早衰 (POF),是指在月经来潮前因卵巢功能丧失而停止月经。
POI女性的特征是无排卵、雌激素缺乏和原发性或继发性闭经。
诊断主要基于血清促卵泡激素水平升高(>40IU/L,等于绝经期范围)。
POI分为三个临床阶段(隐匿性、生化和显性),而POF在第三阶段得到更好的解释。这种疾病具有高度异质性,具有广泛的致病原因,包括遗传、自身免疫、代谢(半乳糖血症)和医源性(抗肿瘤治疗)。
目前,POI的治疗包括激素替代疗法、卵母细胞冷冻保存、体外激活和再生医学等。由于荷尔蒙的副作用,患乳腺癌的风险。最近,体外激活已成为治疗POI不孕不育患者的一种有前途的策略;然而,Akt刺激药物对卵母细胞的负面影响仍不确定。
细胞、组织和器官修复技术已被开发用于治疗器官功能障碍;因此,一种称为再生医学的替代治疗方法蓬勃发展,如图1所示。再生医学的一些关键组成部分是干细胞 (SC),干细胞可分为胚胎干细胞和成人干细胞。他们的发展阶段。在后者中,间充质干细胞 (MSC) 由于其低免疫原性而具有治疗POI的潜力。有几种类型的MSC,包括骨髓间充质干细胞 (BMSC)、脂肪来源的间充质干细胞 (ADSC) 和外周血单核细胞。尽管越来越多的证据表明SC在动物POI模型中有效,SCs在POI管理中的功效基础机制仍有待阐明。

临床前研究和临床试验已使用各种干细胞和祖细胞群来测试它们在治疗应用中的功效。此外,干细胞还可以分泌一些外泌体,这些外泌体可以通过转移microRNA、酶和其他一些生物活性分子来发挥旁分泌功能。正在探索下一代方法,包括体外植入重新编程的工程干细胞以优化表型。工程仿生生殖组织(例如封装在支架中的毛囊)的再生能力仍在评估中。
在这项研究中,我们研究了用于治疗卵巢功能障碍的干细胞类型有哪些和工程化的组织特性、潜在的内在机制以及干细胞治疗的最新临床前和临床进展。我们的讨论表明,干细胞疗法在逆转POI诱发的不孕症方面具有潜在的治疗效果。
方法
使用PubMed搜索了截至2023年5月发表的与POI相关的基于SC的治疗的原始文章。关键词组合包括“卵巢早衰”、“卵巢功能不全”、“干细胞”、“干细胞疗法”、“再生医学”和“工程组织”。我们专注于SC在POI管理中的潜在机制的研究或调查。在适当的情况下,还搜索了参考列表以查找更多相关报告。本研究共鉴定并评估了128篇文章。确认的文章仅限于全文英文论文。
结果
干细胞的特性
治疗卵巢早衰的干细胞类型有哪些?
骨髓间充质干细胞:BMSCs是一种多能成人SCs,可在骨髓微环境中找到。在一定条件下,这些细胞可以分化成各种细胞,如脂肪细胞、软骨和骨骼。
由于主要组织相容性复合物II类分子的最低表达和许多抗炎因子的分泌,BMSCs具有低免疫原性。此外,BMSCs可以作为组织修复的候选者,因为它们具有迁移和回到受伤部位的能力。它们通过各种细胞因子谱调节免疫反应和增强相关细胞的功能,积极参与组织损伤修复。
脂肪来源的间充质干细胞:ADSC是存在于脂肪组织中的另一种多能MSC。这些细胞可以通过胶原酶消化和离心密度梯度分离从处理过的脂肪抽吸物中成功分离,这是一种比其他来源(例如BMSC)更痛苦的收集过程。
ADSCs在再生医学中的最初应用主要集中在它们沿内胚层、外胚层和中胚层谱系的分化潜能。此外,它们对各种细胞因子、趋化因子和生长因子发挥旁分泌作用的能力能够实现受损细胞的自我修复。
月经血来源的基质细胞(MenSCs);卵原干细胞/雌性生殖系干细胞:一些SC独特地来源于女性,包括月经血衍生的基质细胞 (MenSC) 和卵原SC (OSC)。由于MenSC易于获取且无创,因此已被用于多项研究。考虑到它们的分化能力和可塑性,我们建议MenSC可以帮助设计新的不孕症治疗方法。
人羊膜间充质干细胞、脐带间充质干细胞、人胎盘间充质干细胞:在产前期间可以分离出几种类型的SC。母胎物质,包括羊膜、脐带和胎盘,是MSCs的来源。羊水SCs和人羊膜上皮细胞通常被称为人羊膜来源的MSCs (hAD-MSCs)。
婴儿出生后,脐带MSCs保持非常低的免疫原性;在源自脐带的MSCs中,源自脐动脉的血管周围SCs (PSCs) 比源自脐静脉的PSCs或沃顿胶质衍生的MSCs表现出更高的Notch配体Jagged1表达, 这表明它们有前途的血管生成潜力。人胎盘来源的MSCs (hPMSCs),也称为人绒毛膜板来源的MSCs,通常用于卵巢功能的重建。hPMSC已被证明可以分泌多种细胞因子,包括粒细胞集落刺激因子、趋化因子(CC基序)配体5和IL-6/-8/-10。
诱导多能干细胞:诱导多能干细胞(iPSC)的首次成功衍生发生在2006年。 研究人员将四种转录因子Oct4、Sox2、C-Myc和Klf4引入体细胞并获得了iPSC。尽管已经报道了iPSC可能存在的风险,例如遗传和表观遗传异常,以及由于c-Myc等癌基因的过度表达而增加的癌症风险,但iPSC仍然具有恢复卵巢功能的巨大潜力。
工程化的干细胞:基因编辑技术可用于生产与其自然特性相比具有高级功能和特异性的SC。这些工程方法将有助于深化下一代SC的价值和临床适用性。
MSCs的基因修饰是通过转染各种载体来优化表型来实现的。首先,敲除人类白细胞抗原基因可以降低同种异体SC的免疫原性,并提供通用供体细胞的潜在来源。其次,修饰的MSC可以显着改善靶向迁移。第三,工程化的 MSC 能够过度表达细胞因子和生长因子以增强组织修复。例如,治疗可能包括转染 microRNA (miR)-21慢病毒载体、质粒或磷酸血管内皮生长因子 (pVEGF) 以过表达某些调节因子和热休克预处理以增强MSC的活力。
干细胞来源的外泌体:最近的一项研究表明,MSC可以分泌外泌体,外泌体作为多种生物活性分子的货物,包括酶、mRNA、tRNA、miR和热休克蛋白[图2]。外泌体可直接影响细胞间通讯和信号转导,从而调节细胞的生物学行为。外泌体可作为脱细胞治疗的理想选择,因为它们可降低肿瘤形成或在MSC期间植入异位组织的风险移植及其广泛的来源和容易获得。研究表明,MSC外泌体通过植入miR-644-5p和miR-10a等功能性miRNA,在POF小鼠模型中抑制化疗诱导的颗粒细胞 (GC) 凋亡。

潜在的治疗效果
根据干细胞类型列出了干细胞治疗的临床前研究 [补充表1]。在补充表2中提到的临床研究中,大多数包括促卵泡激素水平>20或25IU/l、年龄在40岁以下、临床诊断为POI的患者。我们总结了针对POI的下一代基于SC的疗法,包括使用iPSC、工程SC、外泌体和工程组织进行治疗。
总之,干细胞移植后次级、初级和原始卵泡的数量增加,卵巢质量改善。此外,雌二醇和抗苗勒管激素的血清水平升高,而卵泡刺激素水平随着雌二醇水平的升高而降低。这些结果表明卵巢功能的恢复。然而,需要更好地阐明渐进表型的潜在机制。
干细胞治疗卵巢早衰的作用机制研究
干细胞的分化特性:SC倾向于迁移到受损的组织部位,这会刺激卵巢恢复。多种趋化因子和生长因子受体,例如(CC基序)配体5、血管细胞粘附分子-1、IL-8受体、肝细胞生长因子 (HGF)、P-选择素和基质金属蛋白酶(MMP;MMP-2)在许多研究中,这些细胞分化成其他细胞类型(例如脂肪细胞、成骨细胞、神经元和内皮细胞)的能力已在体内和体外。一项研究表明,卵巢来源的间充质样SCs具有高度可塑性,可以分化成成骨组织和软骨形成组织以及原始生殖细胞的前体。
干细胞的旁分泌作用:人们普遍认为,SC的恢复作用更多地依赖于旁分泌活动,而不是多能分化[图3]。SC的旁分泌活动是指它们分泌趋化因子、生长因子、激素和其他生化信使来调节相邻细胞的能力。旁分泌信号通过触发血管生成、抗炎、免疫调节、抗细胞凋亡和抗纤维化途径。
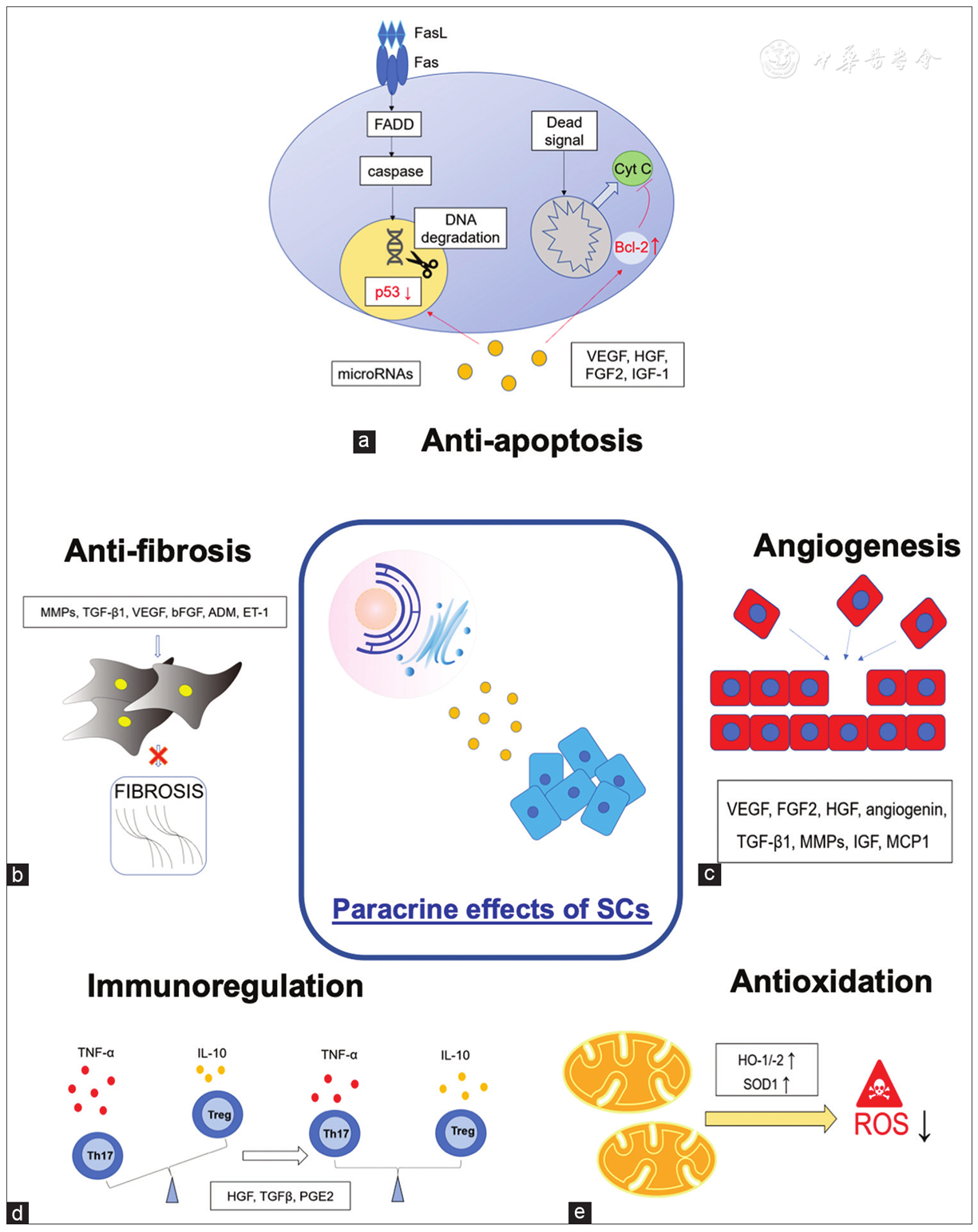
(a) GC 的凋亡受到细胞因子、微小 RNA、转录调节因子和基因的活性的抑制。细胞因子包括 VEGF、HGF、FGF2和IGF-1。(b) MMPs、TGF-β1、VEGF、bFGF、ADM 和 ET-1 可以保护卵巢免受纤维化。(c) 增加VEGF、FGF2、HGF、血管生成素、TGF-β1、MMP、IGF 和 MCP1 的分泌促进目标血管的血管生成。(d) 分泌HGF、TGF-β和PGE2调节T辅助细胞17和T调节免疫细胞的比例。(e) HO-1/-2的规管表达改善氧化应激,导致SOD1增加和ROS水平降低。
抗凋亡作用:当10%的GCs发生凋亡时,卵泡会发生闭锁。多项研究表明,不同的MSCs在化疗引起的卵巢毒性中具有保护和再生作用,SCs 的抗凋亡机制与某些细胞因子、外泌体miRNA、转录生长因子,包括 VEGF、HGF、成纤维细胞生长因子 2和胰岛素样生长因子-1,由 MSCs 产生可能抑制GCs中的细胞凋亡许多信号通路参与抗细胞凋亡作用,包括IRE1-α和神经生长因子/TrkA,已得到证实。
抗纤维化作用:卵巢纤维化可由机械性或低温性卵巢损伤诱发。有证据表明,多种细胞因子,如MMPs、转化生长因子(TGF)-β1、VEGF和内皮素-1,与POI相关的纤维化有关。值得注意的是,已发现POI患者的TGF-β1水平增加,这可能是由于加速卵泡闭锁导致的纤维化。抗纤维化作用与HGF、碱性成纤维细胞生长因子和肾上腺髓质素有关。MSCs可能影响上述细胞因子以抑制成纤维细胞的增殖和细胞外基质的沉积。SCs的抗纤维化作用的内在机制需要进一步澄清。
血管生成作用:重要的是,间充质干细胞会产生大量细胞因子,其中一部分可以促进各种组织的新生血管形成。SCs通过多种生物活性因子促进血管生成和卵巢恢复,包括VEGF、成纤维细胞生长因子 2、HGF、血管生成素、TGF – β1、MMP、胰岛素样生长因子和单核细胞趋化蛋白1。
免疫调节和抗炎作用:据报道,各种类型的SC可调节卵巢炎症和免疫系统。在PMSC移植的POI小鼠中,卵巢恢复后Th17/Tc17和Th17/Treg细胞比率通过PI3K/Akt信号通路降低;同样,ADSC移植促进Treg增殖,脐带间充质干细胞减少Th1/Th2细胞因子hAD-MSC移植还可以通过肿瘤坏死因子-α的活性减少卵巢中的炎症反应。
抗氧化作用:在卵巢中,活性氧的过度积累可以通过减少卵母细胞成熟和GC黄素化来诱发不育,这会降低卵母细胞质量和生殖结果。
展望
在过去的50-60年里,SC治疗的领域大大增加了。几十年前,第一代(主要的、组织来源的)SC用于实验室和诊所,而第二代细胞(人类胚胎干细胞 (hESC) 和iPSC)在过去5-10年中用于基础研究。最近,iPSCs的功能性卵母细胞衍生已经实现,这为卵巢保留不足的女性带来了新的希望。与SC工程工具包一起,工程SC可用于新的治疗应用。
干细胞治疗对卵巢早衰患者有明显的优势。
首先,与激素替代疗法和卵母细胞冷冻保存等常规方法相比,SC疗法可以更好地恢复卵巢储备,促进卵泡生成,防止GC凋亡,调节卵巢激素的分泌。其次,SC疗法可能适用于化疗引起的POI患者。
尽管可以通过使用MSCs作为替代方案来解决有关胚胎SCs移植的伦理问题,但对于治疗用途,仍有几个问题需要解决。
首先,使用SC的一个主要缺点是无法获得高质量的材料。移植方法可能是侵入性的,并可能导致术后副作用,例如免疫反应。
其次,实验模型之间存在变量使得难以标准化SC的功效。
第三,由于SC疗法是一种基于细胞的疗法,其安全性需要进一步评估,因为存在在体内形成肿瘤或异位组织的风险以及MSC在全身注射途径中的不准确迁移。值得注意的是,类器官工程领域有望通过材料、工程和临床兴趣的广泛应用来改革医学。
临床研究发现干细胞和外泌体,包括miR,对恢复卵巢功能具有积极作用,包括血管生成和遗传稳定性。人类SC治疗POI不孕症患者的应用仍处于临床前试验和临床研究的非常早期阶段。
参考文献:
Pei ZL,Wang ZY,Lu WH,Zhang FF,Li X,Tong XY,Feng Y,Xu CJ。对卵巢早衰的干细胞治疗的见解。Reprod Dev Med 2021;5:237-46。
免责说明:本文 仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。



 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号