干细胞治疗已成为神经和脊柱疾病的革命性新治疗方法。一种新兴的干细胞给药方法是鞘内应用,即将细胞直接注射到脑脊液 (CSF) 中。这项技术允许干细胞穿过脑脊液并到达大脑和脊髓,使其成为治疗中枢神经系统疾病的理想选择。
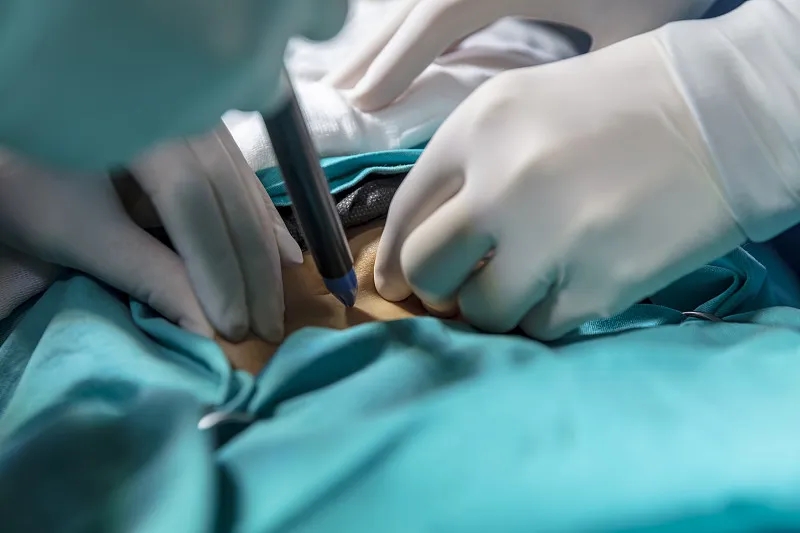
鞘内干细胞移植的工作原理
在鞘内干细胞移植过程中,从患者或捐赠者体内提取少量干细胞样本。然后将这些干细胞在实验室中培养和繁殖,然后悬浮在溶液中以准备给药。
通过腰椎穿刺将干细胞溶液直接注射到脑脊液中。这使得细胞能够随着脑脊液的自然潮起而循环,使它们与脊髓和大脑接触。
一旦通过脑脊液给药,干细胞就有潜力:
- 分化成各种神经细胞,如神经元、星形胶质细胞和少突胶质细胞
- 调节炎症并减少破坏性免疫反应
- 促进神经纤维髓鞘形成
- 通过旁分泌信号刺激常驻干细胞
- 保护现有的神经元和神经组织免于进一步退化
这种再生和保护机制的结合使得鞘内干细胞治疗神经系统疾病如此有希望。
鞘内输送干细胞能治疗哪些病症?
研究人员正在积极研究鞘内干细胞移植治疗多种中枢神经系统疾病,包括:
神经退行性疾病
- 肌萎缩侧索硬化症 (ALS):鞘内输送间充质干细胞 (MSC) 有助于减少ALS患者的炎症并减缓疾病进展。
- 多发性硬化症 (MS):已发现间充质干细胞鞘内移植可抑制多发性硬化症患者的自身免疫反应并支持髓鞘再生。
- 阿尔茨海默病和帕金森病:根据不同阶段,鞘内干细胞可以帮助患者恢复这些疾病中丢失的神经元和神经连接。
脊髓损伤
脊髓损伤后立即鞘内注射各种干细胞类型(例如神经干细胞,MSC)可以帮助改变病变环境,保护现有组织并支持再生过程。
脑瘫
早期临床研究发现鞘内脐带间充质干细胞可以改善脑瘫儿童的运动功能,且没有严重的副作用。
中风
临床研究表明,缺血性中风后鞘内引入MSC可以显着改善神经行为功能。再生中心研究了鞘内干细胞治疗中风患者的安全性和有效性。
凭借在如此广泛的条件下有希望的临床前数据,只要安全性和有效性试验继续产生积极的结果,鞘内干细胞疗法可能具有深远的治疗潜力。
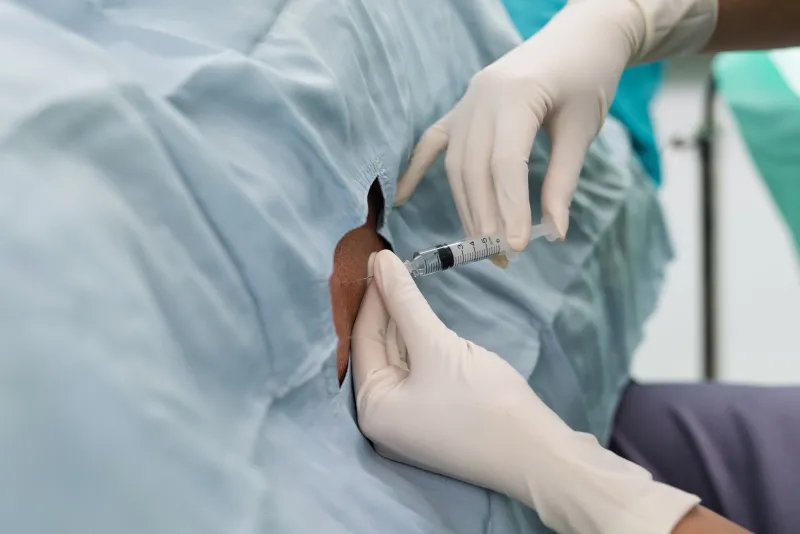
鞘内与静脉内干细胞输送
大多数针对神经系统疾病的研究性干细胞疗法都依赖于静脉输注。然而,静脉注射的细胞广泛分散在全身,由于血脑屏障,只有一小部分到达大脑或脊髓。
鞘内给药允许:
- 靶向递送:直接脑脊液注射可以使更多的干细胞到达中枢神经系统。这提高了植入的几率和功效。
- 更低的细胞剂量要求:由于循环中损失较少,因此可能需要的细胞最多减少10倍,从而降低了成本。
- 非侵入性手术:腰椎穿刺是常规的、耐受性良好的门诊手术。静脉注射可能更具侵入性。
- 重复给药选项:如果需要多次给药,腰部区域允许更直接、更安全的重复鞘内注射。
这些优点使得来自髂嵴和鞘内递送的细胞成为用于治疗神经系统疾病的干细胞疗法的极其有前途的途径。正在进行的研究旨在充分阐明静脉注射的好处并充分建立适当的细胞剂量和安全参数。
鞘内细胞输送时的关键考虑因素
虽然鞘内方法显示出巨大的潜力,但当前试验仍旨在解决以下重要因素:
- 干细胞来源:使用哪些类型的干细胞、组织来源是什么、供体注意事项(自体与同种异体)、细胞是如何培养的?
- 剂量:最佳细胞数量和给药方案因患者而异
- 安全性:再生中心在整个治疗过程中监测感染、免疫反应、毒性等不良反应。
- 跟踪和计数细胞:成像研究和流式细胞术分析帮助我们验证细胞培养物的效力,并协助注射细胞的定位和存活。
- 功能影响:对客观临床终点的严格评估可确定治疗后12个月内的真实疗效
在过去16年里,再生中心最后制定了可带来积极成果的基础方案。随着我们研究的继续,我们不断考虑成本、可扩展性和商业化障碍,将鞘内干细胞疗法转化为再生医疗保健的实际治疗应用。
鞘内干细胞移植的未来之路
未来几十年,先进的干细胞培养技术和更具选择性的间充质干细胞类型将使鞘内递送更加有针对性和有效。通过基因编辑激活干细胞也可能增强其治疗特性。
由于许多神经退行性疾病缺乏足够的治疗选择,充分发挥鞘内干细胞疗法的潜力可能会改变我们治疗肌萎缩侧索硬化症、多发性硬化症、阿尔茨海默氏症和脊髓损伤等衰弱性疾病的方式。虽然仍需要更严格的临床试验,但这种创新的递送策略显示出治愈受伤和患病中枢神经系统的巨大前景。
将干细胞鞘内注射到脑脊液中,可以广泛输送到脊髓和大脑,以治疗神经系统疾病。与静脉输注相比,直接脑脊液注射可以实现更好的干细胞植入。适当的细胞剂量、安全参数和功能影响仍在优化中。改进细胞类型和激活方法可能会进一步增强鞘内治疗的潜力。
再生中心旨在将这种创新的治疗方法转化为安全、有效的新疗法。如需了解更多信息,请联系我们。
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。



 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号