阿尔茨海默病、帕金森病和亨廷顿病等神经退行性疾病目前影响着全球数千万人。不幸的是,随着世界人口的老龄化,许多此类疾病的发病率将持续上升,预计到2050年将增加一倍以上。尽管开展了大量研究,人们对疾病发病机理的认识也在不断加深,但目前只有少数几种疗法可供选择,而且所有这些疗法都只能带来短暂的益处。因此,我们迫切需要开发新型的疾病改变疗法,以预防这些使人衰弱的疾病的发生或延缓其进展。
越来越多的临床前研究表明,移植神经干细胞(NSCs)可为神经变性提供一种前景广阔的新疗法。虽然人们最初对这一策略的兴奋点主要集中在利用神经干细胞替代退化的神经元,但最近的研究表明,神经干细胞介导的神经营养素变化是一种主要的疗效机制。
神经干细胞治疗神经退行性疾病:神经营养支持的作用
在这篇综述中,我们将讨论最近的研究成果,这些成果研究了在神经变性模型中,神经干细胞移植为受疾病影响的神经元群和突触提供营养支持的能力。然后,我们还将讨论神经干细胞移植在神经退行性疾病疗法转化为潜在临床试验之前仍然存在的一些关键挑战。
神经干细胞移植是治疗神经退行性疾病的可行方法吗?
研究人员最初假设,只有在涉及相对局灶性神经变性的疾病中,才有可能实际开发出神经干细胞治疗方法。
例如,帕金森病的主要特征是黑质底部多巴胺能神经元的丧失,它是开发神经元替代范例的绝佳候选疾病。虽然这种方法的发展仍在继续,但神经元替代的概念已被证明比最初预期的要复杂得多。例如,移植的干细胞需要在成人大脑中存活,并从最初的小注射点迁移到目标区域。然后,它们需要高保真地分化成适当的神经元亚型,如多巴胺能神经元。也许最具挑战性的是,这些移植细胞需要投射到适当的靶神经元,并形成适当的突触连接。
在帕金森病领域,这导致大多数研究将细胞移植到多巴胺能神经支配的目标纹状体,而不是受疾病影响的神经元通常所在的黑质。其他神经退行性疾病的病理变化更为广泛,多个脑区的不同神经元亚型都会缺失,如AD,因此这种神经元替代范式变得更具挑战性。那么,神经干细胞如何才能成为治疗这些更复杂的神经退行性疾病的合理疗法呢?
正如我们将讨论的,最近的研究表明,临床前模型中神经干细胞移植后一些最深刻的恢复可能是通过神经营养系统的调节来介导的。事实上,越来越多的研究发现,神经干细胞分化成支持性神经胶质亚型,例如星形胶质细胞,可以产生关键的生长因子,影响突触可塑性和神经元功能,并调节脑血管化和能量学,可能在功能恢复中发挥重要作用。图1)。
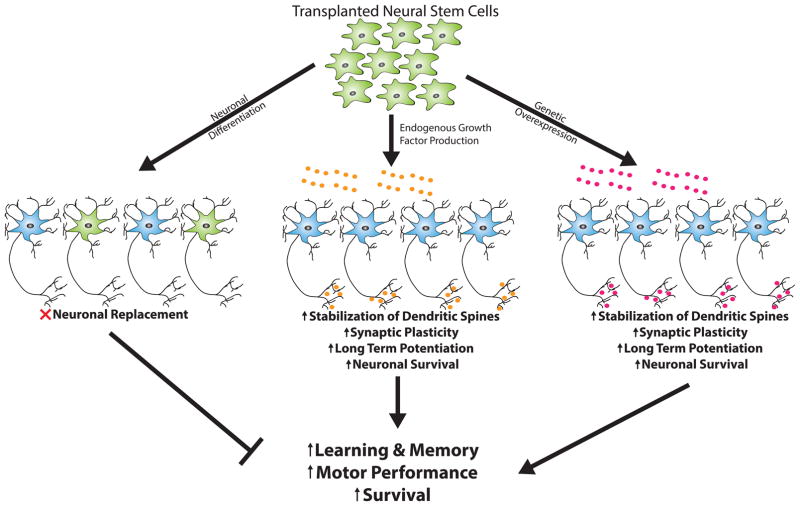
最初,许多人尝试使用神经干细胞进行神经元替代,理论上认为神经元分化(神经元;绿色)后的细胞将与宿主神经元回路(蓝色)整合,以替代在AD、PD或其他神经退行性疾病过程中死亡的神经元。然而,事实证明,实现这一目标的工作具有挑战性,而且结果好坏参半。
最近的研究表明,神经营养因子(BDNF、GDNF、IGF-1、NGF)的内源性分泌(中心,橙色)或基因过度表达(右侧,紫色)可能为基于神经干细胞的治疗提供另一种可能更有前景的方法。移植的分泌神经营养因子的神经干细胞能够增加突触可塑性,增强长期增强作用,并促进神经元存活,从而改善认知和运动表现。
中枢神经系统疾病中的神经营养因子及潜在的治疗方法
从半个多世纪前发现第一个神经营养因子–神经生长因子(NGF)开始,研究人员已经发现了大约50种能够影响中枢和周围神经系统细胞生长、存活和平衡功能的神经营养因子。在对中枢神经系统神经营养因子的研究中,最突出的是NGF、脑源性神经营养因子(BDNF)、胶质细胞系衍生神经营养因子(GDNF)和胰岛素样生长因子1(IGF-1)。这些神经营养素及其受体在人类和啮齿类动物的中枢神经系统中均高度表达,研究表明这些因子在树突棘的生长和稳定、突触可塑性、长期电位、神经元和神经胶质细胞的存活以及学习和记忆等方面起着至关重要的作用。
许多最常见的神经退行性疾病都存在神经元和突触缺失、认知障碍和炎症等共性问题,因此研究人员推测,基于神经营养的疗法可能会成功治疗这些衰弱性疾病。然而,如果从外周给药,这些神经营养因子中的许多都不能有效穿过血脑屏障,而且直接注射神经营养肽或通过基因疗法过度表达神经营养肽迄今为止都存在重大缺陷和挑战。由于间充质干细胞能产生多种神经营养因子并能广泛迁移,许多研究小组已开始研究将其用作神经营养素的潜在递送载体。
神经干细胞移植治疗阿尔茨海默病
阿尔茨海默病是与年龄相关的神经变性的最常见病因,仅在美国就有500多万人受到影响。阿兹海默症的特征是记忆和认知能力逐渐丧失,导致无法进行日常活动,最终导致死亡。尽管阿尔茨海默病普遍存在,且早在100多年前就已被发现,但目前仍没有针对阿尔茨海默病的疾病调节疗法,目前批准的药物只能缓解轻微症状,而不会显著改变疾病的进程。
从病理学角度看,注意力缺失症的特征是广泛的突触和神经元缺失、炎症和两种标志性蛋白质聚集,即由β-淀粉样蛋白(Aβ)组成的斑块和由高磷酸化tau组成的神经纤维缠结。目前流行的阿尔茨海默症认为,淀粉样蛋白的过度产生或清除障碍导致的淀粉样蛋白聚集引发了一连串的病理事件,包括tau过度磷酸化、炎症性胶质细胞病变以及突触和神经元丧失。
尽管AD病理在整个大脑中广泛存在,但某些对学习和记忆很重要的区域,如海马体、内嗅皮层和基底前脑,比其他区域受到的影响更严重。重要的是,在AD患者和动物模型中观察到神经营养蛋白表达减少和神经营养蛋白轴突运输受损,并且可能在突触和神经元损失中发挥重要作用。因此,恢复这些丢失的神经营养素是一个有吸引力的治疗目标,特别是考虑到神经营养素在突触可塑性、神经元健康以及学习和记忆中的既定作用。
我们的小组是最早证明神经干细胞移植在AD小鼠模型中提供神经营养支持方面的潜在益处的小组之一。我们发现将神经干细胞移植到老年阿尔茨海默病小鼠的海马体中可以挽救海马依赖性学习和记忆。我们进一步证明神经干细胞移植改善了海马突触密度,为改善认知提供了潜在的结构基础。有趣的是,神经干细胞移植后淀粉样蛋白和tau蛋白的水平没有变化,这表明神经干细胞移植可能针对AD神经元功能障碍的下游方面,但也意味着这种方法可能为患有严重现有病理的患者带来益处。
神经营养素与帕金森病
帕金森病是一种使人衰弱的神经退行性疾病,其特征是运动功能受损。患者经常表现出标志性运动表型,包括震颤、运动缓慢或过度僵硬以及启动运动困难。不幸的是,高达70%的PD患者在病程中还会发展为帕金森病痴呆 (PDD)。虽然LevaDOPA等PD疗法比目前可用于AD的疗法要有效得多,但仍然没有针对PD的疾病缓解疗法,并且L-DOPA疗法的有效性通常会随着时间的推移而减弱,并导致越来越严重的副作用。
从病理学角度来说,PD的特点是黑质内多巴胺 (DA) 神经元的缺失,黑质是投射到纹状体的中脑核,在运动的启动和控制中发挥着不可或缺的作用。
由于帕金森病神经元缺失的相对局灶性,这种疾病被认为是干细胞疗法的理想候选者,其目标是使用神经干细胞替代死亡和垂死的多巴胺神经元。
与AD类似,帕金森病的特征还在于关键大脑区域内神经营养因子支持的丧失。据报道,PD患者黑质内BDNF和GDNF均缺失,并且重要的是,BDNF和GDNF都与发育、生存和功能有关。中脑多巴胺神经元在 PD中退化。
其他一些研究也探讨了将过表达GDNF或其他神经营养素的神经干细胞单独移植到帕金森病动物模型中可能产生的有效疗法。其中一项研究使用了类似的帕金森病病变模型,发现过表达GDNF的小鼠神经干细胞移植可防止黑质中DA神经元的退化,并减少行为障碍。为了将这些早期努力转化为临床试验,Clive Svendsen及其同事领导的一系列研究还考察了经修饰以过度表达各种神经营养素的胎源性人类神经干细胞是否能够保护DA神经元并挽救运动障碍。
总而言之,来自多巴胺细胞死亡动物模型的证据无疑支持产生神经营养素的神经干细胞治疗帕金森病的潜在用途。然而,这些模型都没有概括大多数人类患者中发现的α-突触核蛋白病理学,而这些病理学可能在PD的发展中发挥重要作用。令人鼓舞的是,我们实验室最近在突触核蛋白病动物模型中发表的一份报告进一步支持了神经干细胞移植为帕金森病和其他突触核蛋白病输送神经营养素的潜在用途。
在这项研究中,我们发现移植产生BDNF的小鼠神经干细胞可以改善突触核蛋白病转基因模型中的运动和认知缺陷,并且BDNF的产生对于这些改善是必要的。
神经营养与亨廷顿氏病(HD)
亨廷顿舞蹈症是一种显性遗传的进行性神经退行性疾病,会导致认知和运动功能受损,最终导致死亡。HD是由亨廷顿基因内三联体重复 DNA序列的扩展引起的,导致产生含有扩大的致病性多聚谷氨酰胺束的突变蛋白 。HD症状通常在35-40岁左右开始,并不断进展,最终导致症状出现后15-20年死亡。从病理学上讲,HD患者表现出神经元和突触损失,影响纹状体的中型多刺GABA能中间神经元,但随着疾病的进展,也会导致皮质和其他大脑区域的退化。
鉴于HD中发生的最初区域特异性变性,研究人员推测神经干细胞移植可能提供一种可行的治疗方法。甚至在人类HD患者中进行了与PD类似的胎儿组织移植。然而,这些临床研究的结果再次好坏参半,再次表明神经元替代范例仍然极具挑战性。与PD和AD一样,HD患者大脑中神经营养因子的表达显着降低。此外,在HD神经毒素模型中,神经营养因子被发现对于纹状体神经元的存活至关重要。
与在PD模型中测试的策略类似,在移植到HD动物模型之前,有几个组在NSC系中过度表达了神经营养因子。
一项此类研究比较了过度表达NGF或BDNF的神经干细胞在亨廷顿舞蹈症模型中挽救纹状体神经元变性的能力。这项研究发现,表达NGF的神经干细胞可以挽救中型棘状中间神经元和胆碱能纹状体中间神经元,并减少炎症迹象。
在本研究中,BDNF过度表达的神经干细胞对这些终点几乎没有影响。另一组使用亨廷顿舞蹈症转基因模型的报告发现,利用过表达GDNF的NSC得到了类似的结果。这项研究的作者发现,与未修饰的神经干细胞相比,过表达GDNF的神经干细胞不仅可以挽救纹状体神经元的损失,而且还可以防止运动功能的下降。表明神经干细胞介导的神经营养因子的传递可以为HD提供有希望的潜在治疗方法。
主要挑战
最大的挑战之一是所使用的方法和细胞的巨大差异。这一挑战绝不是干细胞领域所独有的,而是由于干细胞疗法的复杂性以及不同干细胞系之间的许多固有差异而加剧。
结论
总而言之,本综述中讨论的研究已经开始深入了解神经干细胞移植作为多种神经退行性疾病的潜在疗法的功效。许多神经干细胞移植研究最初集中于替代死亡或垂死的细胞,然而,越来越多的工作现在表明,神经干细胞介导的神经营养支持调节可能提供许多额外的重要益处。
尽管仍然存在许多挑战和问题,但这篇综述中详细介绍的工作为 神经干细胞移植有一天可能为这一毁灭性的神经退行性疾病提供一种真正的疾病修饰疗法带来了希望。
参考资料:Marsh SE, Blurton-Jones M. Neural stem cell therapy for neurodegenerative disorders: The role of neurotrophic support. Neurochem Int. 2017 Jun;106:94-100. doi: 10.1016/j.neuint.2017.02.006. Epub 2017 Feb 20. PMID: 28219641; PMCID: PMC5446923.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信