概述:自身免疫性风湿病(AIRDs)的治疗正经历从“长期免疫抑制”向“持续缓解乃至治愈”的范式转移。2026年4月,发表于《临床风湿病学》(Clinical Rheumatology)的最新综述指出[1]:MSC、Treg、CAR-T 及外泌体疗法正成为精准管理炎症性疾病的新前沿。本文将结合2026年初发布的CASTLE等核心临床试验,深度解析这一领域的革命性进展。
重塑免疫平衡:MSC、Treg、CAR-T及外泌体在治疗自身免疫性风湿病中的最新临床突破

核心速览
| 疗法类型 | 核心机制 | 关键临床数据 | 主要挑战 |
|---|---|---|---|
| 间充质干细胞(MSC) | 旁分泌+细胞接触,免疫调节、组织修复 | 42项RCT荟萃分析:SLE患者SLEDAI显著改善;RA总有效率54%;联合IFN-γ使ACR20达93.3% | 来源、剂量、方案标准化 |
| 调节性T细胞(Treg) | 恢复免疫耐受,抑制自身反应T细胞 | CHILL I/II期试验(QEL-005 CAR-Treg)启动;IL-2mutein IIa期进行中 | 成本高、体外扩增难、致癌风险 |
| CAR-T细胞 | 基因改造T细胞清除致病B细胞 | CASTLE试验(Nature Med,2026):24例难治性SLE/SSc/IIM,91.7%达疗效终点,无药缓解;relma-cel I期:8例SLE均达SRI-4 | CRS、神经毒性、B细胞长期耗竭、成本 |
| 外泌体(无细胞) | 携带miRNA/蛋白,免疫调节、组织修复 | 临床前RA/SLE模型有效;MESAE试验(NCT07131683)探索鼻内给药 | 标准化分离、规模化生产、长期安全性 |
一、为什么自身免疫性风湿病需要细胞免疫疗法?
类风湿关节炎(RA)、系统性红斑狼疮(SLE)、幼年特发性关节炎(JIA)、银屑病关节炎(PsA)、强直性脊柱炎(AS)等自身免疫性风湿病(AIRDs),其核心病理是免疫系统攻击自身组织,导致慢性炎症和组织损伤。

传统治疗从非甾体抗炎药到改善病情抗风湿药(DMARDs),再到生物制剂和靶向合成DMARDs,虽然取得了长足进步,但仍有相当比例的患者面临三大困境:
- 疾病控制不佳(部分患者原发无效)
- 无法耐受不良反应
- 无法实现停药缓解
细胞免疫疗法的目标不再是“压制”免疫系统,而是重建免疫平衡——恢复疾病发生前的生理状态,甚至实现治愈。间充质干细胞(MSC)、调节性T细胞(Treg)、嵌合抗原受体T细胞(CAR-T)以及外泌体,正成为这场范式转变的核心力量。
核心特性与总体免疫调节框架
间充质干细胞(MSC)治疗自身免疫性疾病的核心在于其强大的免疫调节、组织修复与再生能力。MSC通过旁分泌信号和直接的细胞间相互作用,能够系统性地减轻炎症,而非单纯抑制免疫。其作用覆盖固有免疫与适应性免疫,并通过复杂的分泌组、细胞外囊泡以及代谢-表观遗传重编程,从多个维度重建免疫耐受,为治疗难治性自身免疫病提供了创新策略。
对固有免疫细胞的调控
MSC可显著影响树突状细胞(DC)、巨噬细胞和自然杀伤(NK)细胞。它们通过下调MHC II、CD80/CD86和IL-12抑制DC的分化与成熟,并诱导耐受性DC表型,从而促进调节性T细胞(Treg)扩增。MSC还能增加IL-10、TGF-β、PGE2和IDO活性,将巨噬细胞从促炎的M1型转变为抗炎修复的M2型,同时下调TNFα、IL-1β和IL-6。此外,通过PGE2、TGF-β、HLA-G及细胞接触,MSC抑制NK细胞的增殖、细胞毒性和IFN-γ产生,从而减弱驱动自身免疫的早期先天反应。
对适应性免疫(T细胞与B细胞)的调节
在适应性免疫方面,MSC通过IDO、一氧化氮、PGE2、TGF-β及PD-L1/PD-1通路,抑制CD4⁺和CD8⁺T细胞增殖,降低Th1/Th17反应;同时促进FoxP3⁺Treg和Tr1细胞的扩增与功能稳定,恢复外周耐受,减少自身反应性T细胞活性。对于B细胞,MSC通过可溶性因子(如调节IL-6、BAFF,增强IDO)和接触依赖机制,抑制B细胞增殖、分化为浆细胞及免疫球蛋白产生,从而降低致病性自身抗体滴度。
旁分泌、细胞外囊泡及代谢-表观遗传机制
MSC分泌复杂的旁分泌组(含TGF-β、IL-10、HGF、VEGF、PGE2及IDO代谢物),可下调NF-κB信号和促炎因子,促进血管生成与组织修复,并诱导免疫细胞向耐受表型转变。
此外,MSC释放的细胞外囊泡(含miR-21、miR-146a、miR-155等)能重现其免疫调节作用,抑制TLR/NF-κB通路和Th17分化,支持Treg稳定性;相比全细胞疗法,囊泡免疫原性更低、更易标准化。
最后,MSC还通过IDO-犬尿氨酸通路、腺苷信号(CD39/CD73)和活性氧调节,将T细胞和巨噬细胞从糖酵解促炎状态转变为氧化磷酸化调节表型,并通过组蛋白修饰、DNA甲基化稳定耐受相关的转录程序。
临床试验证据
在机制研究不断深化的同时,MSC疗法的临床验证也在持续推进。
一项截至2025年2月的系统性综述与荟萃分析(纳入42项随机对照试验、涉及2,183名参与者)评估了MSC移植在RA、SLE、脊柱关节炎、原发性干燥综合征等多种风湿免疫病中的疗效与安全性[2]。

结果显示,MSC移植可显著改善SLE患者的系统性红斑狼疮疾病活动指数(SLEDAI);在RA中,总临床有效率达到54%,且应答组CD4⁺CD25⁺FoxP3⁺Treg百分比升高,而CD4⁺IL-17A⁺Th17细胞百分比下降。更为重要的是,MSC移植并未增加不良事件的发生率,支持了其在多种风湿免疫病中的安全性。
在临床研究的最新进展方面,多项I/II期试验正在积极招募或已完成初步分析。一项人脐带间充质干细胞(hUC-MSC)治疗中重度SLE的I/II期临床研究(NCT07041801)计划纳入58名受试者,通过低、中、高三个剂量组及安慰剂对照设计,系统评估hUC-MSC注射剂的安全性、药效动力学和免疫原性。
另一项针对活动性增殖性狼疮肾炎的IIb期、双盲、安慰剂对照随机试验(NCT03673748)正在评估单次静脉输注骨髓来源MSC(2百万细胞/kg)对难治性LN患者的疗效,预计2027年完成主要终点分析。
此外,一项脐带来源MSC治疗RA的I期试验(NCT05003934)采用单次静脉输注1亿个细胞,计划进行长达48个月的随访评估。特别值得一提的是,MSC联合IFN-γ的方案在RA治疗中展现出令人瞩目的前景:一项临床试验(ChiCTR-INR-17012462)报告,联合治疗组在3个月时的ACR20应答率达到93.3%,而MSC单药组仅为53.3%,且1年随访期内未发现重大安全性问题。
挑战与窗口期
MSC来源(骨髓、脂肪、脐带)、培养条件、给药方案差异大,限制疗效可比性。最佳治疗窗口可能是疾病早期,此时有机会纠正免疫失衡至接近生理状态。
二、调节性T细胞免疫疗法
概念与基本原理
调节性T细胞(Treg)疗法的目标是通过在慢性自身免疫性炎症疾病患者体内扩增或输注自体、基因工程改造或异体Treg细胞来恢复免疫耐受。在炎症性风湿病中,调节性T细胞的数量和功能均存在不同程度受损。Treg功能失调被认为是自身免疫性疾病的标志性特征,恢复这种功能障碍可能调节疾病进程并诱导疾病缓解。
近年来,Treg疗法已从概念验证阶段进入临床试验的实质性探索阶段。2026年3月,Quell Therapeutics公司已获得英国MHRA批准,启动了名为CHILL的I/II期临床研究,评估其基于CD19靶向的CAR-Treg产品QEL-005在难治性RA和系统性硬化症中的安全性与初步疗效。该研究计划在英国、德国和西班牙纳入最多16名成年参与者,预计2027年第一季度发布早期临床数据[3]。

同时,一项评估新型IL-2mutein(MK-6194)选择性扩增Treg的IIa期试验也在SLE患者中进行中,旨在解决Treg扩增疗法开发中的技术挑战,预计2027年4月完成主要终点分析。
现有挑战与未来方向
初步研究表明,Treg免疫疗法可以抑制自身反应性免疫应答,并可能提供持久的治疗效果。然而,Treg疗法的高昂成本和技术挑战,以及对病原体反应减弱和潜在致癌风险的安全性担忧,仍在很大程度上限制了其广泛的临床应用。未来研究需要进一步优化Treg细胞在体外输注前的稳定性与扩增效率,以提升治疗效果并降低成本。
三、嵌合抗原受体(CAR)-T细胞疗法
疗法原理与基本流程
CAR-T细胞疗法是免疫疗法的前沿技术,最初用于血液肿瘤,现正被探索作为自身免疫性疾病的一种变革性手段。其核心是对患者自身的T细胞进行基因工程改造,使其表达嵌合抗原受体(CAR),从而识别并清除驱动疾病病理的自身反应性B细胞或T细胞(图1)。
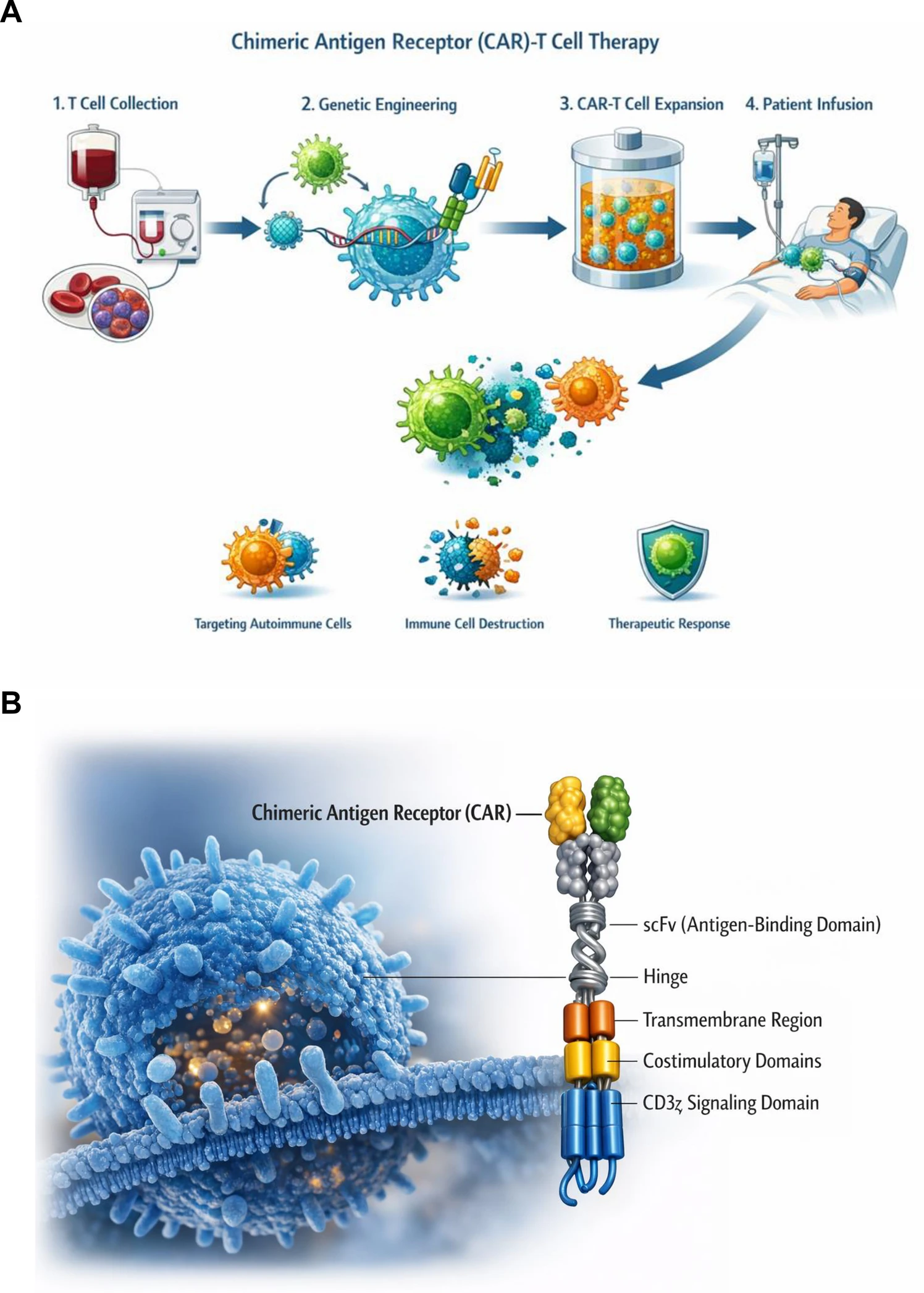
标准流程包括:从患者血液采集T细胞(白细胞分离术);利用病毒或非病毒载体导入CAR构建体;体外扩增修饰后的T细胞至治疗剂量;最后将CAR-T细胞回输患者体内,使其精准寻找并摧毁致病免疫细胞。
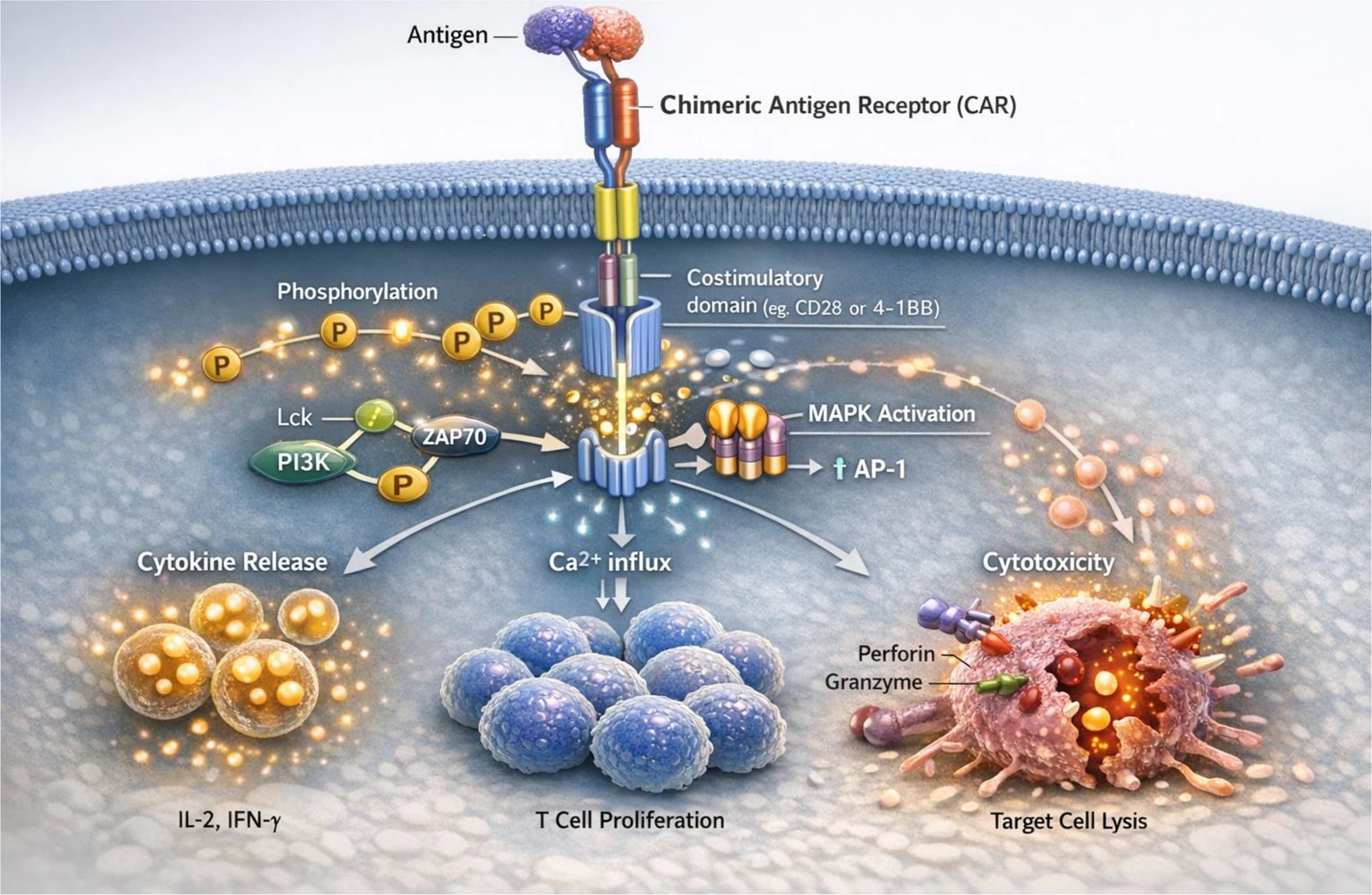
CAR结构与信号激活机制
CAR结构包含细胞外抗原识别域(通常源自单克隆抗体的单链可变区scFv)、跨膜域和多个细胞内信号域(含共刺激域和CD3ζ信号域)。当CAR与靶抗原结合后,细胞内CD3ζ和共刺激域(如CD28或4-1BB)会诱导早期信号事件(如Lck、ZAP70、PI3K及磷酸化级联),进而激活下游通路(Ca²⁺内流、MAPK/AP-1通路),最终产生细胞因子释放(IL-2、IFN-γ)、T细胞增殖以及对靶细胞的细胞毒性作用(穿孔素/颗粒酶途径)。这些效应构成了CAR-T治疗自身免疫病的功能基础。
自身免疫病中的应用靶点与临床前证据
在自身免疫性疾病中,CAR-T细胞疗法正被研究用于选择性清除致病性免疫细胞。靶向CD19的CAR-T细胞可清除自身反应性B细胞,也有研究探索靶向自身反应性T细胞的策略,从而阻断自身免疫级联反应。临床前研究已证实该概念的有效性,尤其在以致病性B细胞为核心驱动因素的RA和SLE等疾病中展示了明确的治疗潜力。
临床试验证据
CAR-T疗法在自身免疫病中的临床研究进展尤为迅猛。最为瞩目的是CASTLE(CAR-T cells in systemic B cell mediated autoimmune disease)I/IIa期临床研究,其完整结果已于2026年1月发表于Nature Medicine[4]。

该研究纳入了24名治疗抵抗的SLE(10例)、系统性硬化症(9例)和特发性炎性肌病(5例)患者,所有患者均接受单次输注自体CD19 CAR-T细胞(Zorpo-cel)。
主要安全性终点方面,未发生2级以上CRS,也未出现ICANS。主要疗效终点方面,22/24(91.7%)的患者在24周时达到了预定义的疗效终点:9/10的SLE患者达到DORIS缓解,9/9的SSc患者疾病未出现进展,4/5的IIM患者达到ACR主要/中度应答。更重要的是,所有患者在24周的整个观察期内均未使用糖皮质激素或其他免疫抑制剂。
在SLE领域,2025年12月,另一项I期剂量递增研究(NCT06551142)评估了relmacabtagene autoleucel(relma-cel)——一种CD19 CAR-T细胞产品——在中重度活动性SLE中的安全性和有效性。8例女性患者在接受氟达拉滨和环磷酰胺预处理后接受了单次CAR-T细胞输注(剂量范围为50×10⁶至100×10⁶)[5]。

结果显示,未发生剂量限制性毒性,不良事件可控(7例出现CRS,1例出现ICANS)。所有患者在6个月时均达到SRI-4应答,6例达到LLDAS,5例达到DORIS缓解。平均SLEDAI-2K评分从基线时的12.625降至随访时的3.25,肾脏功能和补体水平也获得显著改善。
在通用型CAR-T方面,Fate Therapeutics公司的FT819——一种源于诱导多能干细胞系的现货型CD19 CAR-T细胞产品——在I期临床试验中已治疗了12例SLE患者和1例SSc患者。数据显示,FT819在不需强化预处理化疗的条件下即实现了持续的B细胞耗竭和临床应答,SLEDAI-2K评分在剂量2组中从基线的平均14.3降至6个月的4,降幅达78%。
主要安全风险与不良反应
尽管前景广阔,CAR-T疗法伴随显著的安全隐患。主要包括:
①靶向肿瘤外效应——CAR-T可能误伤表达相同抗原的健康细胞,导致非预期组织损伤;
②细胞因子释放综合征(CRS)——由大量活化的CAR-T细胞释放细胞因子引发的全身性炎症反应,可能危及生命;
③神经毒性——部分患者出现机制尚在研究中的神经系统副作用;
④长期免疫抑制——B细胞耗竭增加感染风险,并可能损害疫苗反应能力。这些风险限制了其广泛应用。
当前挑战与未来改进方向
目前CAR-T疗法成本高昂且资源密集,需要专门设施进行个体化细胞处理和患者监测,规模化推广困难。
未来研究方向包括:开发更高特异性的CAR以减少脱靶效应;设计“自杀开关”以便在严重不良事件时可控清除CAR-T细胞;探索同种异体(“现成”)CAR-T产品以降低成本和提高可及性;以及研究与其他免疫调节剂的联合疗法来增强疗效。随着技术改进,治疗成本有望降低,安全性和有效性将逐步提升。
四、外泌体的基本特征与治疗相关功能
外泌体特征与功能
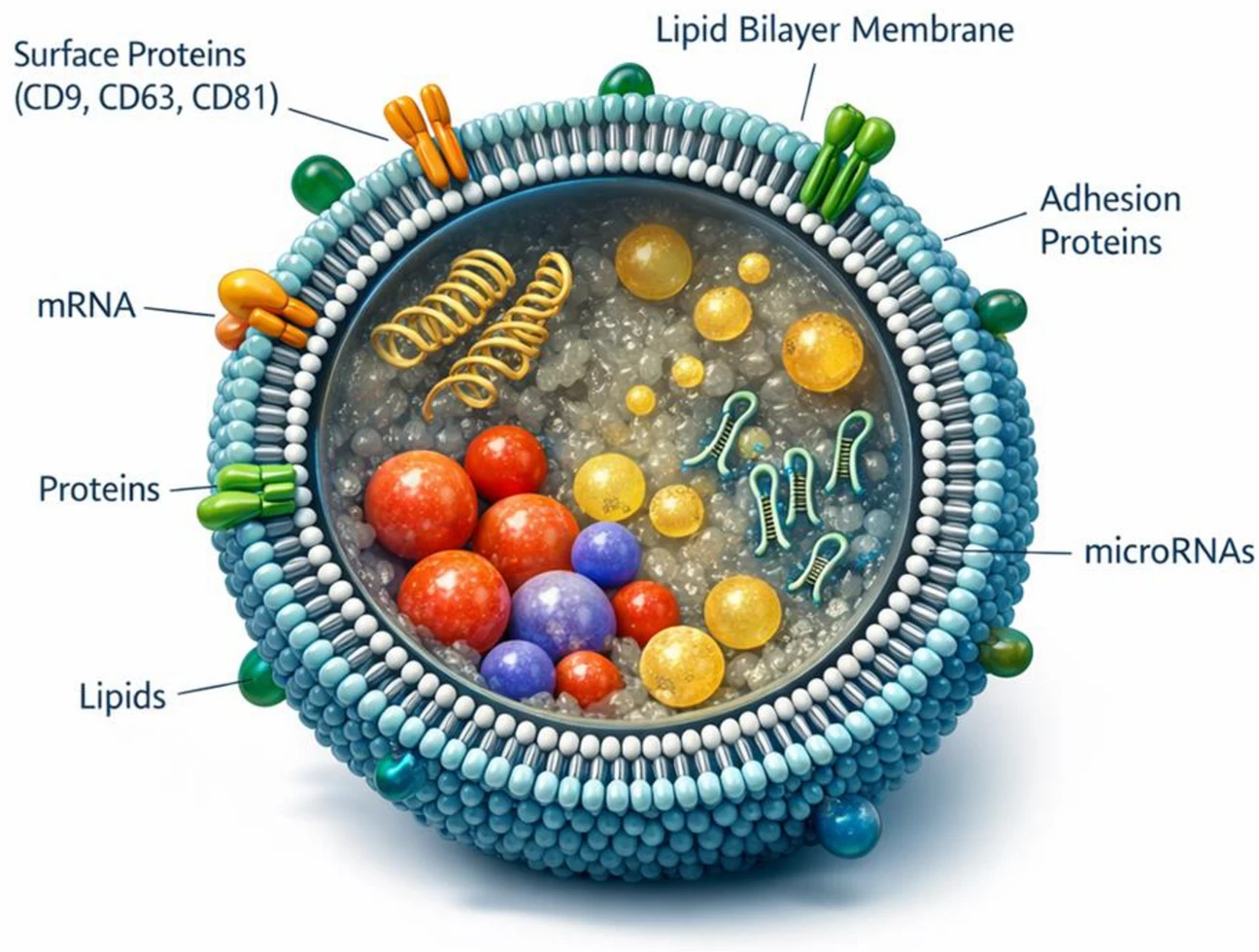
外泌体是直径30—150纳米的纳米级细胞外囊泡,几乎所有细胞类型(包括免疫细胞、间充质干细胞和滑膜成纤维细胞)均可分泌。它们在多囊泡体中形成并释放至细胞外空间,作为细胞间通讯的重要介质。
外泌体富含多种生物活性分子,例如蛋白质、脂质、mRNA和microRNA(miRNA),这些分子可以调节受体细胞的功能和表型表达。外泌体的双层脂质结构如图2所示。外泌体的生物发生途径包括早期内体、多囊泡体(MVBs)以及腔内囊泡释放到细胞外空间(图3A)。
外泌体一旦产生,便会附着在靶细胞上,并通过主要的摄取途径进入细胞,包括胞吞作用、膜融合以及靶细胞受体介导的内化(图3B)。
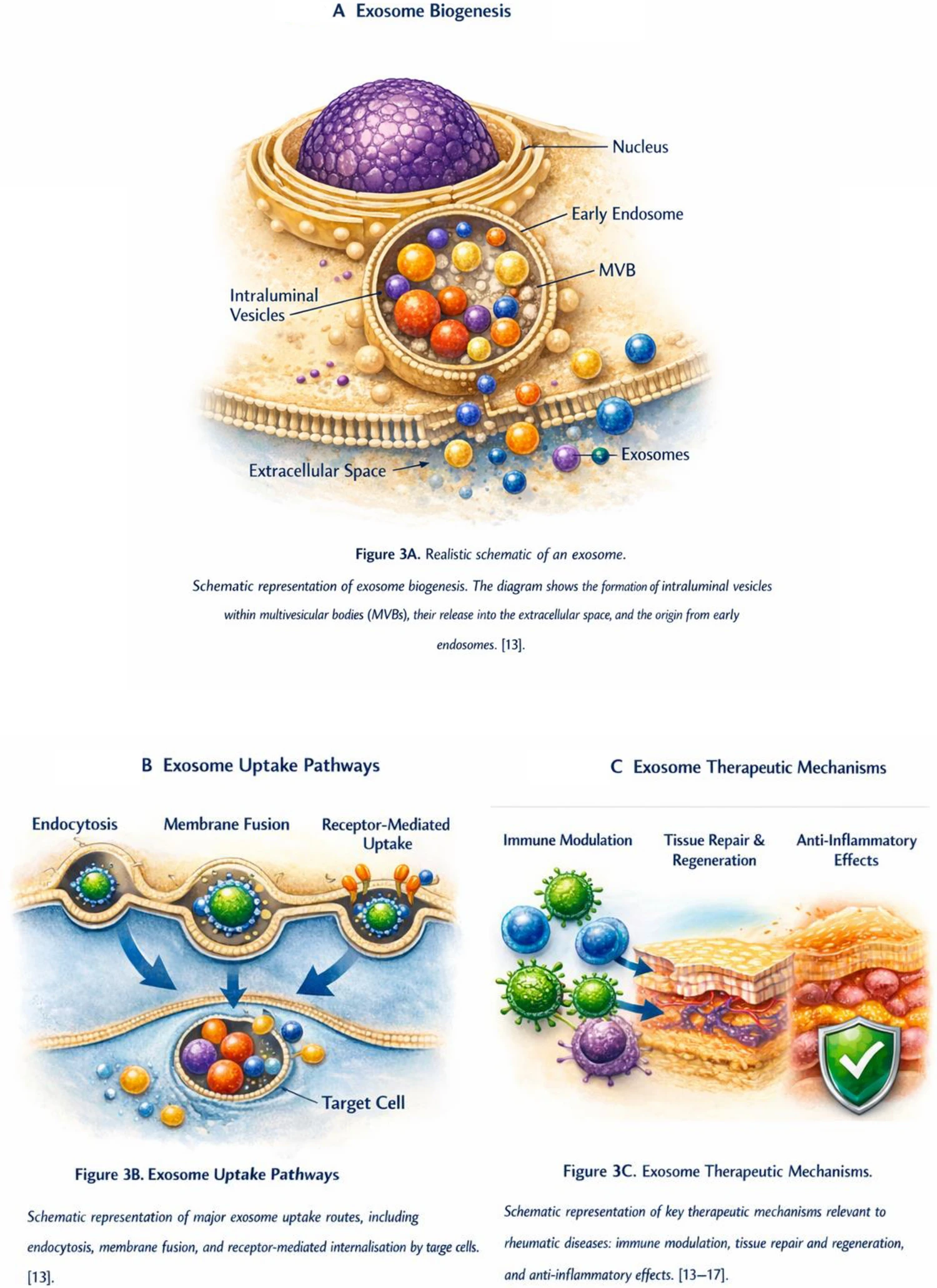
外泌体随后可以发挥多种关键的生物学效应,例如:免疫调节、组织修复和再生以及抗炎作用,所有这些都是与风湿性疾病治疗相关的关键治疗机制(图3C)。
在风湿病中的具体免疫调节机制
MSC来源的外泌体在自身免疫性风湿病中展现出强大的免疫调节能力。它们携带抗炎细胞因子(TGF-β、IL-10)、免疫调节性miRNA及表面分子,能够抑制自身反应性T细胞和B细胞的活化与增殖,抑制树突状细胞成熟并促进耐受性表型,同时诱导巨噬细胞向抗炎性M2表型极化。此外,外泌体还能减少促炎细胞因子(如TNF-α、IL-6)的产生并增强免疫抑制通路,从而系统性地重建免疫平衡(图4)。
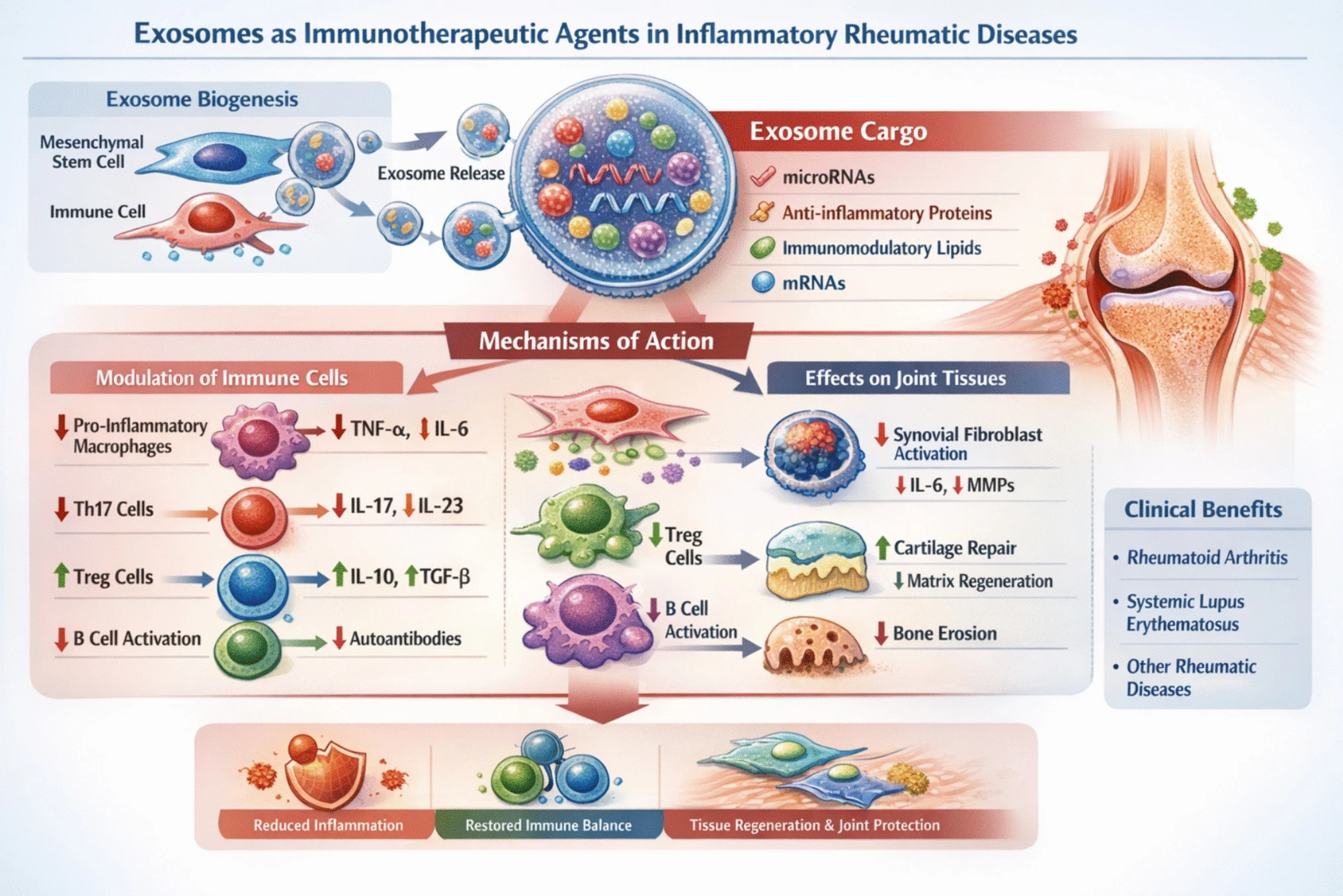
临床前证据与“无细胞纳米免疫疗法”概念
在类风湿性关节炎 (RA) 和系统性红斑狼疮 (SLE) 的临床前模型中,间充质干细胞 (MSC) 来源的外泌体已被证明可以抑制滑膜炎症、减少软骨退化并促进组织修复,凸显了其治疗潜力。因此,外泌体可以提供一种无细胞的纳米细胞免疫疗法(图4)。
临床试验进展与前景
尽管临床前数据令人鼓舞,外泌体疗法在风湿病领域的临床试验尚处于早期探索阶段。目前,一项I/IIA期研究(MESAE,NCT07131683)正在评估人脐带MSC来源外泌体(HUC-MSC-EXO)在自身免疫性脑炎患者中的安全性和初步疗效,采用鼻内给药方案,包含三个剂量队列的剂量爬坡阶段和一个随机双盲安慰剂对照的扩展阶段[6]。

该研究为MSC来源外泌体在自身免疫病中的临床应用提供了重要的可行性参考,但在风湿病领域仍需开展专门的临床试验加以验证。
优势、挑战与未来方向
与全细胞疗法(如CAR-T、MSC)及单克隆抗体相比,外泌体具有多项优势:免疫原性降低(缺乏主要组织相容性复合体分子,最大程度减少了免疫排斥风险)、致瘤性较低、易于储存和标准化(促进“现成”治疗产品的开发)、以及具有靶向递送潜力。
然而,在广泛临床应用前仍需解决若干挑战:包括建立标准化的分离与表征方法以确保纯度和效力,确定最佳剂量、给药频率与途径,评估长期安全性和脱靶效应,以及克服规模化生产和质量控制方面的监管与生产障碍。
未来发展方向包括外泌体工程改造(如负载特定miRNA或药物、表面修饰以实现靶向递送),以及基于外泌体的液体活检用于疾病监测和个体化医疗。最终,外泌体疗法有望为炎症性风湿病带来创新性的无细胞精准治疗策略。
六、四大疗法对比与未来展望
| 维度 | MSC | Treg | CAR-T | 外泌体 |
|---|---|---|---|---|
| 作用方式 | 旁分泌+接触 | 免疫抑制 | 清除致病细胞 | 递送生物活性分子 |
| 细胞来源 | 异体/自体 | 自体(扩增) | 自体(基因改造) | 细胞培养上清 |
| 制备周期 | 数周 | 数周 | 数周 | 可批量生产 |
| 免疫原性 | 低 | 无 | 无(自体) | 极低 |
| 主要风险 | 标准化不足 | 致癌、感染 | CRS、神经毒性、B细胞耗竭 | 长期安全性未知 |
| 成本 | 中等 | 高 | 极高 | 低-中等 |
| 临床阶段 | II/III期 | I/II期 | I/II/III期 | 临床前/I期 |
共同趋势:从“免疫抑制”转向“免疫重建”;从“症状控制”转向“治愈可能”;从“一刀切”转向“精准靶向”。
七、常见问题解答(FAQ)
参考资料:
[1]:Chikanza, I.C., Sakkas, L.I. Cell immunotherapy in autoimmune rheumatic diseases: a paradigm shift in the therapy of autoimmune inflammatory rheumatic diseases. Clin Rheumatol (2026). https://doi.org/10.1007/s10067-026-08103-0
[2]:Zeng, L., Liu, C., Wu, Y. et al. Efficacy and safety of mesenchymal stromal cell transplantation in the treatment of autoimmune and rheumatic immune diseases: a systematic review and meta-analysis of randomized controlled trials. Stem Cell Res Ther 16, 65 (2025). https://doi.org/10.1186/s13287-025-04184-x
[3]:https://reachmd.com/news/chill-trial-launch-quells-qel005-cartreg-enters-phase-12/2485897/
[4]:Müller, F., Hagen, M., Wirsching, A. et al. CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial. Nat Med 32, 1142–1151 (2026). https://doi.org/10.1038/s41591-025-04185-6
[5]:https://www.sciencedirect.com/science/article/pii/S0896841125001349?via%3Dihub
[6]:https://ichgcp.net/zh/clinical-trials-registry/NCT07131683?hl=it
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信