描述:《Experimental Neurology》2026年综述:间充质干细胞(MSC)治疗缺血性卒中,涵盖归巢、免疫调节、促血管神经发生机制,总结2005-2025年关键临床试验(静脉/动脉/鼻内/鞘内给药),分析安全性及疗效瓶颈,附常见问题解答。
引言:缺血性卒中——从血管再通到神经修复的范式跨越
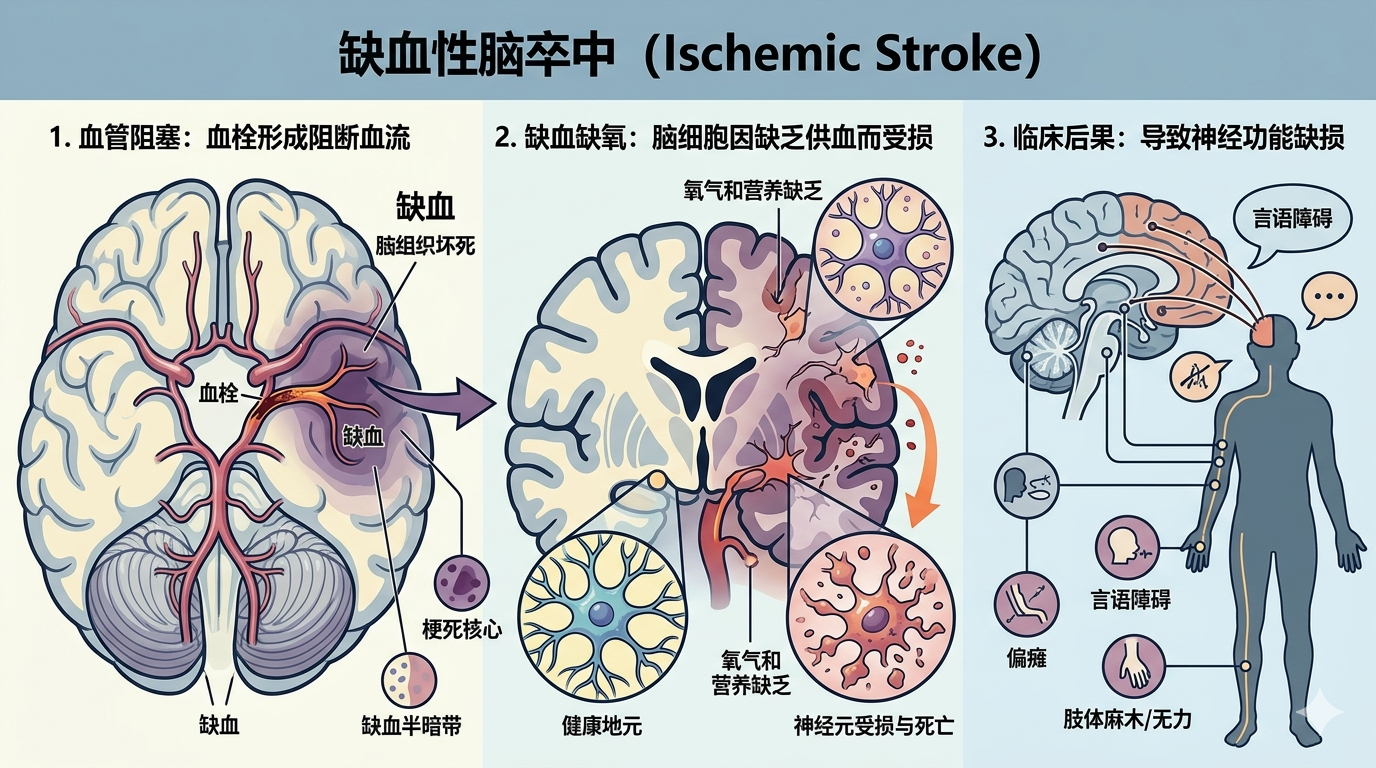
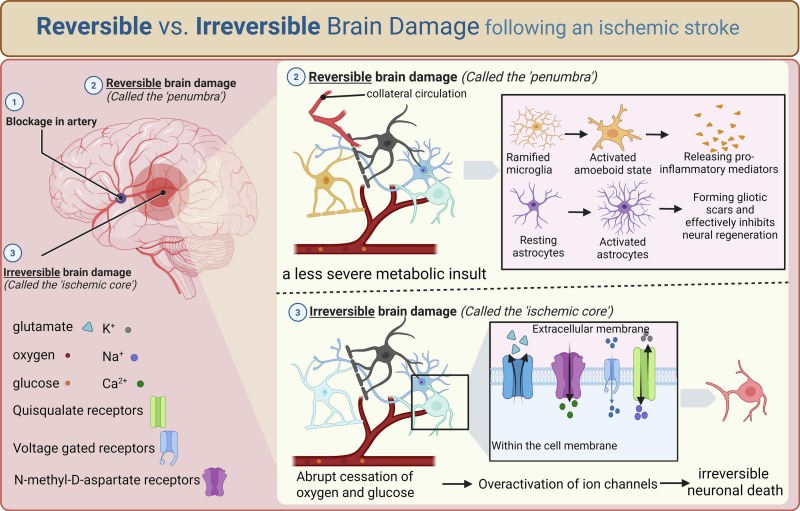
缺血性卒中位居全球致死及致残原因前列,占所有卒中病例的80-85%。其核心病因为脑动脉栓塞、血栓形成或全身性低灌注,导致供血区域血流锐减,继而引发一系列病理生理级联反应。根据灌注不足的严重程度,受累区域被划分为不可逆的梗死核心与可挽救的缺血半暗带(图1)。
现行急性干预措施,如溶栓与机械取栓,均受制于狭窄的治疗时间窗,且策略重心主要在于血管再通。然而,这些方法难以解决卒中后持续存在的神经血管损伤、顽固性炎症反应以及内源性修复能力耗竭等根本问题——后者恰是导致长期功能障碍的症结所在。
深度综述 | 间充质干细胞治疗缺血性卒中:我们离临床普及还有多远?
在此背景下,间充质干细胞(MSCs) 作为一种前景广阔的再生治疗策略崭露头角。其作用靶点已超越急性期血管再通,直指卒中后复杂病理生理机制的核心环节。2026年4月28日,发表于《Experimental Neurology》的一篇题为“间充质干细胞治疗缺血性卒中:机制与进展”的综述,系统梳理了该领域的关键证据[1]。
本文基于该综述,全面分析MSCs的多元来源、多模式作用机制、临床试验进展、现存挑战及未来方向。
间充质干细胞治疗缺血性脑卒中的作用机制:MSCs如何发挥作用?
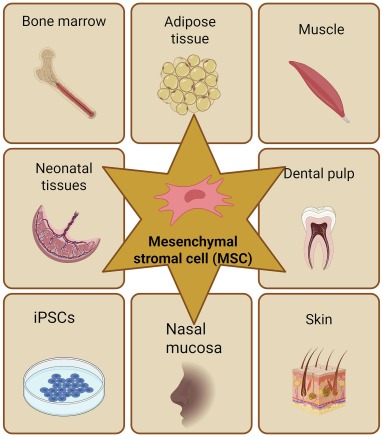
Friedenstein及其同事的奠基性研究,首次分离出具有成骨、成软骨及成脂分化能力的贴壁高增殖细胞,从而确立了MSCs的身份。当前,MSCs已可从脂肪组织、骨髓、牙髓及脐带等多种成人与围产期组织中获取,并因其多方面的药理作用而备受关注(图2)。其易于分离、长期稳定性及良好的伦理记录等实用优势,进一步巩固了骨髓来源(BM-MSCs)、人脐带来源(HUC-MSCs)及脂肪来源(AD-MSCs)MSCs的临床转化基础。
归巢机制:精准奔赴损伤的第一站
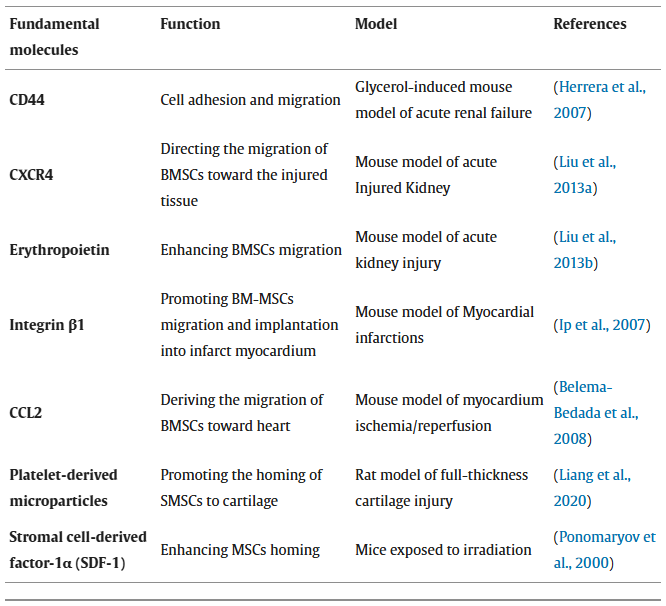
MSCs归巢至损伤部位的能力,是其发挥治疗效应的基本前提。其治疗效果与归巢能力受多重因素调控,既包括细胞自身特性(如组织来源、供体年龄、培养条件及传代次数),也涉及宿主相关因素(如给药途径、细胞剂量及受体的整体生理状态与易感性)。
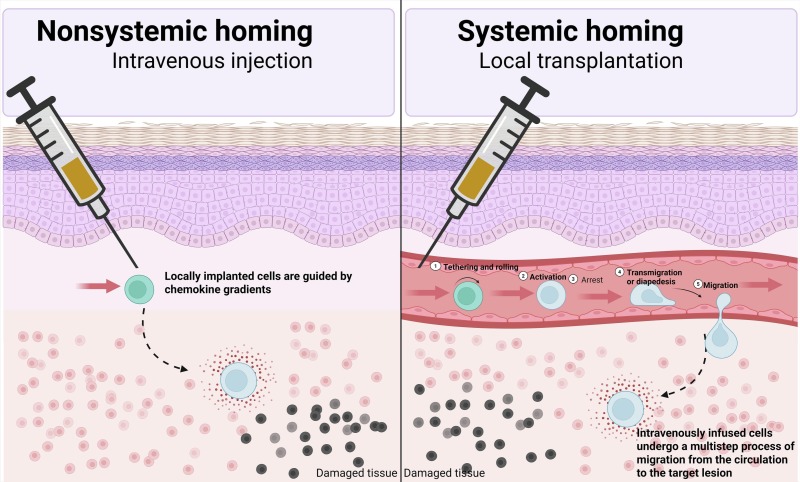
归巢过程可大致分为非系统性与系统性两种模式。前者指局部植入的细胞在趋化因子梯度引导下的定向迁移;后者则指静脉输注的细胞历经循环系统,完成多步骤迁移到达靶病灶的过程(图3)。现有研究已证实,多种分子与细胞机制参与调控MSCs的归巢过程(表1)。
细胞替代:非主导的间接证据
细胞替代并非MSCs治疗缺血性卒中的主要作用机制,具体表现为:
转分化能力有限:在缺血条件下,MSCs向功能性神经元或胶质细胞直接转分化的能力很弱。尽管移植后的MSCs可以表达星形胶质细胞(GFAP+)、少突胶质细胞(GalC+)和神经元(βIII+、NF160+等)的标志物,甚至表达神经干细胞标志物巢蛋白(nestin),但这些细胞的形态始终不成熟(呈球形、突起较少),提示其未能真正分化为成熟的功能性细胞。
与宿主神经回路的整合程度极低:即使在移植后6周,移植细胞仍缺乏成熟形态,难以与宿主脑组织建立有效的突触连接和神经回路整合。
功能改善不依赖细胞替代:在Zhao等人(2002)的大脑中动脉结扎模型中,移植hMSCs后缺血大鼠的肢体功能在2周和6周时均显著改善,但梗死体积并未减少。这表明行为学获益并非来源于移植细胞直接替代丢失的神经元或修复组织缺损。
实际治疗益处主要来自间接效应:MSCs更可能通过调节局部微环境(如分泌神经营养因子、抗炎因子、促进血管生成、抑制凋亡等)来支持内源性修复过程,而非直接替代受损细胞。
综上,在缺血性卒中背景下,MSCs的细胞替代策略不是治疗获益的核心途径,其作用更多是通过旁分泌和免疫调节等间接机制实现的。这一认识已得到临床前研究的广泛支持。
免疫调节和抗炎作用:平息过度激活的炎症风暴
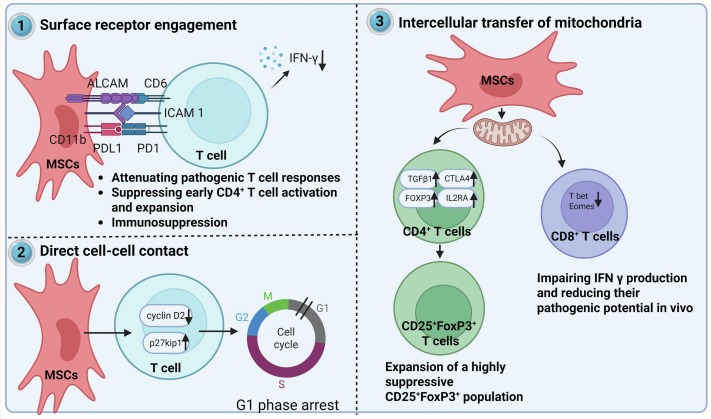
MSCs被视为缓解卒中后细胞因子风暴的潜在药物,这主要归功于其强大的免疫调节能力(图4)。该功能通过双重策略实现:一是直接与T细胞、B细胞、树突状细胞、巨噬细胞及自然杀伤细胞等多种免疫细胞相互作用;二是通过旁分泌释放可溶性介质进行间接调节。
直接调控T细胞,抑制异常活化。MSCs表面表达PD-L1、ALCAM、ICAM等多种黏附分子,可通过直接接触与T细胞表面受体结合。例如,PD-L1/PD-1及ALCAM/CD6相互作用能有效抑制T细胞的活化与扩增。这种接触还可使T细胞停滞于细胞周期G1期,在不诱导凋亡的前提下使其暂时“静默”,从而减少IFN-γ等破坏性细胞因子的产生。此外,MSCs可将自身线粒体转移至T细胞,此举能促进CD4+T细胞向调节性T细胞分化,同时削弱CD8+T细胞的细胞毒性。这些作用联合PGE2等可溶性因子,共同将过激的T细胞免疫反应下调,恢复炎症环境下的免疫稳态。
诱导巨噬细胞表型转化,传递抗炎信号。除调控T细胞外,MSCs还擅长调节巨噬细胞。它们可将易于诱发组织损伤的M1型巨噬细胞,转化为具有抗炎及促修复功能的M2型。这一转化伴随抗炎因子(如IL-10)水平升高,以及促炎因子(如TNF-α、iNOS)水平下降,从而显著改善局部炎症环境。
此外,MSCs释放的外泌体中富含miR-21、miR-223-3p等具有抗炎功能的微小RNA。这些miRNA进入周围细胞后,可抑制NLRP3炎症小体激活,调控NF-κB、JAK/STAT等炎症通路,并激活Nrf2/HO-1抗氧化轴,全面削弱炎症信号。对MSCs进行预处理(如高表达IL-10或低氧环境培养)后,其通过HIF-1α/VEGF/Nrf2等通路获得的抗炎、抗氧化能力将进一步增强(图5)。

疗效明确,但受限于细胞异质性。总体而言,MSCs通过直接接触免疫细胞、转移线粒体、释放外泌体等一系列机制,能系统性减轻卒中后的氧化应激与炎症反应,减少病理性免疫细胞向脑实质的浸润,为组织修复创造有利的微环境。但需客观指出,并非所有MSCs均具有等同的效应。供体年龄、组织来源及体外培养条件均显著影响其实际功能。这也在一定程度上解释了为何部分临床前研究与早期试验结果存在波动。因此,未来的临床应用可能需要根据患者个体情况制定差异化的治疗策略。
促血管神经发生:微环境重塑的双重收益
分泌活性因子与外泌体,直接滋养血管与神经。MSCs促进卒中后血管与神经新生,主要依赖其分泌的多种活性物质,如血管内皮生长因子(VEGF),以及脑源性神经营养因子(BDNF)、胶质细胞源性神经营养因子(GDNF)、神经生长因子(NGF)等。这些因子通过激活PI3K/Akt、ERK1/2等信号通路,一方面刺激内皮细胞增殖以形成新生血管,另一方面支持内源性神经干细胞的存活、增殖及向神经元分化。
同时,MSCs释放的外泌体携带蛋白质、mRNA及miRNA,递送至脑内后可增强缺血区周边的神经可塑性与血管生成,其效果在某些研究中甚至不逊于直接使用细胞。通过低氧预处理或过表达BDNF等策略,可上调HIF-1α,进而提高VEGF与BDNF水平,进一步增强促血管与神经保护效应。此外,MSCs与康复训练(如跑轮运动)或某些药物(如淫羊藿苷)联合应用,可协同提升VEGF与BDNF水平,获得更优的治疗效果。
调节免疫微环境,为修复清除障碍。除直接分泌因子外,MSCs还通过调节免疫环境间接促进血管与神经发生。它们能诱导巨噬细胞和小胶质细胞从促炎的M1型转向抗炎、促修复的M2型,从而提高IL-10水平、降低TNF-α与iNOS水平,减轻恶劣的炎症环境。
需要指出的是,M1/M2的二分法本身是对复杂生物学状态的简化,真实情境下这些细胞常呈现连续变化的混合表型。在此动态环境中,MSCs分泌CX3CL1、TGF-β、TSG-6、半乳糖凝集素-1等抗炎介质;其外泌体中的miR-21-5p还可通过靶向SPRY2/ERK轴及激活PTEN/AKT通路,进一步推动巨噬细胞向M2型转化。
综上,MSCs通过分泌因子、外泌体、基因增强及免疫调节这一整套组合策略,构建了一个协同作用的分子网络,同步驱动血管生成与神经发生,这与前述免疫调节机制形成了高效的联动。
给药途径:将细胞输送到大脑
选择最佳给药途径对于将间充质干细胞(MSCs)及其衍生物(例如细胞外囊泡,EVs)递送至大脑至关重要,需要在治疗效果、侵入性和安全性之间取得平衡(图6)。
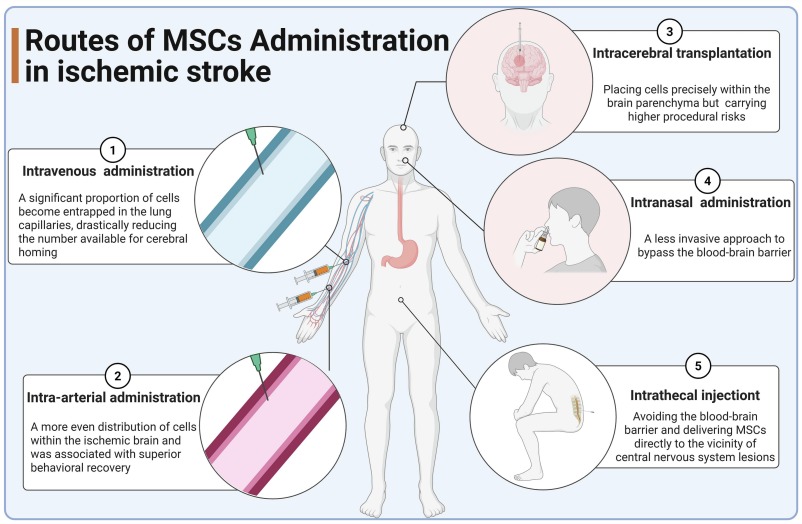
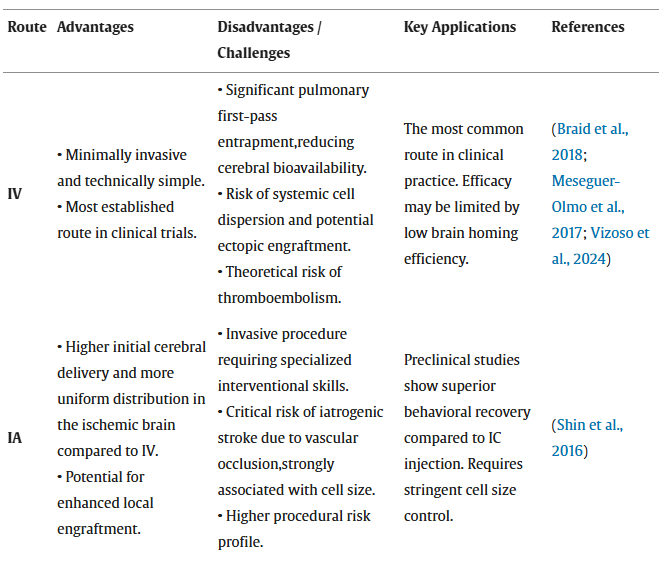
- 静脉输注最为常见,但细胞易滞留于肺毛细血管网,导致脑部归巢数量显著减少,且存在短暂植入、细胞衰老、栓塞及理论上的致瘤风险等障碍。
- 动脉内给药作为策略性替代方案,可使细胞在缺血脑组织中分布更为均匀,行为学恢复更佳。
- 脑内移植虽能将细胞精确递送至脑实质,但其侵入性高、手术风险大。
- 鼻内给药是一种微创方法,可有效递送MSC来源的细胞外囊泡进入大脑,已在神经退行性疾病模型中证实了其免疫调节与神经保护作用。
- 鞘内注射通过脑脊液循环,使治疗药物广泛分布于中枢神经系统,已成功用于缺血性卒中后遗症的治疗。
此外,重复全身注射MSC分泌组(无细胞疗法) 在帕金森病模型中亦显示出神经保护与促恢复效果。
总体而言,最佳给药途径的抉择需权衡三大因素:治疗药物的性质(细胞、外泌体或分泌组)、神经系统疾病的具体病理生理机制与阶段(如急性期或恢复期),以及最大化脑内生物利用度与最小化临床侵入性之间的核心平衡。静脉、动脉、脑内、鼻内、鞘内等不同途径各有其适用场景,临床决策应基于上述多维因素进行个体化考量,以追求最佳疗效与安全性(表2)。

临床转化:已完成和正在进行的试验
最早是2005年Bang他们做的开创性工作,给5个大脑中动脉梗死很重的病人静脉输注了自体的骨髓间充质干细胞,剂量一个亿。跟25个对照组比,治疗组的Barthel指数和改良Rankin评分在一年里持续改善,而且没有严重的细胞相关副作用,至少说明这条路安全、走得通(表3)。
| 疾病类型 | 细胞类型 | 行政路线 | 主要发现 | 参考 |
|---|---|---|---|---|
| 脑梗死患者,梗死部位位于大脑中动脉供血区,且伴有严重的神经功能缺损 | 自体骨髓间充质干细胞 | 静脉 | 安全性:未发生严重的细胞相关不良事件。 疗效:与对照组相比,1 年后 Barthel 指数和 mRS 评分均显著改善。 | (Bang等人,2005) |
| 严重大脑中动脉供血区梗死患者 | 自体骨髓间充质干细胞 | 静脉 | 安全性:已证实长期安全性,未发生与治疗相关的严重不良事件。 疗效:与对照组相比,mRS评分显著改善。 | (Lee等人,2010) |
| 严重大脑中动脉供血区梗死患者 | 自体骨髓间充质干细胞(预处理) | 静脉 | 安全性:未发生与治疗相关的严重不良事件。 | (Chung等人,2021) |
| 疗效:主要终点(3个月时mRS评分变化)未达到。与标准治疗相比,腿部运动功能(运动功能指数)有显著改善,尤其是在预测康复率较低的患者中。 | ||||
| 严重大脑中动脉供血区梗死患者 | 自体骨髓间充质干细胞 | 静脉 | 疗效:MRI 显示皮质脊髓束免受 Wallerian 变性的影响,运动网络连接性增强,与运动功能恢复相关。 | (Lee等人,2022b) |
| 非腔隙性梗死患者位于大脑中动脉供血区 | 自体骨髓间充质干细胞 | 静脉 | 疗效:MSC 治疗可增加循环 EV,这与运动功能改善和磁共振成像可塑性指标相关。 | (Bang等人,2022) |
| 中脑动脉区域严重缺血性卒中患者 | 同种异体脂肪间充质干细胞 | IV(急性/亚急性) | 安全性:已证实长期安全性(24 个月随访)。未发生注射相关不良事件或肿瘤。 疗效:AD-MSC 组患者在长达 24 个月的随访期间,NIHSS 评分和 mRS 评分中位数均略低于对照组,但差异无统计学意义。 | (德塞利斯-鲁伊斯等人,2022) |
| 亚急性缺血性卒中患者 | 自体骨髓间充质干细胞 | 静脉 | 安全性:可行且安全。 有效性:总体评分(Barthel指数、mRS评分)无差异。运动特异性评分显著改善,且初级运动皮层任务相关功能磁共振成像(fMRI)活动增强,提示神经可塑性增强。 | (Jaillard等人,2020) |
| 足月出生的新生儿,经MRI确诊为大脑中动脉区域PAIS | 同种异体骨髓间充质干细胞 | 鼻内给药;7天内单次给药(新生儿PAIS) | 安全性:耐受性良好。仅报告一例短暂轻度发热。未发生严重不良事件或意外的MRI异常。 | (Baak等人,2022) |
| 缺血性卒中后遗症患者 | 同种异体脐带间充质干细胞 | 鞘内注射与静脉注射 | 安全性:两种给药途径均安全。静脉给药途径不良事件发生率更低。 疗效:两种给药途径均改善了预后。静脉给药途径在6个月时即可显著改善NIHSS评分和FIM评分。 | (Nguyen等人,2025) |
到了2010年,Lee他们做了长期随访,平均21个月,确认长期安全性没问题,没出大事件,甚至隐约有点生存获益。
2021年发表的STARTING-2试验(注册号NCT01716481)算是比较关键的一个前瞻性开放标签随机对照,纳入了54个发病90天内的严重大脑中动脉梗死患者,一组单次输注预处理的自体MSCs,一组标准治疗。结果主要终点(3个月时的mRS变化)没做出显著差异,但次要分析里发现MSCs组的下肢运动功能明显更好,尤其是那些本来恢复希望不大的患者。
2022年这个试验的影像学亚组研究又指出,MSCs能保护皮质脊髓束不变性,增强运动网络的功能连接;同一年发表的生物标志物分析还发现,治疗后循环中的细胞外囊泡突然增多,增多的程度跟运动功能改善和神经可塑性变化相关,暗示细胞外囊泡可能不只是伴随现象,搞不好就是起效的载体。
还有一些试验把治疗窗口往前推了。比如2022年报道的AMASCIS试验,是个IIa期随机对照,针对60岁以上中重度卒中患者,在发病两周内单次静脉输注异体脂肪来源的MSCs,随访了24个月,没发现注射相关的不良事件,也没长肿瘤,长期安全性没问题。
2020年发表的ISIS-HERMES试验也是在亚急性期(卒中后两周内)给自体骨髓MSCs,虽然整体功能评分(Barthel、mRS)没有显著差别,但运动特异性评分(运动NIHSS、Fugl-Meyer)有明显改善,而且功能磁共振显示初级运动皮层的任务相关活动增强,说明感觉运动可塑性确实被调动起来了。
特别值得一提的是2022年报道的PASSIoN试验,这是头一回在新生儿围产期动脉缺血性卒中里尝试微创途径——鼻内给药。10个确诊大脑中动脉卒中的足月新生儿,症状出现7天内接受了一剂异体骨髓MSCs(4500万到5000万个细胞),耐受很好,只有一例短暂低热。到了2025年,Wagenaar他们发表了2年随访结果,MRI显示这些孩子的皮质脊髓束不对称发生率比历史对照低,运动能力也明显更好,有明确的神经保护迹象。
最近的是2025年Nguyen他们发表的II期随机对照试验,直接比较了鞘内注射和静脉注射脐带来源MSCs对32个慢性缺血性卒中后遗症患者的效果。两种途径都间隔3个月给两次,同时配合康复训练。结果两种方式都安全有效,12个月内神经功能和生活质量都有改善。静脉注射不良事件更少,而且在6个月的时候NIHSS和功能独立性评分就出现了显著改善。
总结一下,从2005年到2025年这二十年,不管是自体还是异体,骨髓、脂肪还是脐带来源,不管是静脉、鼻内还是鞘内给药,在急性期、亚急性期、慢性期,成人或者新生儿,间充质干细胞治疗的安全性都相当不错。对整体残疾程度的影响各试验结果还不完全一致,但在运动功能恢复这个具体层面,信号比较一致,影像学也支持MSCs确实有神经保护和增强可塑性的作用。接下来能不能真正用到临床上,关键就看能不能把更大规模的III期随机对照试验跑通,再把细胞产品、给药方案和患者筛选这些细节优化好。
常见问题解答(FAQ)
总结
自2005年Bang团队的开创性工作以来,间充质干细胞治疗缺血性卒中已从“急性期保命”发展为“长期神经修复”策略。其作用机制主要依赖免疫调节、促血管神经发生和旁分泌效应,而非直接细胞替代。二十年间,从成人到新生儿,从静脉到鼻内、鞘内,大量试验证实了良好的安全性和运动功能改善信号。
然而,疗效异质性、脑归巢效率低下、标准化方案缺失是通向临床应用的三大障碍。未来需要通过大规模III期RCT、细胞优化、无细胞外泌体替代以及工程化递送系统,将这一变革性策略真正转化为卒中后残疾负担降低的临床现实。
参考资料
[1] 间充质干细胞治疗缺血性卒中:机制与进展. Experimental Neurology, 2026年4月28日.
https://www.sciencedirect.com/science/article/abs/pii/S0014488626001597(其他原始研究引用已在文中标注,包括Bang 2005, Lee 2010, STARTING-2, AMASCIS, ISIS-HERMES, PASSIoN, Nguyen 2025等。)
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议。本文内容不能替代医生或药剂师的专业建议。所有治疗决策请咨询正规医疗机构专科医生。杭吉干细胞所发布的信息仅供参考。如有版权等疑问,请随时联系。




 扫码添加官方微信
扫码添加官方微信