描述:《Brain Sciences》2026年系统综述:间充质干细胞、神经干细胞、诱导多能干细胞治疗脊髓损伤的机制与临床证据。盘点国内外研究进展(中山三院iPSC完成首例给药),分析疗效异质性与致瘤风险,附常见问题解答。

引言:脊髓损伤——从“不可逆”到“可修复”的范式转变
脊髓损伤(Spinal Cord Injury, SCI)由创伤(如车祸、坠落)或非创伤性因素(如缺血、肿瘤)导致,造成损伤平面以下不同程度的感觉、运动及自主神经功能障碍。全球年发病率约为每百万人26.48例,男女比例约3.2:1,美国年发病率更高(约每百万人55例)。由于现有常规治疗仅能减轻继发性损伤、保留残余功能,无法实现神经组织再生,多数患者终生遗留严重残疾。
近年来,干细胞疗法凭借多向分化潜能、神经营养因子分泌、免疫微环境调节和促进轴突再生等特性,为脊髓损伤的神经修复开启了新可能。2026年发表于《Brain Sciences》的系统综述指出,间充质干细胞、神经干细胞及诱导多能干细胞等策略,可通过神经保护、髓鞘再生和轴突再生发挥修复作用[1]。
本文系统梳理主要细胞类型的研究进展与临床转化态势,分析疗效差异的核心原因,并展望未来方向。
脊髓损伤的病理双相与治疗困境
脊髓损伤由创伤性或非创伤性因素导致,造成损伤平面以下不同程度的感觉、运动和自主神经功能障碍。全球年发病率约为每百万人口26.48例,男女比例约3.2∶1;美国年发病率更高,约每百万55例(未计入入院前死亡病例),构成沉重的公共卫生负担。
脊髓损伤被认为分为两个阶段:原发性损伤和继发性损伤(图1),如图1所示的损伤进展模型所示。原发性损伤发生于创伤瞬间,由机械暴力直接造成神经结构破坏、出血和水肿;继发性损伤则在数小时至数周内演进,涵盖炎症反应、细胞凋亡、脱髓鞘、兴奋性毒性及胶质瘢痕形成等一系列分子和细胞级联事件。这一从急性机械损伤到慢性修复抑制的演进,划定了治疗干预的时间窗口,也决定了策略选择的基本逻辑。
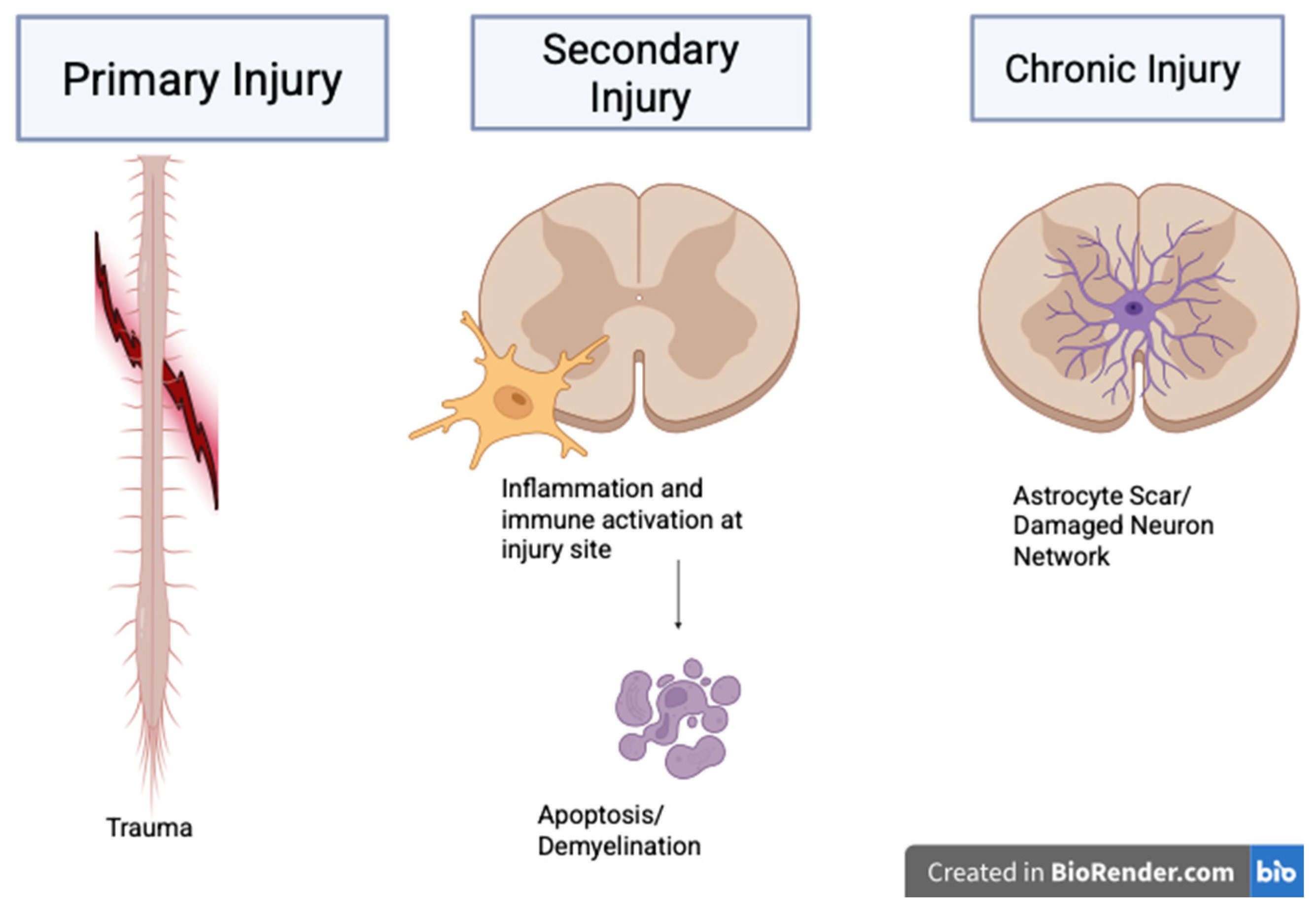
原发性损伤阶段涉及脊髓的即刻机械损伤,导致神经组织结构破坏。继发性损伤阶段随后到来,其特征是小胶质细胞和免疫细胞的激活,进而引发炎症反应、细胞凋亡和脱髓鞘,进一步加剧组织损伤。慢性期以星形胶质细胞激活介导的胶质瘢痕形成和神经元网络的持续破坏为标志,导致长期功能障碍。该图突出了SCI病理从急性机械损伤到慢性抑制性修复状态的顺序演变过程。
目前,临床常规治疗以早期手术减压(通常力争在伤后24小时内完成)、大剂量甲泼尼龙冲击、脊柱稳定及长期康复训练为主。这些措施虽能减轻继发性损伤、预防并发症并尽量保留残余功能,却无法从根本上修复受损神经组织或重建已丧失的神经功能。
正是在此背景下,干细胞疗法凭借多向分化潜能、神经营养因子分泌、免疫微环境调节和促进轴突再生等多重生物学特性,成为脊髓损伤再生修复领域的焦点。本文系统梳理间充质干细胞、神经干细胞、诱导多能干细胞、施万细胞及嗅鞘细胞等主要细胞类型的研究进展与临床转化态势,分析其修复机制与疗效证据,剖析当前核心挑战,并展望未来的发展前景。
干细胞疗法治疗脊髓损伤的主要细胞类型与研究进展
干细胞疗法作为脊髓损伤的治疗策略,其核心在于通过修复神经组织、调节炎症微环境、促进轴突再生及改善功能预后,实现对结构性及功能性缺陷的多靶点干预。该疗法所体现的多管齐下理念契合脊髓损伤复杂的病理本质,强调基于损伤类型与程度的个体化治疗必要性。
不同细胞类型、递送方式及联合疗法的探索反映了脊髓损伤异质性对治疗策略多样化的要求。然而,支持各疗法的证据强度因研究设计、损伤严重程度、干预时间窗口及细胞来源等因素而异,这些变量构成解读疗效差异的关键参数。
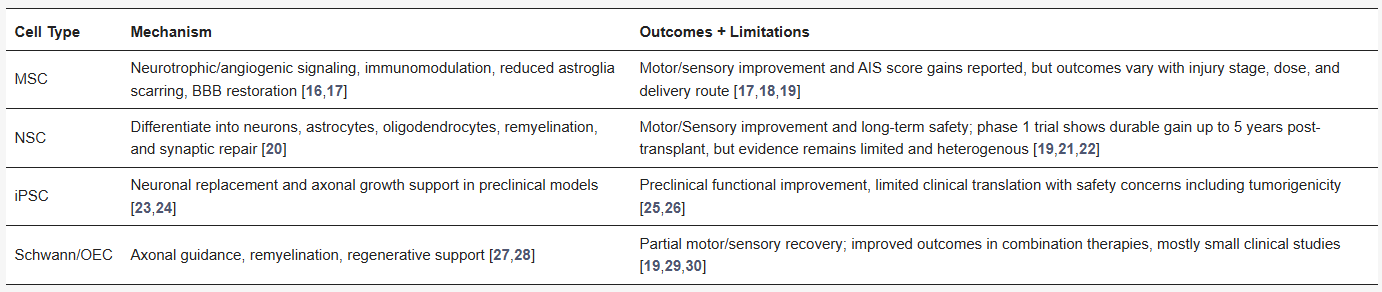
基于上述背景,目前被广泛研究的细胞类型主要包括间充质干细胞、神经干细胞与祖细胞、诱导多能干细胞以及神经支持细胞,各自的机制与临床证据呈现显著差异。表1总结了主要的基于细胞的再生策略。
间充质干细胞:旁分泌主导的免疫调节与营养支持
间充质干细胞(MSCs)是目前脊髓损伤治疗领域研究最为广泛和深入的干细胞类型。MSCs可来源于骨髓(BM-MSCs)、脐带(UC-MSCs)以及华通胶(WJ-MSCs)等多种组织,具备多向分化能力和低免疫原性,这一特性使其在异体移植中具有明显优势,因较低的免疫排斥风险有助于改善患者预后。
MSCs治疗脊髓损伤的修复机制并非以直接分化为神经元并替代受损细胞为主,而是主要通过旁分泌效应发挥神经营养、免疫调节和促血管生成等多重活性。具体而言,MSCs可分泌脑源性神经营养因子(BDNF)、神经生长因子(NGF)等多种神经营养因子,促进损伤区神经元的存活与轴突再生;同时通过调节小胶质细胞/巨噬细胞的极化状态——抑制促炎性M1表型、促进抗炎性M2表型——来改善损伤区的炎症微环境。
在临床研究层面,2025年12月,一项针对26项间充质干细胞治疗脊髓损伤的临床研究系统分析表明,MSC移植在脊髓损伤患者中具备良好的安全性,所有研究均报告了不同程度的功能改善和神经功能缺损减轻,但疗效在不同研究之间存在显著异质性。

2025年5月,一项采用WJ-MSCs经多途径(鞘内、肌肉内及静脉)联合给药的I期研究显示,慢性完全性脊髓损伤患者在治疗后1年随访期内,ASIA运动评分和排尿功能相关生活质量评分均获得统计学显著改善,但该研究未设对照组,且未能控制同期药物与康复治疗的混杂效应,因此结果解读需持审慎态度。

值得注意的是,2026年3月,一项针对慢性不完全性颈髓损伤的I/II期随机双盲安慰剂对照试验显示,虽然鞘内注射WJ-MSCs总体安全性良好,但在主要疗效终点上,治疗组与安慰剂组之间未观察到显著的组间差异。这种疗效的不一致性进一步印证了MSC治疗中剂量、时机和个体化方案的优化需求。

神经干细胞与神经前体细胞:神经替代与髓鞘重建
神经干细胞和神经前体细胞(NSCs/NPCs)具备分化为神经元、星形胶质细胞和少突胶质细胞的能力,能够直接参与损伤后髓鞘再生和突触重建。与MSCs主要通过旁分泌发挥修复作用不同,NSCs的优势在于其固有神经谱系分化能力,可替代丢失的神经元和胶质细胞、为幸存轴突重新形成髓鞘、分泌神经营养因子,甚至可能在宿主与移植物之间形成中继回路,重新连接中断的神经通路。
在递送方式上,直接的髓内移植能够实现最精准的移植物定位,已在早期临床试验中展现出令人鼓舞的安全性和初步疗效信号。一项利用人脊髓源性神经干细胞进行的I期临床试验表明,所有受试者对移植耐受良好,且在移植后长达五年的长期随访中观察到持久的运动和感觉评分改善。
此外,2025年5月,全球首个利用人胚胎干细胞系分化获得PSA-NCAM阳性神经前体细胞治疗AIS-A级亚急性脊髓损伤的I/IIa期临床试验也正在进行中,旨在系统评估其安全性和初步疗效。

这些研究共同展现了NSC在脊髓损伤修复中的临床潜力,但现有证据仍主要来自小规模早期临床试验,疗效尚需更大样本的随机对照研究加以验证。
诱导多能干细胞:个体化再生的新前沿
诱导多能干细胞(iPSCs)是通过重编程成体体细胞获得的类胚胎干细胞,具有无限的增殖能力和向各类神经细胞分化的潜能。iPSCs技术的出现为脊髓损伤治疗开辟了新途径——既克服了胚胎干细胞涉及的伦理争议,又解决了异体移植中的免疫排斥问题,可实现患者特异性的个体化治疗。
在作用机制方面,iPSC来源的神经细胞不仅能在体内分化为成熟的神经元和胶质细胞以替代受损细胞,还能通过调节损伤微环境——促进小胶质细胞和星形胶质细胞向抗炎、神经保护表型极化——来改善宿主环境,进而促进轴突再生、髓鞘修复和运动感觉功能恢复。
在临床转化方面,领域进展显著:由中山大学附属第三医院等机构联合推动的全球首个iPSC衍生亚型脊髓神经前体细胞新药(XS228细胞注射液)已完成首例受试者给药,初步观察显示患者在短期内即出现了运动功能的令人惊喜的改善。该产品的后续II期随机双盲安慰剂对照试验已规划入组约60例胸腰段亚急性脊髓损伤患者,以ASIA运动评分作为主要终点。

然而,iPSCs在临床应用中的核心挑战在于其潜在的致瘤风险。由于iPSCs可能携带发生肿瘤转化所需的基因或表观遗传学异常,移植后的肿瘤形成风险构成了当前临床推广的最大安全障碍,亟需长期安全性随访数据来对其进行系统评估。
施万细胞与嗅鞘细胞:神经支持的独特补充
除了上述三大类干细胞,施万细胞(Schwann cells)和嗅鞘细胞(OECs)这两种神经系统的支持细胞也在脊髓损伤修复中展现出应用潜力。施万细胞是外周神经系统的髓鞘形成细胞,可在损伤部位促进轴突髓鞘再生;嗅鞘细胞则兼具施万细胞和星形胶质细胞的特性,具有引导再生轴突穿越胶质瘢痕的独特能力。美国FDA已批准首个施万细胞移植治疗脊髓损伤的I期临床试验。
综合上述各类细胞疗法的证据,可以得出结论:联合应用多种细胞类型有望通过不同机制的互补协同效应,产生更全面的再生效果,而单一细胞疗法的疗效受限于损伤阶段、细胞来源及给药策略等多重因素。未来研究需着力于标准化实施方案,并开展长期随访以验证安全性及有效性。
五、安全性考量与疗效异质性分析
已知安全性问题
| 细胞类型 | 主要安全风险 | 是否可控 |
|---|---|---|
| MSCs | 低免疫原性,罕见感染、栓塞 | 可控 |
| NSCs | 移植相关手术风险(髓内注射) | 较可控 |
| iPSCs | 致瘤性、异常分化 | 当前最大障碍 |
| 施万细胞/OECs | 无明显特异性严重风险 | 可控 |
疗效不一致的可能原因
- 损伤阶段差异:亚急性期(伤后2周内)效果最好;慢性期胶质瘢痕阻碍移植物存活。
- 细胞类型与剂量:不同来源、代次、活力细胞疗效差异大。
- 递送方式:鞘内、静脉、髓内直接注射各有优劣。
- 结局指标选择:运动评分(ASIA)、感觉评分、膀胱功能改善往往不平行。
- 个体异质性:患者年龄、损伤等级、合并症等。
六、常见问题解答(FAQ)
七、结语与展望
干细胞疗法代表了脊髓损伤治疗从传统对症康复向神经再生修复的范式转变。经过数十年研究,MSCs、NSCs和iPSCs已在多种模型中显示出明确修复潜力,部分产品进入早期临床并报告了令人鼓舞的信号——尤其是中山大学附属第三医院主导的全球首例iPSC衍生神经前体细胞给药。
然而,疗效异质性、最佳方案未知,以及iPSC的致瘤风险,共同决定了干细胞疗法距离常规临床实践仍有相当距离。未来需要:
- 开展更大规模、随机双盲、多中心III期试验
- 建立标准化的细胞制备与质控体系
- 探索联合治疗策略(细胞+电刺激+康复)
- 进行长期(≥10年)安全性随访
干细胞疗法有望在未来5-10年脊髓损伤治疗领域实现突破性进展,为数百万患者带来真正意义上的功能重建与生活质量改善。
参考资料:
[1]:Anwar, A.I.; Abd-Elsayed, A.; Kaye, A.D. Regenerative Medicine Strategies for Spinal Cord Injury: Advances in Stem Cell Therapy. Brain Sci. 2026, 16, 461. https://doi.org/10.3390/brainsci16050461
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信