神经退行性疾病严重侵蚀患者生活质量,然其有效疗法仍如晨星般稀缺。传统治疗多聚焦于症状缓解,难以触及疾病根源。间充质干细胞,因其兼具自我更新与多向分化潜能,成为再生医学领域,尤其是神经系统疾病治疗中备受瞩目的候选者。
从76项研究看未来:MSC如何加速推进阿尔茨海默病、帕金森病的临床转化
为精准评估间充质干细胞在神经系统疾病中的临床应用价值,2026年2月21日,《Biomedicines》期刊发表了一项系统性综述,题为“间充质干细胞疗法在神经系统疾病中的应用”[1]。

该综述通过对过往文献的全面梳理,勾勒出该领域的核心图景:总体而言,现有证据一致表明,间充质干细胞及其衍生物对多种神经退行性疾病具有疾病修饰作用。在阿尔茨海默病、帕金森病、亨廷顿病和肌萎缩侧索硬化症的临床前研究中,科学家们反复观察到行为学结局的改善、神经炎症的减轻以及神经保护效应——这些获益主要由MSCs的旁分泌信号所介导,而非源于直接的细胞替代。
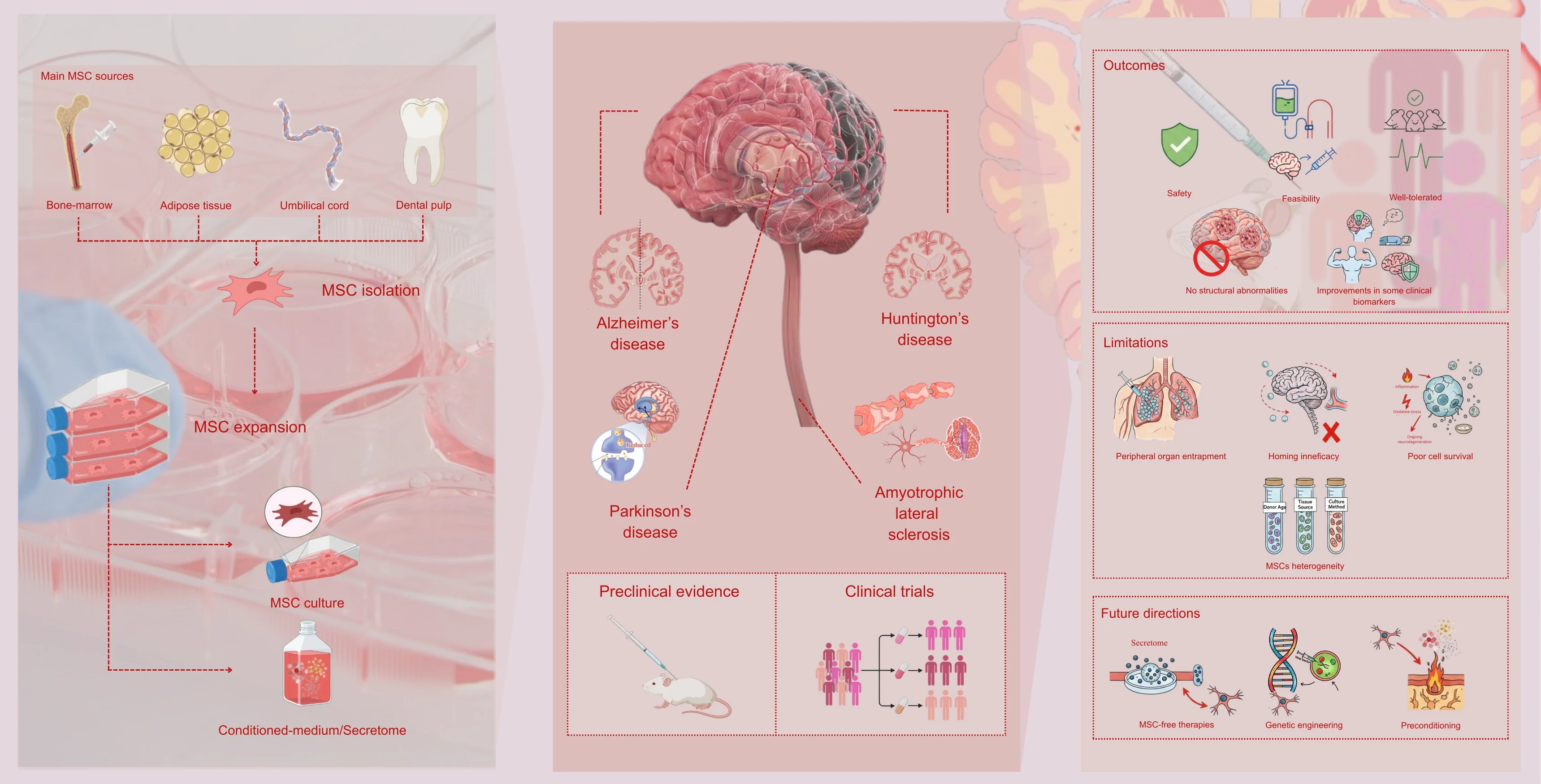
该综述并非简单的罗列,而是旨在构建一座从实验室通往病床的认知桥梁。其对基于MSC的疗法在上述四种疾病中的应用进行了比较与转化视角下的剖析,尤其着力于厘清两条线索:一是区分确凿的临床前证据与仍显单薄的早期临床试验结果;二是评估基于完整细胞的疗法与基于分泌组的新型策略;三是探讨旨在突破当前转化障碍的前沿技术方案。
研究方法:循证筛选,严控标准
本研究恪守系统综述的方法论圭臬,严格遵循PRISMA指南进行文献检索与筛选。研究团队在PubMed数据库中,针对2010年至2025年间发表的文献展开系统检索,通过构建包含“间充质干细胞”与“阿尔茨海默病”、“帕金森病”、“亨廷顿病”、“肌萎缩侧索硬化症”四大关键词的检索策略,初步锁定485篇相关文献(图1)。
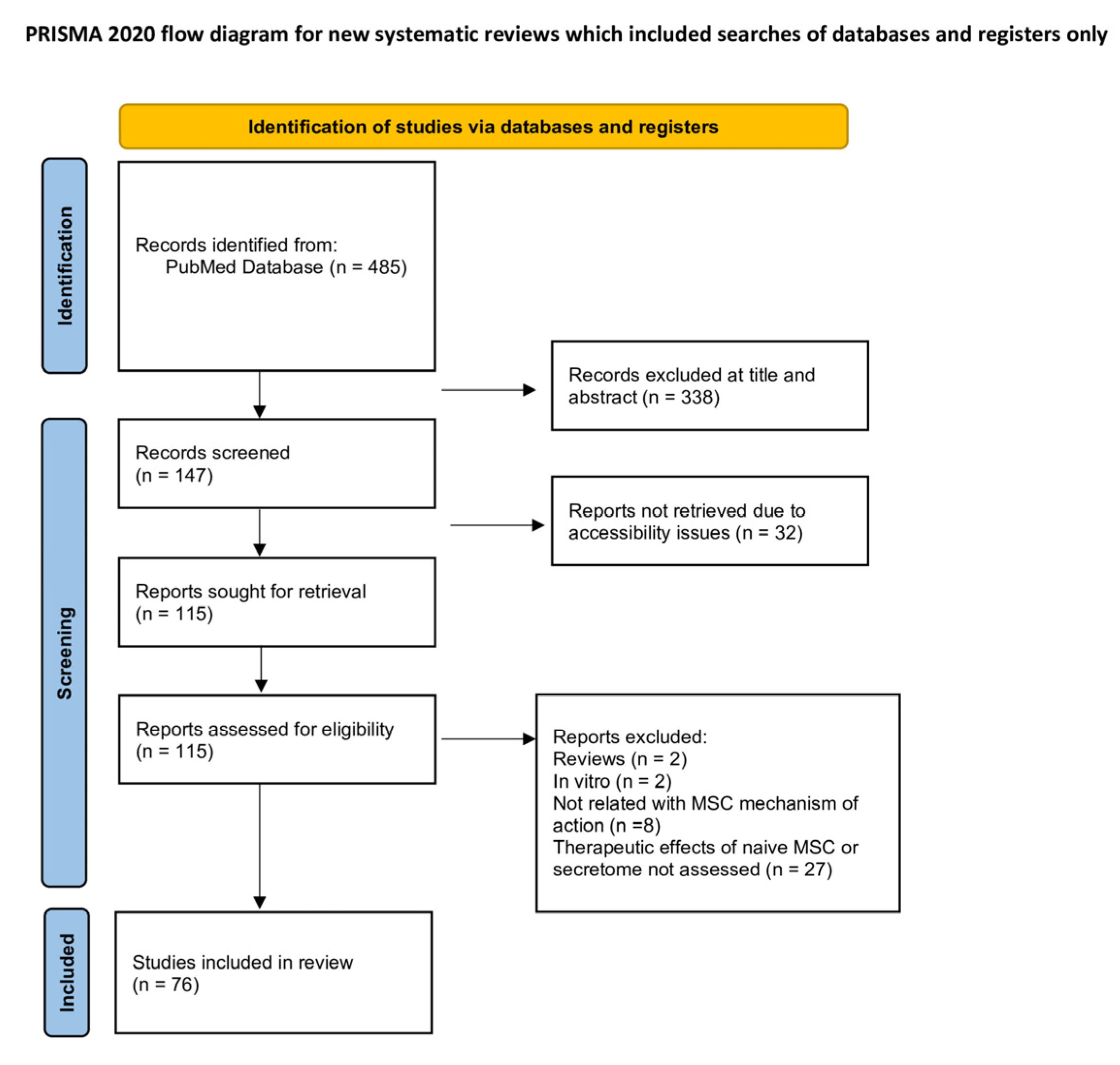
图1:PRISMA流程图,概括了选择过程。
筛选过程采用多阶段、标准化的流程。借助Rayyan网络应用程序剔除重复文献后,经过标题与摘要的初步筛选,排除338篇;再经由全文复筛,剔除71篇,最终将符合全部预设标准的76项研究纳入分析。纳入标准极为严格,仅限于涉及原始间充质干细胞或其分泌组的体内动物研究及临床试验,明确排除了体外研究、综述、非英文发表,以及涉及基因修饰或分化干细胞的研究。
间充质干细胞靶向神经系统疾病的治疗策略
干细胞因其自我更新、复制、再生与分化的内在禀赋,正驱动着科学家探寻其干预神经退行性疾病的有效方案。下文将分述MSC在四种典型疾病中的研究进展。
间充质干细胞与阿尔茨海默病:从病理靶向到临床曙光
阿尔茨海默病(AD)是神经退行性疾病中最常见的类型之一,主要影响老年人群。临床上,AD与痴呆症相关,其特征是进行性记忆丧失和一个或多个认知领域的损害。退行性变主要影响海马和皮质神经元,包括谷氨酸能和胆碱能神经元群,导致记忆丧失和认知能力下降(图2)。
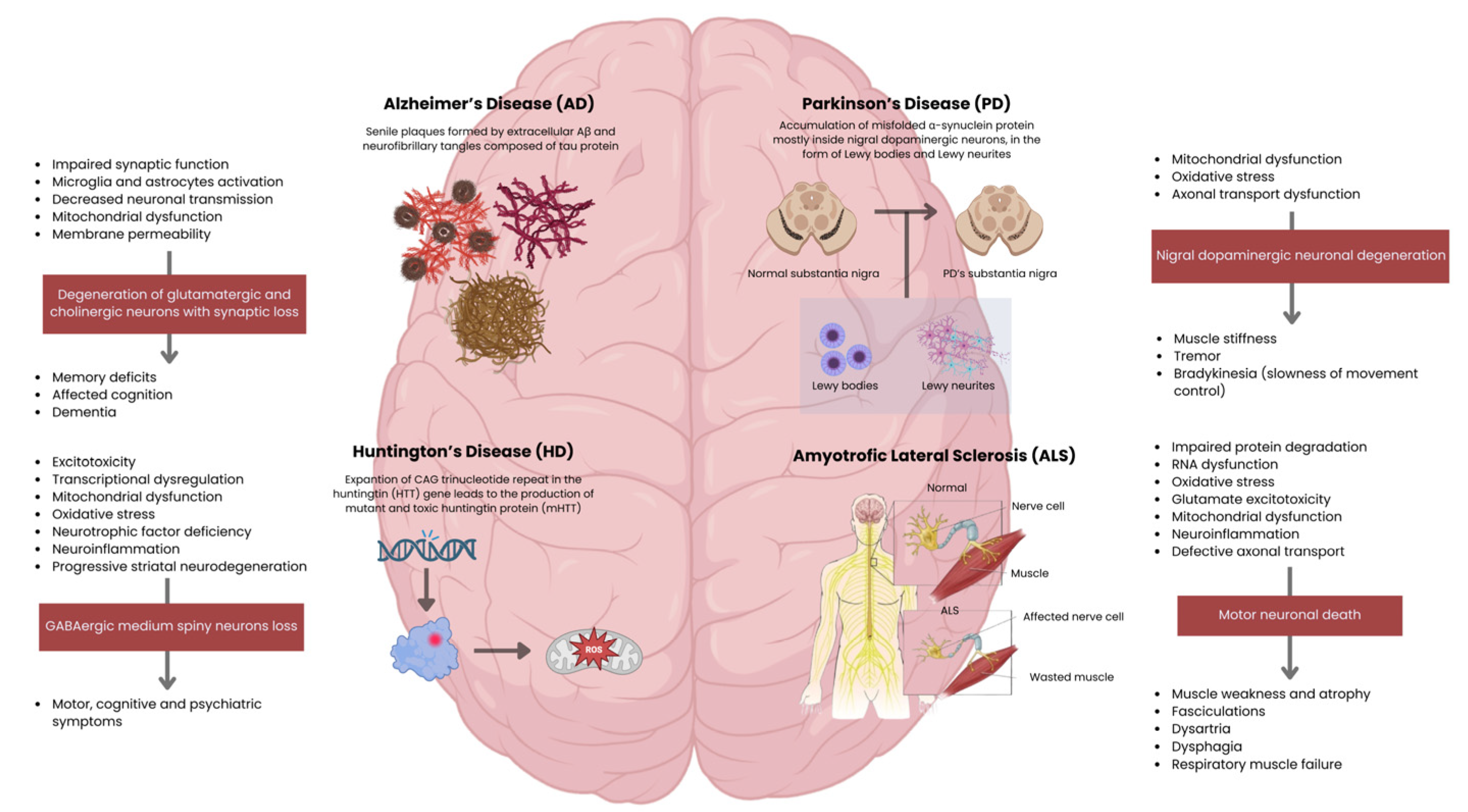
图2:主要神经退行性疾病的病理生理机制和临床特征。侧边栏概述了从细胞功能障碍到特定神经元丢失以及随后临床表现的进展过程。
针对AD的治疗,MSC的切入点直指其两大核心病理特征:β-淀粉样蛋白沉积形成的老年斑,以及Tau蛋白过度磷酸化缠结而成的神经原纤维缠结。这些病理改变不仅直接破坏突触通讯,更激活小胶质细胞与星形胶质细胞,诱发慢性神经炎症,释放炎症因子与活性氧,加剧神经元损伤。
此外,可溶性Aβ与Tau寡聚体亦具显著神经毒性,可引致线粒体功能障碍与膜通透性改变。鉴于现有疗法仅能缓解症状,而针对Aβ与Tau的靶向药物临床试验尚未取得理想突破,MSC疗法因其多靶点作用的潜力而备受瞩目。
丰富的临床前研究为MSC治疗AD提供了坚实的证据链。在多种AD动物模型中,无论通过海马内、脑室内、鼻腔或静脉途径给予不同来源的MSCs或其衍生物,研究者均观察到一致的治疗效果:Aβ负荷降低、斑块形成减少、神经炎症得到调节(小胶质细胞向抗炎表型转变)、Tau蛋白过度磷酸化水平下降,最终体现为动物空间学习与记忆能力的改善。
机制研究表明,这些获益主要依赖于MSC的旁分泌效应——通过分泌神经营养因子、免疫调节分子与细胞外囊泡,发挥神经保护、突触维持与促进神经发生的作用,而非依赖细胞的长期植入与替代(图3)。
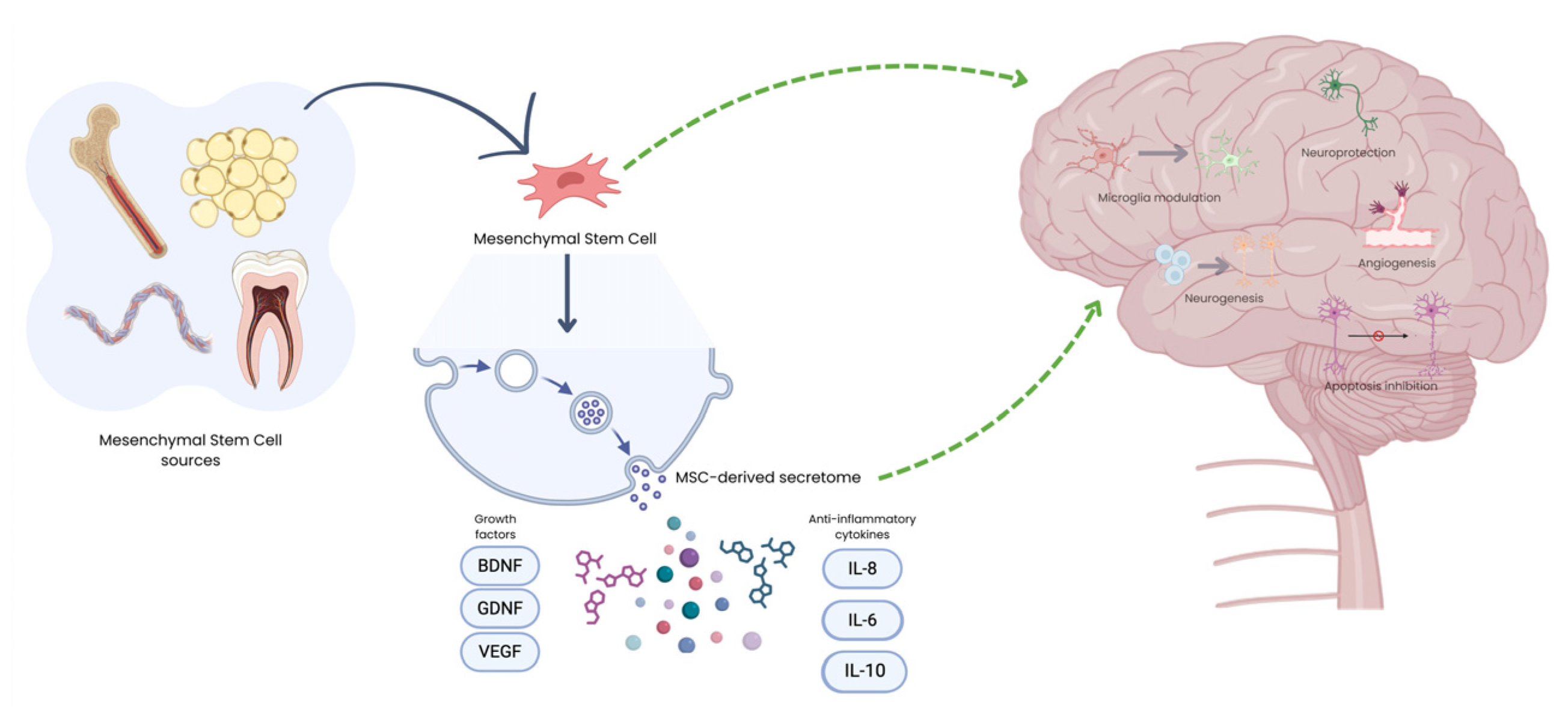
图1:MSC来源及其在神经退行性疾病 (ND) 中的治疗机制示意图。给药后,MSC 主要通过释放生物活性分泌组发挥作用,该分泌组由细胞外囊泡 (EV)、生长因子和免疫调节细胞因子组成。深蓝色曲线箭头表示从不同来源获取MSC,而绿色箭头表示MSC或其分泌组的作用机制。
在临床转化方面,针对AD的MSC疗法已从早期安全性试验迈向更高级的研究阶段。
2021年,一项针对阿尔茨海默病的I期临床试验显示,通过Ommaya储液囊向侧脑室重复注射三次人脐带血间充质干细胞 (hUCB-MSCs) 是可行的,且相对安全,耐受性良好。目前,我们正在对参与IIa期试验的患者进行一项长期随访研究,希望在研究完成后,能够更深入地了解MSC阿尔茨海默病疗法的临床疗效。

向阿尔茨海默病痴呆患者脑室内注射人脐带血间充质干细胞:一项 I 期临床试验
2025年,一项针对同种异体骨髓间充质干细胞(BM-MSC)疗法Laromestrocel的IIa期随机对照试验,在49名轻度AD患者中证实了其安全性,并初步观察到疗效信号,包括联合治疗组脑与海马萎缩减缓以及临床评分改善,且这种结构保护与认知功能相关。然而,该试验样本量较小且持续时间仅为39周。

必须正视的是,当前从早期临床试验中获得的证据强度,尚无法与临床前模型的丰硕成果相媲美。大量动物研究在高度可控条件下一致证实MSC能改善认知、减轻病理,但这些发现未必能完全外推至复杂的人类疾病。目前的临床证据仍主要集中于以评估安全性与可行性为首要目标的I期和早期II期试验,样本量小。
尽管认知功能稳定、脑萎缩减缓等信号令人鼓舞,但仍处于探索阶段,无法得出关于确切疗效的确定结论。因此,在解读临床前研究的积极结果时须保持审慎,同时必须强调开展更大规模、更具针对性且长期随访的临床试验,以验证该疗法在AD中的转化潜力。
间充质干细胞与帕金森病:疗效信号与试验困局
MSC在帕金森病治疗中的潜力,根植于针对其核心病理机制的广泛临床前探索。PD的主要特征是由α-突触核蛋白异常积聚所导致的黑质纹状体多巴胺能神经元进行性丧失,进而引发运动功能障碍。
大量来自毒素诱导与基因修饰动物模型的证据表明,基于MSC的疗法能有效减轻多巴胺能神经元退化、减少神经炎症并改善运动表现。这种治疗效果主要归因于MSC的旁分泌作用——通过释放脑源性神经营养因子和胶质细胞源性神经营养因子等分子,保护神经元、调节免疫反应,并减少α-突触核蛋白聚集,从而对疾病的多重病理特征产生调节作用。
基于这些临床前发现,早期人体临床试验已初步验证了MSC疗法在PD患者中的安全性与可行性。
2021年,一项单中心、开放标签、剂量递增的I期临床试验,纳入20名轻度至中度PD患者,评估单次静脉输注的安全性与耐受性。该研究达到了主要安全性终点,表明输注安全、耐受性良好且无免疫原性。在探索性疗效方面,最高剂量组显示出最显著的临床获益,第52周时统一帕金森病评定量表(UPDRS)运动评分持续降低。从生物学角度看,这种临床改善伴随着外周炎症标志物减少与BDNF水平升高的强效免疫调节作用。

基于I期结果,2025年,研究者进一步开展了一项II期随机、双盲、安慰剂对照试验,纳入45例患者,评估重复静脉输注异体BM-MSC的疗效。受试者被随机分配接受3次活性药物、2次活性药物(首次为安慰剂)或3次安慰剂输注,每次间隔18周,持续36周。该研究达到了主要终点,再次证实安全性,未报告严重不良事件或免疫原性。

然而,该II期试验揭示了一个令人困惑的矛盾:接受两次输注的组别,其疗效显著差于安慰剂组,改善甚微。此外,对照组中观察到的显著安慰剂效应,使结果解读更为复杂。其他局限性包括单中心设计限制了结果的普遍适用性,以及样本量较小。
这一现象深刻揭示了当前研究的复杂性:尽管高频输注组呈现积极结果,但剂量-反应关系的非线性、安慰剂效应的干扰,以及患者异质性、给药方案标准化不足等问题,都使得现有临床证据难以与高度一致的临床前研究相匹配。因此,尽管临床前与早期临床研究均显示积极信号,但MSC治疗PD的确切疗效,仍需通过更大规模、设计更严谨、随访时间更长的多中心随机对照试验来加以验证与确认。
亨廷顿病:临床前潜力与转化断层
间充质干细胞在治疗亨廷顿病方面的研究策略,并非直接针对其根本的遗传病因——突变的亨廷顿蛋白,而是致力于减轻由其引发的下游病理过程。HD是由HTT基因CAG重复序列扩增导致的显性遗传病,主要引起纹状体GABA能神经元进行性退化,并伴随兴奋性毒性、线粒体功能障碍、神经营养因子缺乏及神经炎症等多重机制。
因此,基于MSC的治疗旨在通过其旁分泌作用,提供神经营养支持、调节神经炎症环境,从而延缓神经元死亡与疾病进展,而非修正潜在的基因缺陷。
来自多种HD转基因动物模型的临床前研究为MSC疗法的有效性提供了证据。研究表明,通过纹状体内移植或鼻内给药等方式施用MSCs,可在一定程度上保护纹状体结构、改善运动协调性,并延缓疾病进展。其作用机制主要与减少细胞凋亡和神经炎症、上调BDNF等神经营养因子水平有关。然而,研究结果亦显示出一定异质性,例如对认知功能的改善效果通常有限,这可能与动物模型、细胞来源及给药策略的差异有关。
肌萎缩侧索硬化症:短暂改善与重复给药的需求
间充质干细胞在治疗肌萎缩侧索硬化症方面的应用,主要基于其针对运动神经元进行性死亡的神经保护与免疫调节作用。
ALS是一种致死性极高的神经退行性疾病,其特征为运动神经元选择性丧失,导致肌肉无力、萎缩直至呼吸衰竭。尽管其确切机制尚不完全明确,但基于SOD1等动物模型的研究表明,蛋白质稳态失衡、氧化应激、谷氨酸兴奋性毒性和神经炎症等均参与其中。
因此,MSC治疗策略并非直接修复遗传缺陷,而是利用其旁分泌功能,通过分泌BDNF、GDNF和抗炎细胞因子,调节小胶质细胞和T细胞的异常活化,保护运动神经元免受兴奋性毒性与氧化应激的损害。
来自ALS转基因动物模型的临床前研究为MSC疗法的有效性提供了丰富证据。系统评价与荟萃分析显示,MSC移植能够显著延缓疾病发病、减缓临床进展并延长生存期。这些益处在鞘内、脑室内、鼻内和静脉等多种给药途径后均被观察到,其作用机制主要涉及免疫调节、减少神经炎症以及促进脊髓血管修复。
在临床转化方面,早期人体试验已初步证实了MSC疗法在ALS患者中的安全性与可行性。
2016年,一项II期开放标签临床试验表明,重复鞘内注射自体骨髓间充质干细胞安全且耐受性良好。在疗效方面,该研究观察到部分患者疾病进展速度显著降低,且临床获益与给药频率相关,提示需重复给药以维持效果。其他早期临床试验亦证实,脊髓内自体BM-MSC输注在数月至数年的随访期间未出现严重移植相关毒性或肿瘤形成。此外,26例患者接受鞘内BM-MSC输注后,疾病进展暂时减缓,且许多患者的用力肺活量在数月内保持稳定。

2021年Petrou等人开展的一项单中心、开放标签II期临床试验,纳入20名患者,评估重复鞘内注射自体BM-MSC的安全性与有效性。结果表明,该疗法安全且耐受性良好,未发生与MSC给药直接相关的严重不良事件。疗效方面,研究报告称疾病进展速度显著降低;许多患者被归类为有效应答者,与治疗前导入期相比,他们的ALS功能评定量表修订版(ALSFRS-R)评分斜率改善更为显著,部分患者甚至表现出实际的临床改善。

值得注意的是,该研究强调,临床获益似乎是短暂的,并且与给药频率相关,注射间隔越短,疗效越显著,这表明需重复给药周期以维持治疗效果。类似的重复鞘内注射方案在12个月内亦显示出可接受的安全性。
临床转化的瓶颈:为何MSC疗法迟迟未能普及?
尽管间充质干细胞在临床前研究与早期临床试验中展现出良好的安全性与多靶点生物活性,但其向临床的规模化转化仍横亘着多重屏障。
其一,生物利用度不足。MSCs在中枢神经系统内的存活率低、归巢效率差,全身给药后大量细胞滞留于外周器官,且难以穿透血脑屏障,导致抵达靶区的细胞数量远不足以发挥预期效应。
其二,产品异质性显著。MSCs本身存在显著的异质性——不同组织来源、供体特征、培养条件等因素均会影响其分泌谱与治疗效力,使得各研究结果难以直接比较,临床疗效也因此出现较大差异。
其三,给药策略缺乏标准化。临床前研究中给药方案缺乏系统的剂量-反应评估,导致人体试验的剂量与途径多为经验性选择,进一步削弱了转化研究的可靠性。
其四,机制理解与监管框架尚不完善。由于对MSCs作用机制的理解尚不完全,缺乏能够反映其功能异质性的效力检测方法和统一的监管框架,这使得MSCs作为复杂生物制品的临床开发难以获得可比性数据。这些因素共同导致目前尚无足够证据支持MSCs在神经退行性疾病中的确切疗效,因此迟迟未能实现大范围临床应用。
未来方向:聚焦关键环节,突破转化壁垒
为突破上述瓶颈,未来研究需从多个关键环节协同发力。
一是优化细胞的存活与靶向能力。通过预处理或基因修饰等技术,增强MSCs在病变微环境中的适应性与中枢神经系统归巢效率,从根本上提升其生物利用度。
二是推动从细胞疗法向分泌组疗法的转变。基于细胞外囊泡的疗法可规避细胞存活与归巢的限制,同时保留旁分泌效应,有望实现更微创、更可控的治疗。
三是建立标准化的研究框架。明确不同来源MSCs的“适用性”特征,根据疾病病理机制合理选择细胞类型,并系统评估剂量-反应关系,以优化给药方案。
四是开发机制驱动的效力检测方法。将免疫调节、神经营养等核心功能与具体疾病通路关联,形成统一的监管评估体系,为临床开发提供可比性数据。
五是扩大临床试验规模。注重患者分层与长期随访,验证疗效并推动治疗方案的标准化与可扩展性,为最终临床应用奠定坚实基础。
总结与展望
本综述系统梳理了间充质干细胞在阿尔茨海默病、帕金森病、亨廷顿病与肌萎缩侧索硬化症等神经退行性疾病中的研究脉络。尽管早期临床试验证实了MSCs的安全性,并观察到一些生物学效应,但后期试验匮乏,临床疗效有限,主要受限于细胞存活率低、归巢效率差、产品异质性大、剂量方案不明确以及缺乏效力检测标准等问题。
展望未来,随着对MSCs作用机制理解的深入,结合预处理、基因修饰、分泌组技术以及标准化研究框架的建立,有望开发出更精准、高效且微创的治疗策略。特别是基于细胞外囊泡的疗法与非侵入性给药途径的探索,将为神经退行性疾病的干预提供新的可能。
最终,通过多学科协作与规范化临床转化,MSCs及其衍生物或将成为这类复杂疾病治疗图景中的重要组成部分。
参考资料:
[1]:Trabulo, A.; Sousa, P.; Alvites, R.; Maurício, A.C. Mesenchymal Stem Cell-Based Therapies Applied in Neurological Diseases: A Systematic Review. Biomedicines 2026, 14, 475. https://doi.org/10.3390/biomedicines14020475
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信