核心速览:间充质干细胞(MSC)通过免疫调节、抗纤维化、促再生及铁死亡调控四重机制,在肝病治疗中展现独特价值。临床研究证实,MSC可改善酒精性肝硬化患者Child-Pugh评分(下降2-3分)及白蛋白水平(提升15%-20%);在肝衰竭中,异体MSC输注将24周生存率从55.6%提升至73.2%;病理研究亦提供了纤维化逆转的直接组织学证据(Laennec评分显著降低)。安全性良好,未见致瘤性报告。当前瓶颈在于归巢效率低与细胞异质性,工程化细胞外囊泡、基因编辑及AI标准化策略正推动临床转化。
南方医科大学最新综述:间充质干细胞修复肝脏的核心机制与临床进展
01 引言:肝病治疗的未满足需求与MSC的潜力
肝病(包括肝硬化、病毒性肝炎、酒精性肝病、肝衰竭等)是全球范围内导致死亡和残疾的主要原因之一。终末期肝病的唯一根治手段是肝移植,但供体短缺、免疫排斥及高昂费用限制了其广泛应用。
间充质干细胞凭借其独特的免疫调节特性、多向分化潜能与旁分泌功能,在肝组织修复与疾病治疗领域展现出重要潜力。MSC并非作为“细胞替代物”直接分化为肝细胞,而是以“药用信号细胞”的身份,通过协同网络重塑病理微环境。
近期,由广州南方医科大学第一临床医学院牵头,联合深圳市龙华区人民医院、西安国际大学医学院共同完成的研究综述发表于《Frontiers in Medicine》(洛桑版),题为《利用间充质干细胞治疗肝病:从机制发现到临床突破》[1]。本文基于该综述及其他关键临床证据,系统梳理MSC治疗肝病的机制、临床试验数据及未来转化策略。

间充质干细胞(MSCs)在肝病治疗中的作用并非依赖单一通路,而是通过协同网络重塑病理微环境。MSCs并非仅作为细胞替代物,而是以“药用信号细胞”的身份,通过四个层级协调组织修复:免疫调节、直接抗纤维化干预、促进再生与新兴代谢调控。
02 间充质干细胞介导肝脏修复的四大机制
一、免疫调节:重塑肝脏免疫微环境(图1A)
MSCs通过固有免疫调节能力重塑肝脏微环境,其核心机制在于将巨噬细胞由促炎M1表型极化为抗炎修复型M2表型,这一过程依赖TSG-6、IL-10等可溶性因子。在IFN-γ与TNF诱导的炎症环境下,MSCs上调PD-L1与IL-10,促进调节性T细胞生成,并通过IDO降解色氨酸抑制CD4+T细胞活化与增殖,同时下调CXCL9等趋化因子,阻断T细胞迁移。
此外,MSC来源的细胞外囊泡(MSC-EVs)通过抑制MAPK/NF-κB通路中断B细胞活化级联反应,而MSCs本身则通过Fas/FasL通路诱导T细胞凋亡,并以IL-6/HGF依赖方式抑制单核细胞分化为树突状细胞。上述机制形成正反馈回路,放大IL-10的生成,最终恢复免疫稳态(图1A)。
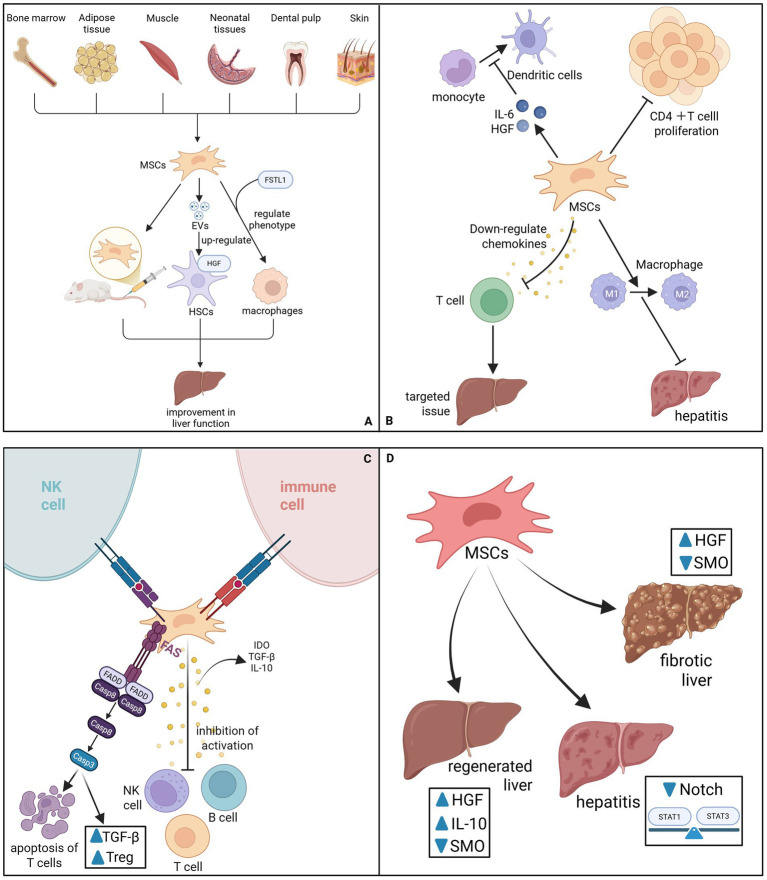
二、抗纤维化活性:直接靶向肝星状细胞(图1B)
作为纤维化发生的核心驱动因素,活化的肝星状细胞(HSC)是间充质干细胞(MSC)的主要治疗靶点。
MSCs通过直接干预纤维化级联反应,实现对活化肝星状细胞(HSCs)的抑制作用。MSCs及其细胞外囊泡可下调α-SMA、Col1α1及波形蛋白的表达,促使活化的HSCs恢复静止状态,这一作用通过旁分泌FSTL1、HGF等因子进一步增强。
与此同时,MSCs通过阻断Notch信号通路、恢复STAT1/STAT3稳态平衡,并下调Smo表达以抑制Hedgehog/SMO通路,从信号层面拮抗纤维化进程。在基质重塑方面,MSCs分泌MMP-1、MMP-9并下调TIMP,促进已形成的胶原沉积降解(图1B)。
三、促进血管生成与肝细胞再生(图1C)
为了促进功能恢复,间充质干细胞(MSCs)提供关键的营养支持,刺激内源性修复过程。它们释放大量生物活性介质,包括肝细胞生长因子(HGF)、血管内皮生长因子(VEGF)和细胞外囊泡(EVs),这些介质协同作用,刺激肝细胞增殖并促进新生血管形成。
在急性肝衰竭中,该旁分泌功能可迅速抑制炎症并阻止肝损伤进展;经基因工程过表达VEGF的MSCs可进一步增强上述疗效。此外,MSC-EVs通过富集lncEEF1G作为竞争性内源RNA,调控miR-181a-5p/HGF轴,增强HSCs中HGF的表达,从而间接促进肝细胞再生(图1C)。
四、新兴机制:铁死亡调控与线粒体转移(图1D)
近期研究进展揭示了间充质干细胞(MSCs)与肝细胞之间复杂的代谢和细胞器水平相互作用,为治疗提供了精准的新靶点。
一方面,MSCs经隧道纳米管将功能性线粒体转移至受损肝细胞,恢复GPX4活性与线粒体稳态,抑制脂质过氧化;另一方面,MSCs在铁死亡调控中呈现双重作用——脐带间充质干细胞来源的细胞外囊泡(UC-MSC-EVs)通过外泌体BECN1通路选择性诱导活化的HSCs发生铁死亡,降低xc⁻/GPX4系统活性,而健康肝细胞不受影响。这种“铁死亡-线粒体轴”既阻断HSCs活化,又避免全身性铁代谢紊乱,实现了肝细胞保护与纤维化靶向清除之间的平衡(图1D)。
03、间充质干细胞治疗肝病的临床试验
基于间充质干细胞(MSCs)的临床试验已覆盖多种主要肝脏疾病,包括肝硬化、病毒性肝炎、酒精性肝病、肝衰竭及肝移植并发症(表1)。

细胞来源与给药方案
目前进入临床试验的MSCs主要来源于骨髓、脐带与脂肪组织。其中脐带MSCs应用最为广泛,原因在于其取材无创、伦理争议小、细胞活性强、增殖能力高,且免疫原性低,异体使用时基本无需配型,便于实现标准化批量制备,成本与质量控制均优于骨髓来源。
给药方式以静脉输注为主,操作简便,但肝脏归巢效率有限。部分研究选择肝动脉或门静脉直接输注,实现细胞向肝脏的“定向投放”,理论疗效更优,但操作风险相应增加,需介入科配合。剂量范围跨度较大,从5×10⁵至5×10⁷个细胞/公斤不等,目前尚无统一标准,各中心仍处于经验积累阶段。
不同肝病的疗效数据
酒精性肝硬化:NCT03838250II期试验采用自体骨髓MSCs,结果显示Child-Pugh评分平均下降2至3分,血清白蛋白提升15%至20%。长期随访至75个月,生存率明显优于对照组,为终末期肝病提供了较为坚实的数据支持。
病毒性肝炎:该类试验中MSCs通常联合抗病毒药物使用,主要效果体现在炎症控制方面,IL-6、TNF-α等炎症因子水平显著下降,但病毒载量未受明显影响,提示MSCs发挥免疫调节而非抗病毒作用。
肝衰竭:NCT01322906试验采用异体骨髓MSCs,24周生存率为73.2%,显著高于标准治疗组的55.6%,差异近18个百分点。值得注意的是,该疗效在联合血浆置换基础上实现,提示MSCs在肝衰竭等急重症中更适合作为综合治疗策略的一部分。
终末期肝病:NCT01224327试验采用异体脐带MSCs经肝动脉输注,结果显示MELD评分明显下降,凝血功能改善,且疗效与自体MSCs相当。该发现表明,异体细胞在终末期患者中同样有效,并可规避自体细胞功能受损的问题。
纤维化逆转:NCT01741090试验从病理层面进行评估,肝硬化患者接受自体骨髓MSCs后,Laennec纤维化评分显著降低,提供了组织学上纤维化逆转的直接证据,终点指标较为坚实。
安全性数据
安全性是MSCs临床研究中较为一致的领域。超过90%的试验报告的不良反应主要为短暂性发热(发生率约5%至10%)及注射部位不适。严重不良事件少见,目前所有公开发表的临床试验中均未观察到致瘤性,这对细胞治疗领域而言是一项关键优势。
疗效差异的影响因素
不同试验间的疗效差异较为明显,主要原因包括:一是细胞来源不同,骨髓、脐带与脂肪来源的MSCs生物学特性存在差异,难以直接比较;二是患者状态不同,代偿期与失代偿期肝硬化对治疗的反应存在显著差异;三是剂量与给药方式缺乏标准化,静脉与肝动脉输注、单次与多次给药、剂量从数百万至数千万不等,均导致疗效难以横向对比。
自体与异体移植的选择
从现有临床实践看,选择倾向大致如下:代偿期肝硬化患者自体骨髓或脂肪来源MSCs功能通常正常,自体移植可规避免疫排斥风险,无需配型与供体问题,为首选方案。
失代偿期肝硬化或肝衰竭患者自身处于严重炎症状态,自体MSCs功能常受损,异体MSCs更具优势。从病种来看,肝炎与肝硬化以自体移植为主,肝衰竭则以异体移植为主。
目前MSCs治疗肝病面临两大瓶颈:归巢效率低——静脉输注后多数细胞滞留于肺部,抵达肝脏者甚少;细胞异质性——同一批次中不同亚群疗效差异显著,质量控制难度较大。
04 当前瓶颈与临床转化新兴策略
促进临床转化的新兴策略包括:
第一,以工程化细胞外囊泡为核心的无细胞疗法精准化策略:间充质干细胞来源的细胞外囊泡(MSC-EVs)是间充质干细胞旁分泌效应的关键介质。它们通过携带包括miRNA和细胞因子在内的生物活性分子来调节肝脏免疫稳态。这一过程抑制IL-6和IL-1β等促炎因子,同时平衡Th17/Treg细胞比例,最终缓解慢性肝脏炎症和纤维化。
研究表明,静脉注射的MSC-EVs主要积聚在肝脏中,其小尺寸(<200nm)有利于穿透组织屏障。这一特性表明其在肝硬化和脂肪性肝炎模型中具有治疗潜力(图2A)。早期临床试验(ChiCTR2300075676)已初步证实其安全性。然而,仍需进行大规模疗效验证。
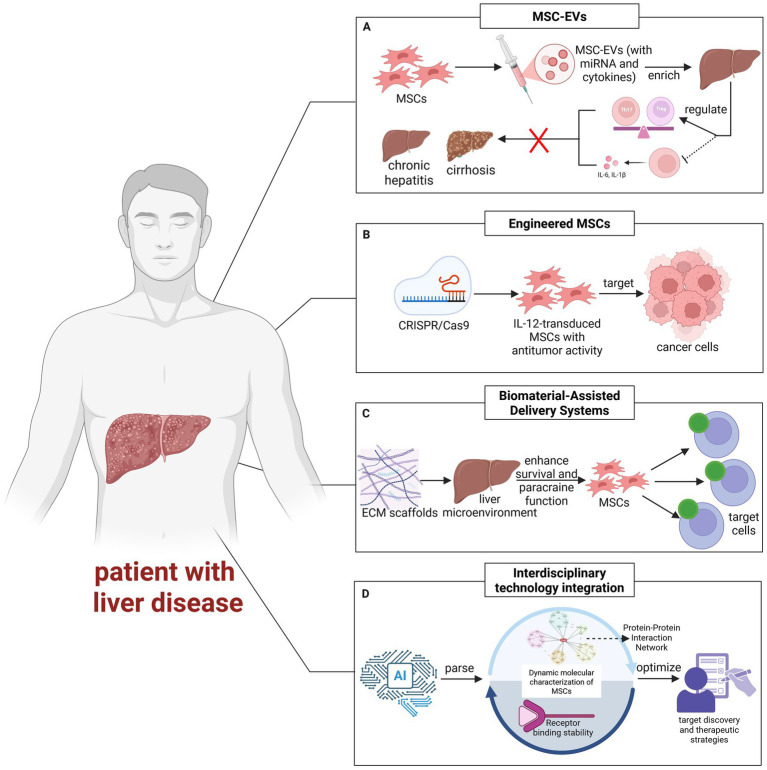
与天然分泌的间充质干细胞来源的细胞外囊泡(MSC-EVs)相比,后者本身就具有良好的生物分布和低免疫原性,而工程化细胞外囊泡则经过人为修饰,以提高其治疗的精准性和疗效。这些修饰包括用靶向配体(例如RGD或GE11肽)进行表面功能化,以改善组织特异性递送;或负载核酸(例如siRNA或lncRNA)以调控受体细胞的基因表达。这些策略性的改进凸显了工程化细胞外囊泡作为下一代无细胞疗法的巨大潜力,使其具有更强的靶向性和再生能力。
第二,结合基因编辑与生物材料工程的细胞功能强化与递送系统优化策略:利用CRISPR/Cas9等工具对MSCs进行预编辑(如敲除Smad7或导入IL-12),可从源头增强其免疫调节或抗肿瘤功能;诱导多能干细胞来源的MSCs则为标准化、规模化生产提供了可复制的细胞平台。与此同时,生物材料工程(如脱细胞ECM水凝胶、MSCs球体培养)通过模拟肝脏微环境,显著提升工程化MSCs及其分泌的SpEVs在体内的存活率、滞留时间与生物学功能。
这种“细胞内源工程化+外源微环境模拟”的组合有望通过协同效应放大治疗效果,但其长期安全性(如插入突变风险)及材料免疫原性的精细调控仍是临床转化前必须攻克的关键问题。
第三,依托跨学科技术整合与标准化体系的全链条创新策略:人工智能通过解析多组学数据与动态分子网络,正在解决MSCs异质性这一核心生产痛点,实现从培养参数优化(如缺氧预处理时间)到高效批次筛选的智能化质控。纳米技术与机械灌注等前沿手段进一步拓展治疗场景:前者通过表面修饰提升EVs靶向性,后者联合EV脱细胞疗法直接应用于移植器官修复。
然而,上述技术的临床落地高度依赖建立从EV分离鉴定到CRISPR递送的全流程GMP标准化体系,并通过多学科验证机制确保跨技术整合(如AI+纳米材料、机械灌注+细胞疗法)的疗效稳定性与安全性,最终为实现基于患者疾病分型的个性化联合治疗奠定基础。
05 结论与研究展望
核心结论
本研究明确,间充质干细胞治疗肝病最核心且证据最为充分的机制与疗效在于:其作用主要依赖旁分泌因子介导的免疫调节与基质重塑,而非直接分化。
具体而言:
- 抑制肝星状细胞活化并诱导其凋亡
- 将巨噬细胞由促炎M1型极化为抗炎M2型
- 调控胶原降解相关酶系
上述机制在多种动物模型及I/II期临床试验中持续降低纤维化指标并改善肝功能合成指标,是MSC发挥肝脏修复作用最可重复且临床证据最坚实的核心机制。
未来三大转化方向
| 方向 | 具体策略 | 目标 |
|---|---|---|
| 优化细胞来源 | 推进iPSC-MSCs;探索肝脏驻留MSCs | 解决供体短缺,提高肝脏相容性 |
| 提高靶向特异性 | CRISPR介导归巢受体过表达;EV表面修饰;生物材料支架 | 实现精准递送与局部滞留 |
| 评估长期安全性 | 大规模、多中心、长期随访(≥5年)临床试验 | 系统评估致瘤性与慢性免疫风险 |
研究强调,只有系统性地填补上述知识空白并推进相关方向,基于MSC的疗法才能最终成为安全、可及的终末期肝病常规治疗手段。
06 常见问题解答(FAQ)
参考资料:
[1]:Huang Y, Cheng R, Wang G, Xu Z, Liu S, Wan Y, Hou X, Wang J. Harnessing mesenchymal stromal cells for liver disease therapy: from mechanistic discoveries to clinical breakthroughs. Front Med (Lausanne). 2026 Feb 4;12:1677021. doi: 10.3389/fmed.2025.1677021. PMID: 41717346; PMCID: PMC12913439.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信