银屑病是一种由免疫介导、慢性、复发性、炎症性、全身性疾病,由个体与环境相互作用而诱发,且由于治疗难度较大,往往伴随终身疾病。近年来,包括生物制剂在内的多种靶向治疗手段虽然改善了大多数银屑病患者的皮损和生活质量,但仍未能解决复发问题,且可能随着时间的推移导致疗效下降或出现感染等不良事件。因此,银屑病治疗亟需突破,延缓复发及非药物治疗策略,而干细胞治疗银屑病应运而生。近年来,干细胞治疗银屑病的研究备受关注,但目前尚无可参考的标准和共识。
湘雅领衔发表国际首部指导干细胞在银屑病治疗领域中的共识
近日,由中南大学湘雅医院皮肤科牵头的“Expert consensus on the application of stem cells in psoriasis research and clinical trials (干细胞在银屑病研究领域和临床试验的专家共识)”在国际杂志《Aging and disease》在线发表。

该共识为国际首部指导干细胞在银屑病治疗领域中的共识。
中南大学湘雅医院陈翔教授、中国医学科学院基础医学研究所赵春华教授担任通讯作者,中南大学湘雅医院匡叶红教授为第一作者、与张谧主治医师为共同执笔人。
该共识明确了银屑病治疗常用的干细胞类型、干细胞治疗银屑病的方法、剂量和途径,以及干细胞治疗银屑病的临床评价。此外,此共识还规范了干细胞及其相关产品的采集、制备、保存和质量控制过程,为银屑病干细胞治疗领域提供了最新的具体参考标准和实践指南。
1、对干细胞研究机构开展研究治疗疾病试验的要求有什么?
干细胞研究通用规则
干细胞可源自胚胎或成体组织,具备自我更新和分化潜能,可分为自体或异体类型,并支持体外分离传代及新鲜/冻存储存。
干细胞研究规范:临床前与临床研究执行准则
临床前研究:需制定严谨方案,确保记录完整可追溯。细胞质量须符合临床应用标准(优质且纯净),生产流程须遵守GMP规范。须开展基因组稳定性、致瘤性、异常分化等生物学分析,动物实验遵循”减少、优化、替代”三原则。有效性研究需模拟临床条件、设置充分对照、随机盲法设计,并建立量效关系;安全性研究需监测细胞体内分布、异常分化及长期毒副作用。
临床研究:须以充分科学依据为基础,权衡受试者与公众的健康收益与风险(收益须大于潜在危害),保障受试者权益。根据ISSCR指南,所有干细胞干预临床应用须经独立伦理委员会前瞻性审查批准。研究方案需经独立专家评估(涵盖临床前数据、统计方法及受试者保护),结束后需长期随访监测治疗安全性与有效性。
干细胞制剂制备机构管理规范:设施、质控与人员体系要求
硬件设施:须配备万级(局部百级)洁净度的GMP车间,布局符合药品GMP标准,每台仪器配备标准操作规程(SOP)。
质量管理:建立符合GMP的完整质量管理体系,设立独立质管部门承担质量保证(QA)与质量控制(QC)职能,并基于产品特性与工艺进行风险评估。
人员与设备:指定专人负责制备管理、质量管理及质量监督;建立人员设备档案,提供专业培训(含安全防护、应急预案及继续教育);定期校准维护设备以保障生产质量。
2、治疗银屑病常用的干细胞类型有哪些?
2.1、脂肪间充质干细胞
ADMSCs于1973年首次在脂肪组织中发现,2001年由Zuk正式命名。其可通过高效的胶原酶消化法从脂肪组织中分离,产量高且操作简便。ADMSCs具有多向分化潜能及组织修复功能。
2016年,De Jesus团队报道2例银屑病患者接受自体ADMSCs输注后,PASI评分显著下降(分别从21.6降至8.9、24降至8.3),症状缓解最长持续292天,但其中1例关节炎症状未改善。
2023年,Amir团队对5名患者进行皮损内注射,6个月观察期所有患者皮损轻至显著改善,且无严重不良反应,证实ADMSCs治疗安全性。
2.2、脐带间充质干细胞
UCMSCs源自脐带华通胶及血管周围组织,21世纪初被报道。其分离主要采用组织块贴壁法或酶消化法,具有增殖力强、免疫原性低、来源伦理风险小(取自医疗废弃物)等优势。
临床证据表明:2022年,中南大学基础医学院生殖与干细胞工程研究所进行了一项为期1/2a的单臂临床试验,17名银屑病患者接受了UCMSC输注。治疗后,47.1%的患者的PASI评分改善至少40%,17.6%的患者的医生整体评估(PGA)评分(医生用来评估患者病情总体严重程度的指标)提示皮损已消退或基本消退;治疗期间及随后的6个月随访中均未见明显副作用。
Chen等[10]报道,使用UCMSC治疗2名寻常型银屑病患者后,皮损消失,且四五年内无复发。
2.3、真皮来源的间充质干细胞
DDMSCs是存在于真皮层的主要间充质干细胞,体外呈成纤维细胞样形态增殖,可通过组织块法或酶消化法分离,具有来源丰富、增殖力强的特性。
Campanati研究发现:将健康供体的DDMSCs(H-MSCs)与银屑病患者的DDMSCs(PsO-MSCs)共培养,可显著改善PsO-MSCs的炎症表型,表明DDMSCs在调节银屑病病理过程中具有重要治疗潜力。
| 作者 | 来源 | 地点 | 年 |
|---|---|---|---|
| 萨赫 | 脐带 | 韩国 | 2016 |
| 六户 | 胖的 | 日本 | 2016 |
| 李 | 脐带 | 韩国 | 2017 |
| 金 | 扁桃体 | 韩国 | 2018 |
| 坎帕纳蒂 | 真皮 | 意大利 | 2018 |
| 陈 | 脐带 | 中国 | 2019 |
| 今井 | 羊膜 | 日本 | 2019 |
| 金 | 胚胎 | 韩国 | 2019 |
| 孟 | 纸浆 | 中国 | 2021 |
| 张 | 胚胎 | 新加坡 | 2021 |
| 陈 | 脐带 | 中国 | 2022 |
| 叶 | 牙龈 | 中国 | 2022 |
| 张 | 脐带 | 中国 | 2022 |
| 张 | 脐带 | 中国 | 2022 |
| 魯 | 脐带 | 中国 | 2022 |
| 丁 | 脐带 | 中国 | 2022 |
| 任 | 脐带 | 中国 | 2023 |
| 温 | 纸浆 | 中国 | 2023 |
| 卡里略 | 脐带 | 智利 | 2023 |
| 王 | 脐带 | 中国 | 2023 |
2.4、牙龈间充质干细胞(GMSCs)
GMSCs提取自牙龈固有层组织,具有抑制炎症和免疫调节功能,长期培养仍能保持形态稳定和端粒酶活性。其伦理风险低、获取便捷、分化潜能突出,被视为优质间充质干细胞来源。Ye等通过咪喹莫特诱导的银屑病小鼠模型证实,GMSCs输注可通过降低Th1/Th17相关细胞因子显著缓解皮肤炎症。
Wang团队报道1例19岁重度斑块状银屑病患者(既往多种治疗失败),经5次异体GMSCs注射后皮损完全消退,随访3年无复发且无不良反应。
2.5、牙髓间充质干细胞(DPSCs)
DPSCs存在于人牙髓组织中,具备强增殖力、多向分化能力和免疫调节特性。Wen等研究发现,在银屑病模型小鼠皮下注射DPSCs可有效减轻皮损症状,并显著抑制表皮异常增殖标志物(角蛋白16、S100A8/A9)的表达,证实其治疗银屑病的临床潜力。
2.6、羊膜间充质干细胞(AMSCs)
AMSCs源自胎盘羊膜层,属高分化潜能的围产期干细胞。分离时需先释放羊膜上皮细胞,再经胶原酶消化获取。其特点包括:
- 形态为短梭形贴壁细胞,可稳定传代至30代
- 获取率高、增殖速度快,供体年龄不影响细胞活性
- 异体应用免疫原性低,排斥风险小
- 适合大规模标准化生产
Imai等动物实验表明AMSCs能抑制银屑病皮炎进展并减轻角质细胞炎症反应,但尚缺临床研究证据。
2.7、扁桃体间充质干细胞(TDMSCs)
TDMSCs从人扁桃体组织中分离(常来源于扁桃体切除手术废弃物),具有标准MSCs的增殖与分化能力。Kim团队通过银屑病小鼠模型证实其有效抑制皮炎炎症,但因缺乏临床研究,现阶段主要价值在于原料易得性及治疗潜力探索。
2.8、骨髓造血干细胞
生物学特性与临床应用:骨髓造血干细胞(BMHSCs)具备强大的自我更新与多向分化能力,可生成各类免疫细胞祖细胞,是外周免疫细胞的主要来源。通过免疫磁珠法或流式细胞术可从骨髓中分离BMHSCs。其移植分为自体与异体两类,其中异体移植因复发率显著低于自体移植,已成为银屑病(尤其合并血液疾病患者)的重要治疗手段。
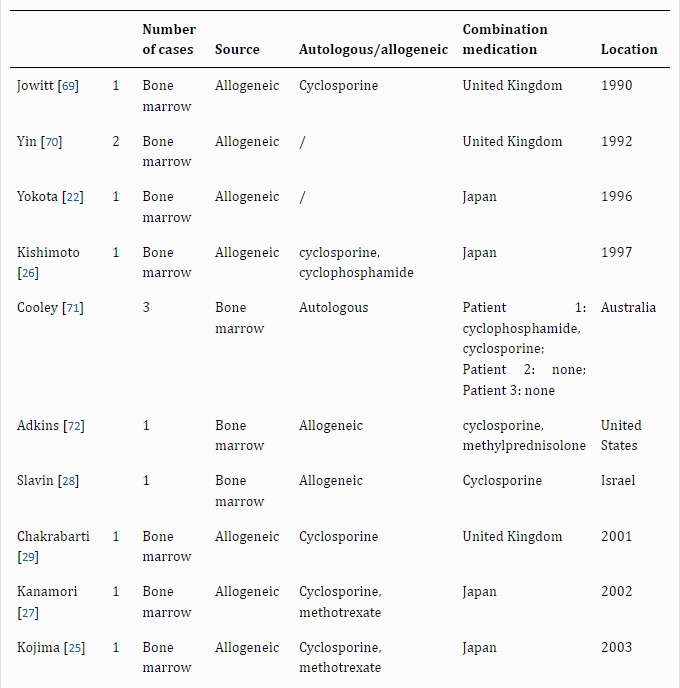
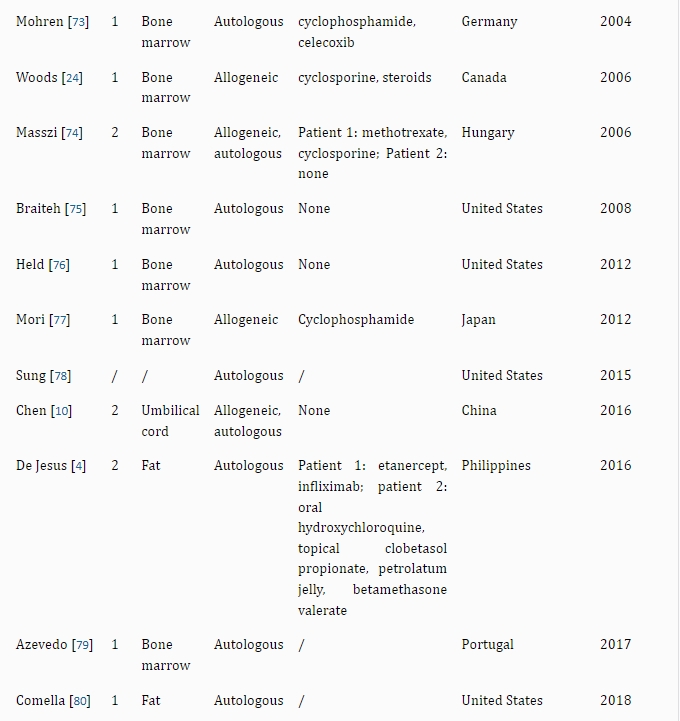
临床证据与疗效:多项病例研究证实异体BMHSC移植对银屑病合并血液疾病具有双重疗效。横田、居莱尔等学者报道的案例显示,合并再生障碍性贫血的银屑病患者移植后皮损完全消退且贫血缓解;小岛、岸本等研究则证明其对急性髓系白血病合并银屑病患者同样有效(移植后皮损消退且白血病无复发)。此外,针对慢性髓系白血病、淋巴瘤(NHL)及脓疱型银屑病的案例也观察到银屑病与血液病的同步长期缓解,最长随访达2年无复发。
研究现状与局限:BMHSCs是目前治疗银屑病历史最久、病例积累最多的干细胞类型,其疗效数据支持度优于其他干细胞(如脐带间充质干细胞仅17例研究)。然而,不同干细胞疗法之间尚无直接对比研究,限制了对最优治疗策略的评估(见表2)。现有证据凸显了BMHSCs在难治性银屑病(尤其合并血液疾病)中的临床潜力,但需进一步对照研究明确其比较优势。

3. 干细胞治疗牛皮癣的科学基础
疾病机制与干细胞异常:银屑病的核心发病机制涉及免疫系统失调,包括树突状细胞异常激活Th1/Th17通路、促炎-抗炎因子失衡及角质形成细胞过度增殖形成的炎症循环。关键证据表明,患者皮损处的间充质干细胞呈现功能异常:促血管生成能力增强,而免疫抑制与抗氧化能力减弱,且分泌谱向促炎状态偏移,提示异常干细胞可能通过多重机制参与疾病进展。
干细胞疗法的多元作用机制:不同来源干细胞通过特异性途径干预银屑病进程。研究最深入的脐带间充质干细胞(UCMSCs)可显著降低IFN-γ、TNF-α等核心炎性因子,减少致病性Th1/Th17细胞,并通过抑制中性粒细胞浸润及调节MMP13通路抑制角质增生。脂肪、骨髓等其他来源干细胞同样能下调炎症因子并抑制角质细胞增殖(如通过上调TGF-β),而真皮与牙髓干细胞则分别依赖PD-L1通路调控Th17反应或通过调节T细胞亚群平衡(如降低Th17/Treg比值)发挥作用。
治疗潜力的共性基础:尽管干细胞来源各异,其治疗银屑病的科学基础均指向三大核心机制:抑制异常免疫细胞(如T细胞亚群)的增殖分化、阻断关键促炎因子表达级联、直接干预角质形成细胞病理性增殖。这些共性作用机制为干细胞疗法奠定了坚实的理论基础,凸显其在重塑银屑病免疫微环境中的广阔前景。
4. 干细胞及相关产品制备的机构要求
机构干细胞产品制备涉及生物医药、伦理、法律法规等多个领域,核心要求如下。
4.1 道德与合规
研究人员应当对干细胞研究进行伦理审查,确保符合《涉及人类的生物医学研究伦理审查办法》,干细胞的来源和获取过程应符合伦理道德。
4.2 质量管理
- 干细胞的制备需要建立质量控制和保证体系,包括细胞表征、无菌技术和环境监测。
- 制剂生产应遵循GMP及相关规定,建立完整的质量管理体系。
- 机构必须进行风险评估,合理设计工作区域,确保各职能区域独立且满足要求。
- 控制微生物、微粒及热原污染风险。
- 管理、质量控制人员必须具备相关专业知识和经验,且不得兼职。所有相关人员均须接受专业培训。
- 人员应及时报告可能的污染并采取措施避免污染。
- 必须保证设备、仪器的可追溯性,并按照使用说明书的要求进行管理。
- 如果使用电子信息系统,机构应建立并验证相关的管理程序。
4.3 知识产权
在考虑干细胞领域的创新和发明时,应关注知识产权,例如专利保护。
5. 干细胞采集、制备、储存和质量控制
标准化采集与分类检测:干细胞采集需在GMP规范下建立严格的操作与管理流程。自体干细胞(未经复杂体外操作)需进行基础检测,包括细胞活力、增殖能力、外源性病原微生物及基本特性鉴定;而异体干细胞(经复杂体外操作)还需增加内源性病原微生物筛查、特性深度分析及细胞纯度检测,确保源头安全性与功能性。
精细化制备与微环境适应:干细胞制备涵盖分离、纯化、扩增、定向分化等全链条环节,每个步骤均需制定独立SOP并定期更新。针对移植后病理微环境(如缺氧、炎症因子)的挑战,研究强调通过”预处理”提升干细胞适应性:例如用TNF-α预激活可增强MSCs在氧化应激下的增殖与存活能力,利用疾病相关刺激物优化干细胞功能已成为提升疗效的关键策略。
差异化冻存保障细胞活性:稳定储存是临床应用的核心前提。基于不同类型干细胞的低温生物学特性差异(如抗冻损伤能力),需定制最优冻存方案。低温冻存技术不仅保障运输与长期储存可行性,更通过个性化冻存方法维持细胞解冻后的活性与功能,为治疗有效性提供底层支撑。
双轨质控与全周期稳定性管理:质量控制分为质量检验(全面评估安全性、有效性及质量)和放行检验(批制备后快速检测)。前者覆盖细胞特性、无菌性、致瘤性等21项检测;后者依据前者定制简化标准。此外,需在临床前/临床阶段持续进行稳定性研究(包括储存期、运输后状态),通过评估活力、纯度等参数确定保存液配方、运输条件及有效期,构建全生命周期质控体系。
6. 干细胞治疗银屑病的方法、剂量和途径
目前,国内外现有的用于治疗银屑病的干细胞疗法主要有BMHSC静脉输注、ADMSC静脉输注或皮下注射、UCMSC静脉输注、GMSC静脉输注(图1)。
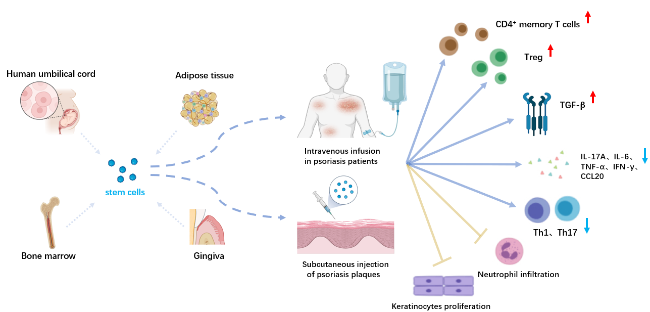
干细胞治疗银屑病的剂量和途径
BMHSCs的个体化给药特点:骨髓造血干细胞(BMHSCs)目前缺乏统一治疗方案,临床多用于银屑病合并血液病患者。主要采用静脉输注,剂量跨度大(CD34+细胞0.5×10⁶至2.5×10⁷细胞/kg),或单次输注总量高达4×10⁸细胞/kg。关键操作包括输注前使用抗组胺药物预防过敏反应,凸显其方案的高度个体化特征。
ADMSCs的双途径精准干预:脂肪源性间充质干细胞(ADMSCs)具备静脉与皮下注射双途径方案:静脉输注推荐0.5~3×10⁶细胞/kg(每4周1次,共2~3次);皮下注射则根据皮损面积精准给药(单点1×10⁶细胞或3×10⁶细胞/cm²),实现局部病灶的靶向治疗。
UCMSCs与GMSCs的差异化方案:脐带间充质干细胞(UCMSCs)静脉输注方案最复杂,含三种剂量-周期组合(如1.5~2×10⁶细胞/kg每2周1次,或2.5~3×10⁶细胞/kg每4周1次),部分需分阶段追加输注。牙龈间充质干细胞(GMSCs)因临床数据稀缺,暂定剂量为3×10⁶细胞/kg(每周2次),5周后可启动第二疗程。
输注规范与标准化挑战:所有静脉输注均需遵循严格操作流程:混匀细胞悬液、使用输血过滤器、控制初始滴速(20-30滴/分钟)及生理盐水冲管。当前不同干细胞因来源与给药途径差异导致疗效参差,尚无标准化方案。未来需深入探索最佳剂量、疗程及给药策略,以提升治疗可重复性与安全性。
7. 干细胞输注治疗牛皮癣的管理:调理、监测和不良反应的处理
预处理:治疗当天,应将干细胞解冻并准备注射。每批干细胞在移植前都应经过放行检验。注射前应将干细胞悬浮于5mL生理盐水中[14]。局部注射时,干细胞以3×106细胞/mL的密度重悬于0.9%生理盐水中。静脉输注时,干细胞以1×106细胞/mL的密度重悬于0.9%生理盐水中[43]。
目前,尚无关于干细胞预处理治疗银屑病的临床研究。在现有的干细胞治疗银屑病的临床试验中,为防止不良反应的发生,通常在输注前肌肉注射抗组胺药,如苯海拉明。对于使用干细胞治疗银屑病,需要进一步研究预处理方案,所采用的各种方法和组合需要进一步优化。
监控:输液过程中应密切监测患者呼吸、脉搏、血压、血氧饱和度的变化,做好急救措施。少数患者可能出现一过性胸闷、发热等不适症状,一般可自行缓解。如症状持续或严重,应停止治疗,监测生命体征、完成心电图等检查,并采取吸氧等必要的急救措施。
不良反应处理:综合Stem Cell Reports发表的治疗其他疾病的研究及治疗银屑病的临床研究资料和病例报告,临床应用中未观察到严重不良事件。
报道的安全性事件主要为低热、胸闷、头晕、轻微腹痛、心电图异常、咽炎等[ 9,45],一般在24小时内消退。个别患者可出现高热,可给予物理降温及对症药物治疗。另外,不排除发生输液反应、过敏性休克的可能,一旦出现应积极对症治疗。
8. 干细胞治疗牛皮癣的临床评价(疗效及安全性)
临床研究中,常采用PASI评分评估治疗前后皮损严重程度。PASI评分是对皮损面积、红斑、鳞屑及厚度程度的综合评估。主要评估部位为头部、躯干、上肢和下肢。PASI 75表示治疗后PASI评分与基线相比改善75%,PASI 90、PASI 100等分别表示改善90%、100%等。
综合目前已发表的关于干细胞治疗银屑病领域的临床研究和病例报告,治疗可分为治疗期、缓解期和复发期三个时间窗。
治疗期间,有2项临床研究以PASI评分改善率作为主要评价指标,1份病例报告评估了治疗期间PASI评分绝对值的变化。在评估皮损改善的同时,可以从医患双方的角度同时评估治疗后PGA、皮肤病生活质量指数(DLQI)和瘙痒数值评定量表(INRS)评分的变化趋势。
在缓解期,银屑病患者的皮损逐渐消退,多项研究报道,银屑病患者经干细胞治疗后皮损完全消退,即PASI100反应率。此外,有3项研究证实干细胞治疗后银屑病皮损基本消退,即达到PASI 90缓解率或PGA 0/1评分。
虽然既往研究证实了干细胞治疗的有效性,但也有不少研究注意到了干细胞治疗后的复发问题,观察时间窗为2至5年不等。对于复发的定义,目前公认的标准为PASI评分改善≤基线PASI评分的50%,复发时间为停止治疗至PASI改善率降低50%的时间。
因此,评价干细胞治疗银屑病的疗效时,建议治疗期间以PASI改善率或PASI绝对值评分作为主要评价指标,缓解期以PASI 75/90/100作为主要评价指标。对于长期观察的患者,应关注复发情况及中位复发时间。鉴于银屑病是一种全身性疾病,建议使用银屑病关节炎疾病活动评分 (PASDAS) 和整体患者评估等工具来评估患者的整体状况。
9.干细胞衍生物应用研究
干细胞衍生物是干细胞释放或分泌到细胞外基质中的活性成分,包括干细胞培养基(CM)和细胞外囊泡(EVs)。干细胞培养基含有干细胞分泌的蛋白质、microRNA、生长因子、抗氧化剂等活性物质。干细胞EVs包括外泌体、微泡、凋亡小体等。现有与银屑病治疗相关的EVs研究主要以外泌体为主。
Seetharaman[54]等将ADMSC衍生条件培养基(ADMSC-CM)局部应用于银屑病皮损,每天一次,持续一个月,治疗了一名38岁的寻常型银屑病患者。患者的PASI评分从28分降至0分,生活质量改善,且无不良反应。
虽然干细胞衍生物尚未广泛应用于临床研究,但与干细胞相比,干细胞衍生物具有以下特点:
- (1)更易于储存和运输;
- (2)作为非细胞生物疗法,伦理问题较少;
- (3)非自我复制,避免了致癌风险;
- (4)免疫原性和致敏性较低,比干细胞更安全。
这些特点提示干细胞衍生物在银屑病治疗方面具有巨大的潜力。
10. 结论与展望
干细胞作为人体中具有多种分化潜能和免疫调节功能的细胞,多年来一直被研究作为银屑病治疗的选择,其潜在机制也不断被研究,有望成为银屑病治疗的新方法。
不同类型的干细胞已被发现通过调节银屑病皮损中免疫细胞的浸润和炎症因子的水平来纠正不平衡的免疫反应,改善银屑病的临床症状。干细胞衍生物,如干细胞分泌的生长因子和外泌体,是一种非细胞治疗方法,具有获取方便、性质稳定、易于保存、伦理问题较少等应用优势,因此有在临床上推广的潜力。此外,干细胞与药物、中药、小分子化合物相结合的方法也在研究之中。例如,有研究表明,中药成分槲皮素在治疗类风湿关节炎中可以促进UCMSCs的抗炎作用。
因此,可以优化各种方法的组合,以最大程度地发挥干细胞治疗银屑病的治疗效果。值得注意的是,在干细胞技术的商业化过程中,与专利权和知识产权相关的复杂挑战需要特别注意。尽管干细胞研发带来了创新的治疗方法,但在保护专利、确保技术转让的公平性和遵守道德标准之间找到平衡是研究机构和商业实体必须解决的关键问题。
总之,作为治疗银屑病的新兴方法,干细胞及其衍生物具有巨大的未来应用潜力。
参考资料:Ye-Hong Kuang , Wu Zhu , Ge Lin , La-Mei Cheng , Qun Qin , Zhi-Jun Huang , Yu-Ling Shi , Chun-Lei Zhang , Jin-Hua Xu , Ke-Xiang Yan , Cheng-Zhi Lv , Wei Li , Qin Han , Ilia Stambler , Lee Wei Lim , Sasanka Chakrabarti , Brun Ulfhake , Kyung-Jin Min , Georgina Ellison-Hughes , William C Cho , Kunlin Jin , Danni Yao , Chuanjian Lu , Robert Chunhua Zhao , Xiang Chen. Expert Consensus on the Application of Stem Cells in Psoriasis Research and Clinical Trials. Aging and disease. 2024 https://doi.org/10.14336/AD.2024.0012
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信