Meta描述:跃赛生物UX-GIP001获中美双批临床试验,成为全球首款iPSC来源治疗难治性癫痫的通用型细胞疗法。动物实验显示癫痫波消失率达90%。解读技术原理、临床前数据与监管意义。
全球首款!跃赛生物iPSC来源癫痫细胞疗法UX-GIP001获中美双批临床试验
核心速览
| 项目 | 关键信息 |
|---|---|
| 产品名称 | UX-GIP001注射液 |
| 研发企业 | 上海跃赛生物科技有限公司(UniXell Biotechnology) |
| 细胞类型 | iPSC来源的GABA能神经祖细胞 |
| 适应症 | 药物难治性癫痫(尤其是内侧颞叶癫痫MTLE) |
| FDA批准 | 2026年3月12日 |
| CDE批准 | 2026年4月8日 |
| 全球地位 | 首款同时在中美获批临床的iPSC来源癫痫细胞疗法 |
| 技术原理 | 移植后分化为GABA能中间神经元,修复兴奋-抑制失衡 |
| 临床前数据 | 动物实验中,约90%癫痫相关脑活动消失,8个月后癫痫波几乎检测不到 |
| 研发阶段 | I期临床试验即将启动 |
| 上市预期 | 5-8年(若I-III期顺利) |
一、全球7000万患者的希望:难治性癫痫的新解法
全球约有7000万癫痫患者,其中大约30%——也就是超过2000万人——对现有的抗癫痫药物没有反应。这种情况被称为药物难治性癫痫。
在成人中,最常见的局灶性癫痫类型是内侧颞叶癫痫(MTLE),约占70%。它的典型病理特征是海马硬化——海马区的神经元大量丢失,胶质细胞增生,导致脑内兴奋-抑制严重失衡。简单说就是“油门太猛,刹车太软”。
现有治疗手段都有各自的短板:
- 药物:对30%的患者无效,而且长期服用有认知障碍、骨质疏松等副作用
- 手术:切除癫痫灶,但创伤大,可能损伤记忆功能
- 神经刺激:效果有限,需要植入设备
所以,科学家一直在寻找一种能从根源上修复神经网络的方法——不是“控制发作”,而是“修复大脑”。
二、里程碑事件:全球首款中美双批的iPSC癫痫细胞疗法
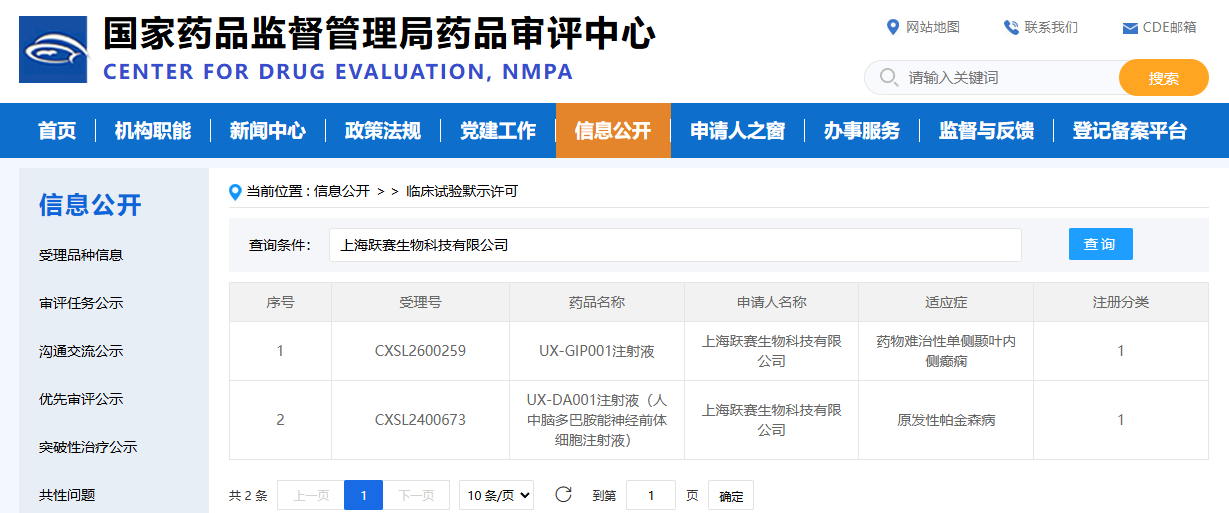
2026年4月8日,上海跃赛生物科技有限公司宣布,其自主研发的UX-GIP001注射液获得中国国家药监局药品审评中心(CDE)临床试验默示许可。
就在不到一个月前(3月12日),该药已经获得美国FDA的临床试验批准。
至此,UX-GIP001成为全球首款同时在中美两国获批进入临床试验的iPSC来源、用于治疗药物难治性癫痫的通用型细胞疗法。
这标志着中国在干细胞治疗难治性癫痫领域,已经从“跟跑”进入了“领跑”行列。
三、技术原理:用“刹车细胞”修复失衡的大脑
UX-GIP001的核心技术是:用人类诱导多能干细胞(iPSC)定向分化制备GABA能神经祖细胞。
GABA(γ-氨基丁酸)是大脑中最重要的抑制性神经递质——它就像汽车的刹车。癫痫的本质,就是大脑的“油门”(兴奋性神经元)太强,“刹车”(GABA能中间神经元)太弱。
跃赛生物的做法是:
- 在体外用iPSC大规模生产GABA能神经祖细胞
- 把这些细胞移植到患者的海马区
- 细胞在体内成熟为功能性GABA能中间神经元
- 它们与宿主神经元建立突触连接,修复失衡的兴奋-抑制网络
- 从而抑制癫痫异常放电,同时保留海马的正常功能
最关键的一点:这不是“控制症状”,而是“修复神经回路”——属于疾病修复性疗法(Disease-modifying therapy),有可能从根源上治疗MTLE。
而且,该产品采用异体通用型设计,不需要从患者自身取材,可以实现规模化生产,降低成本。
四、临床前数据:90%癫痫波消失
动物实验的数据相当亮眼:
- 干细胞植入小鼠约6个月后,约90% 的癫痫相关脑活动消失
- 8个月后,癫痫波几乎检测不到
这些数据表明,移植的GABA能神经祖细胞不仅存活了,还成功整合进了宿主神经网络,并且长期发挥抑制作用。
临床前研究已经充分验证了安全性和有效性,这也是中美两国药监机构敢于批准进入人体试验的基础。
五、研发进度:接下来会发生什么?
5.1 I期临床试验(即将启动)
I期试验的主要目标是评估安全性、耐受性和初步疗效。将在中美两国同步或分别开展。入组患者通常是药物难治性癫痫患者,对现有治疗反应不佳。
5.2 后续时间线
如果I期结果积极,后续需要推进II期(扩大样本,评估疗效)和III期(多中心,随机双盲对照)试验。
从I期到上市,通常需要5-8年。当然,如果数据特别突出,可能会获得突破性疗法认定或优先审评,加速上市。
六、研发主体:跃赛生物是谁?
跃赛生物由中国科学院脑科学与智能技术卓越创新中心高级研究员陈跃军博士于2021年创立,总部位于上海张江。
2025年2月,公司完成了1.4亿元人民币(约2050万美元)的A+轮融资,投资方包括高瓴创投、天士力、浦东创投等知名机构。
公司在上海自贸试验区设有4000平方米的研发中心及GMP级生产设施。
值得注意的是,跃赛生物还有另一款iPSC衍生细胞疗法(用于治疗帕金森病),已于2025年启动I期临床。这说明其iPSC分化技术平台具有强大的拓展性——可以针对不同疾病生产不同类型的神经细胞。
七、监管意义:为什么“中美双批”很重要?
同时获得FDA和NMPA的临床试验批准,意味着什么?
第一,科学性和创新性得到全球最严格审评体系的认可。 美国FDA和中国CDE对细胞治疗产品的审评标准都非常严格,能同时通过,说明产品的临床前数据扎实、生产工艺可控、安全性风险可控。
第二,中国CDE通过“创新药30日审批通道”快速获批,体现了国家对具有临床价值的创新疗法的优先支持。
第三,中美双批可以实现全球同步临床研发,加速上市进程,也为中国创新药“出海”提供了成功范例。

八、展望与挑战
UX-GIP001为全球数千万难治性癫痫患者带来了从“控制发作”到“修复大脑”的曙光。
但我们也必须清醒地看到,细胞疗法仍然面临一些挑战:
- 长期安全性:致瘤风险(iPSC来源细胞的残留未分化细胞)、免疫排斥(异体细胞)
- 手术移植风险:细胞需要直接注射到海马区,属于侵入性操作
- 可及性和定价:细胞药物的生产成本高,未来上市后的价格和医保覆盖是实际问题
尽管如此,这一里程碑事件的意义不可否认——它标志着中国在干细胞治疗领域,已经从“跟跑”进入了“领跑”行列。
九、常见问题解答(FAQ)
参考资料
- 跃赛生物官方公告(2026年4月8日)
- 中国国家药监局药品审评中心(CDE)公开信息
- FDA临床试验批准信息(2026年3月12日)
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信