核心速览:间充质干细胞(MSCs)治疗脑卒中等神经系统疾病,核心机制之一是促进血管新生——为缺血区建立新的血流通道。本文基于2026年《Stem Cells and Development》综述,系统解析MSCs促血管生成的三大机制(旁分泌主导、分化辅助、细胞接触调控),以及增强其疗效的四种策略:药物预处理(简单短效)、基因修饰(强效高风险)、低氧/3D培养(温和安全)、生物材料支架(解决存活难题)。临床证据显示,MSCs移植可改善脑卒中患者运动功能,外泌体作为无细胞疗法正成为新方向。
干细胞如何促进血管新生并治疗神经系统疾病?四大方法让“血管搭桥”更高效
一、为什么MSCs能治脑中风?血管新生是关键
脑中风(缺血性脑卒中)后,大脑某区域的血管被堵死,下游神经元因缺血缺氧而死亡。现有的溶栓和取栓手术能开通大血管,但已经梗死的脑组织和缺血半暗带里的濒死神经元,需要新的微血管来提供营养、清除坏死组织。
间充质干细胞(MSCs)正好能促进血管新生——这是它治疗神经系统疾病的核心机制之一,甚至比它直接变成神经元更重要。
华中科技大学同济医学院附属同济医院神经外科团队近期在《Stem Cells and Development》上发表了一篇综述,系统梳理了MSCs促血管生成的机制,以及如何通过四种修饰策略让MSCs“更强、更准、更安全”。这篇文章不仅总结了临床证据,还指出了从“细胞疗法”向“无细胞疗法”过渡的趋势[1]。
二、直接移植MSCs:临床证据有了,但还不够
2.1 脑卒中患者的临床试验
MSCs移植在脑卒中患者中已经有不少临床试验。
2021年,Chung团队做了一项针对慢性重度脑卒中患者的研究。他们给患者注射了自体MSCs,3个月后整体残疾评分(改良Rankin量表)没有显著改善——听起来有点失望。但仔细分析功能细节发现,患者的腿部运动功能有明显提升。这说明MSCs可能不是“全脑修复”,而是对特定功能区域有效。
2020年,Jaillard团队针对亚急性脑卒中患者(发病后几周内)做了另一项试验。他们静脉输注了自体骨髓来源的MSCs,结果证实安全可行,而且患者的运动功能恢复与感觉运动神经可塑性有关。也就是说,MSCs帮助大脑重新组织了神经网络。
2.2 直接移植的三大隐患
尽管有效,但直接往血管里打活的MSCs有三个让人担心的问题:
- 免疫原性:异体MSCs虽然低免疫原性,但不是零。反复输注可能引发排斥。
- 致瘤风险:任何活细胞在体内长期存在,理论上都有变成肿瘤的可能,虽然MSCs概率极低。
- 堵塞血管:MSCs直径约15-30微米,静脉输注后大部分被肺部截留,少数能到达脑部。但如果细胞团块形成,可能堵塞梗死区已经脆弱的微血管。
这就是为什么研究者开始寻找“无细胞”的替代方案。
三、外泌体:MSCs的“无细胞使者”
3.1 外泌体是什么?
外泌体是细胞分泌的一种纳米级小囊泡,直径只有50-150纳米,里面装着蛋白质、mRNA、miRNA等生物活性分子。它们就像细胞之间的“快递包裹”,MSCs通过外泌体把指令传递给其他细胞。
3.2 临床证据:外泌体数量与疗效相关
Bang等人的临床试验发现了一个有趣的现象:患者接受自体MSCs注射后24小时内,血液中的外泌体水平升高了大约5倍。而且,外泌体的数量与患者运动功能的改善程度独立相关。与此同时,脑内MSCs分泌的神经营养因子水平并没有升高。
这说明什么?MSCs的神经修复作用,很可能主要是通过外泌体介导的,而不是靠MSCs自己跑到脑子里干活。
动物实验也证实了这一点:给缺血性脑卒中小鼠注射MSCs外泌体,这些外泌体能够迁移到损伤脑区,显著促进血管新生和神经发生。
3.3 外泌体的优势
与直接移植MSCs相比,外泌体疗法有几个明显好处:
- 无免疫排斥:外泌体没有细胞膜表面的MHC分子,不会引起排斥。
- 无致瘤风险:不是活细胞,不会分裂增殖。
- 无栓塞风险:尺寸小,不会堵塞血管。
- 易于保存:可以冻干,不需要液氮。
所以,外泌体正在成为再生医学领域的一个热门方向。
四、MSCs促血管新生的三大机制
目前,MSCs主要用于治疗神经系统疾病中的脑缺血性疾病(图1)。其对急性缺血性卒中的治疗机制可概括为抑制急性局部炎症、促进长期神经功能恢复和血管重塑,其中血管重塑对患者的功能恢复至关重要。新的功能性血管结构能为梗死灶提供更多营养支持,促进局部坏死组织清除,并减轻缺血半暗带区内神经元的缺氧状态和代谢紊乱。
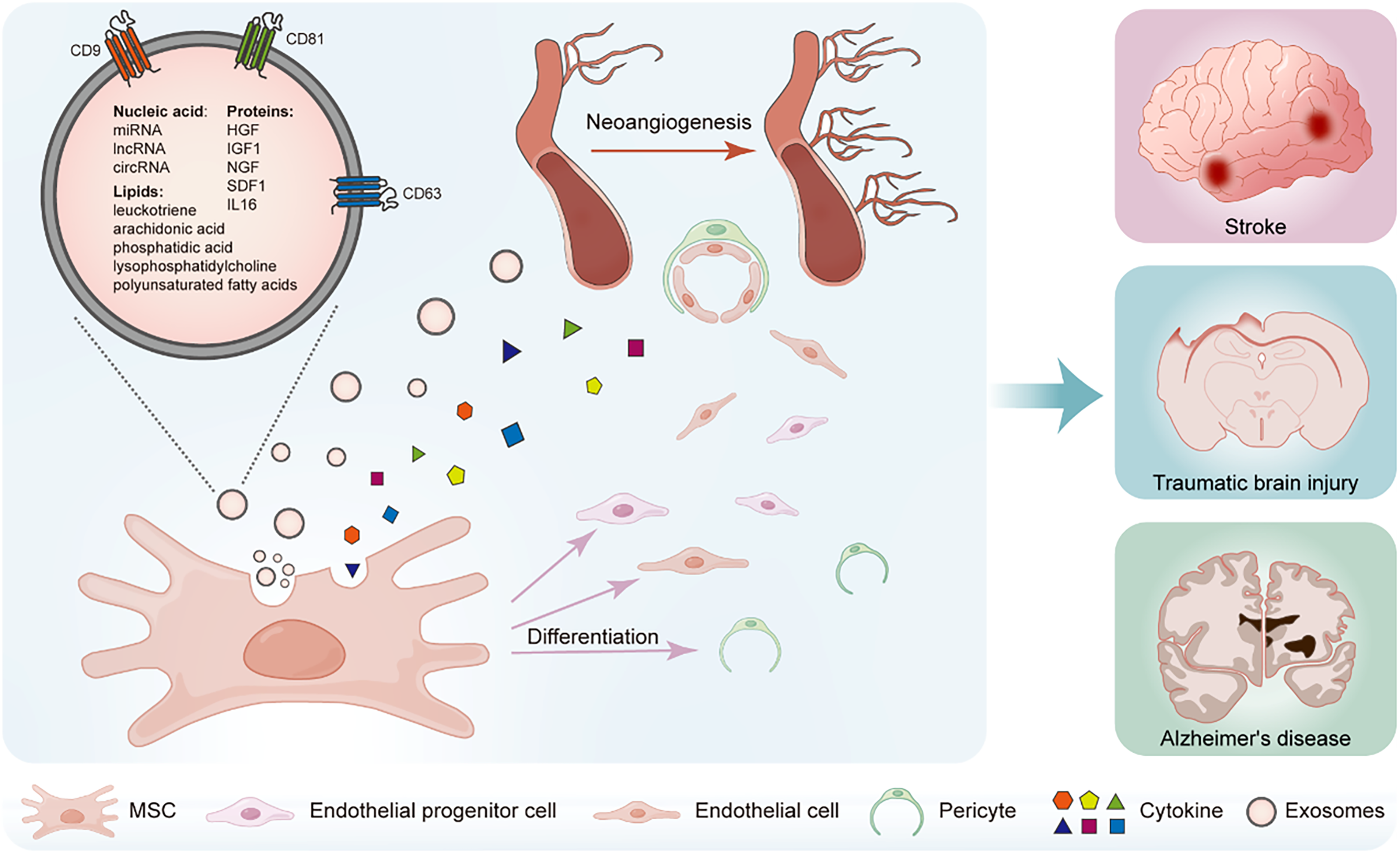
围绕这一关键环节,MSCs的促血管生成机制可归纳为三个层面,其中旁分泌占据主导地位,分化与直接接触分别作为辅助和新兴补充。
3.1 第一,旁分泌作用——主导机制。
MSCs能够分泌大量生物活性分子(包括VEGF、FGF、TGF-β等可溶性蛋白以及携带核酸和蛋白质的外泌体),这些旁分泌因子被释放到局部微环境中,通过以下顺序促进血管新生:首先诱导内皮细胞迁移和增殖,随后促进管腔形成,最后募集周细胞、沉积基底膜以稳定新生血管。
实验证据表明,仅使用MSCs的条件培养基(含旁分泌产物)即可在脑缺血模型中显著减少梗死体积并改善神经功能,证实旁分泌效应足以产生治疗效果,且无需MSCs直接存在。
3.1 第二,直接分化为内皮细胞——体外明确但体内证据不足。
在特定诱导剂(如VEGF、辛伐他汀)或机械刺激下,MSCs在体外可表达内皮细胞标志物并形成管状结构。然而,目前缺乏MSCs在体内稳定、可控地转分化为功能性内皮细胞的临床证据,因此这一机制对实际血管生成的贡献尚不明确,不是主要作用途径。
3.2 第三,直接细胞-细胞相互作用——新发现的辅助机制。
近期3D微血管芯片模型观察到,MSCs会选择性地定位于血管生成芽的隆起或根部,并通过直接接触参与毛细血管的激活与稳定。这一机制超越了传统的旁分泌和分化范畴,提示MSCs可能通过物理接触实时调控血管生成过程,但其在体内的普遍性和重要性仍需进一步验证。
综上,MSCs促血管生成并非单一路径,而是以旁分泌为始动与主导,以分化为潜在补充(实际贡献有限),以细胞间接触为精细调控节点。正是旁分泌的主导地位,催生了“无细胞疗法”(直接使用外泌体或条件培养基),以规避直接移植MSCs的免疫原性与致瘤风险;但无细胞疗法也丧失了持续分泌和细胞接触调控的优势,故并非完全替代方案。
表1列出了利用MSC的促血管生成特性进行疾病治疗的其他研究。
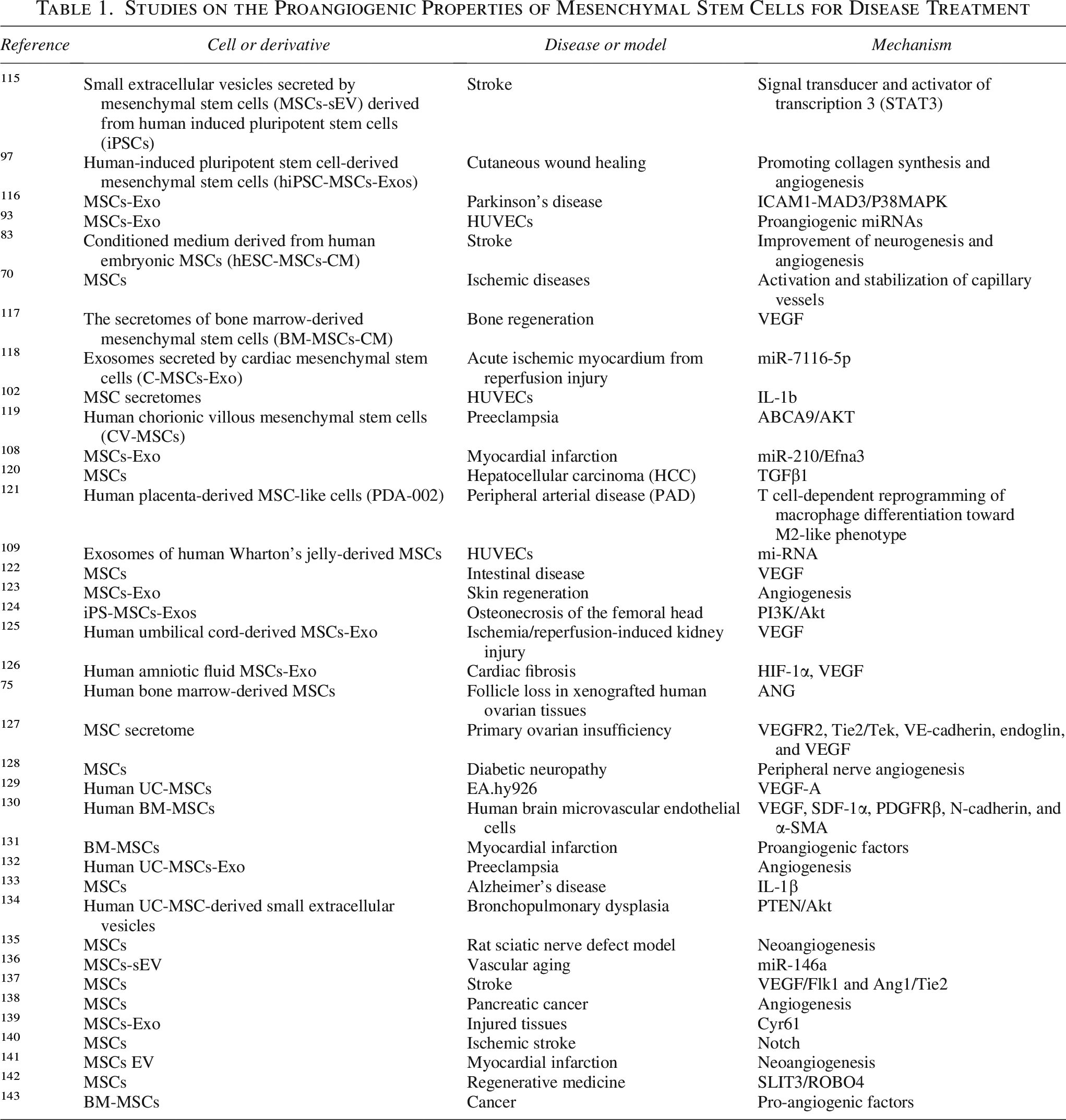
五、修饰提高间充质干细胞的疗效的方法
过去20年间,MSCs已成为临床试验中最常用的细胞治疗剂之一。ClinicalTrials.gov数据显示,截至2025年11月28日,以“间充质干细胞”注册的研究已达1405项。
然而,全球获批上市的MSCs疗法数量屈指可数。野生型MSCs固有的诸多缺陷,严重制约了其临床应用的范围与效果。为此,研究者正从多个维度对MSCs进行工程化改造,以提升其治疗潜能。当前主流修饰策略包括药物预处理、基因修饰、培养环境调控及联合生物材料,各具逻辑,亦各有困境(图2)。
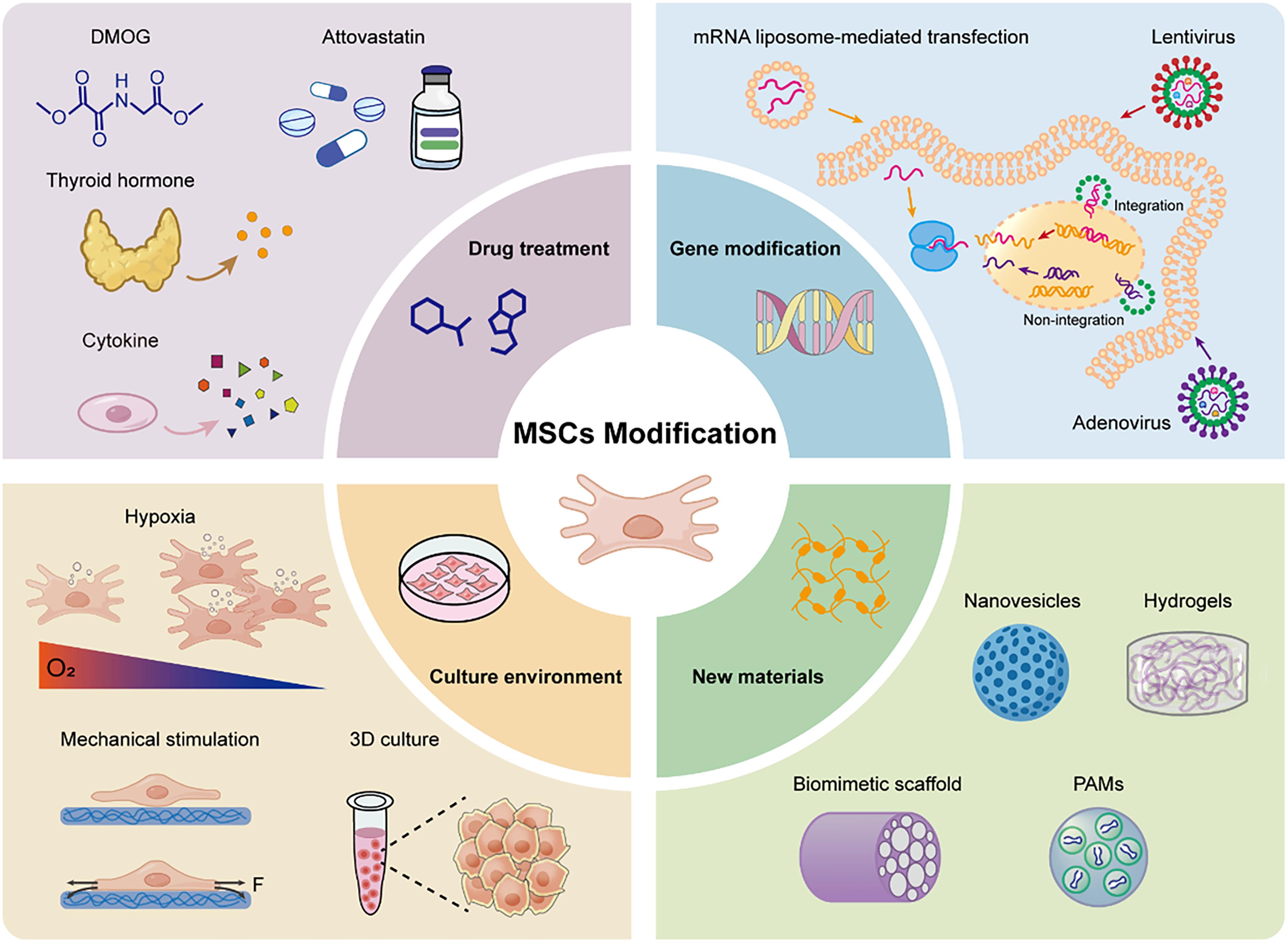
5.1、药物预处理:短效激活,简便易行。
间充质干细胞(MSC)对外部刺激敏感,易于接收外部信号并调节自身的生物学行为。用不同的药物刺激MSC可以显著改变其功能。研究发现,许多药物可以增强MSC的血管生成功能,包括各种生长因子、细胞因子、激素和市售药物(表2)。
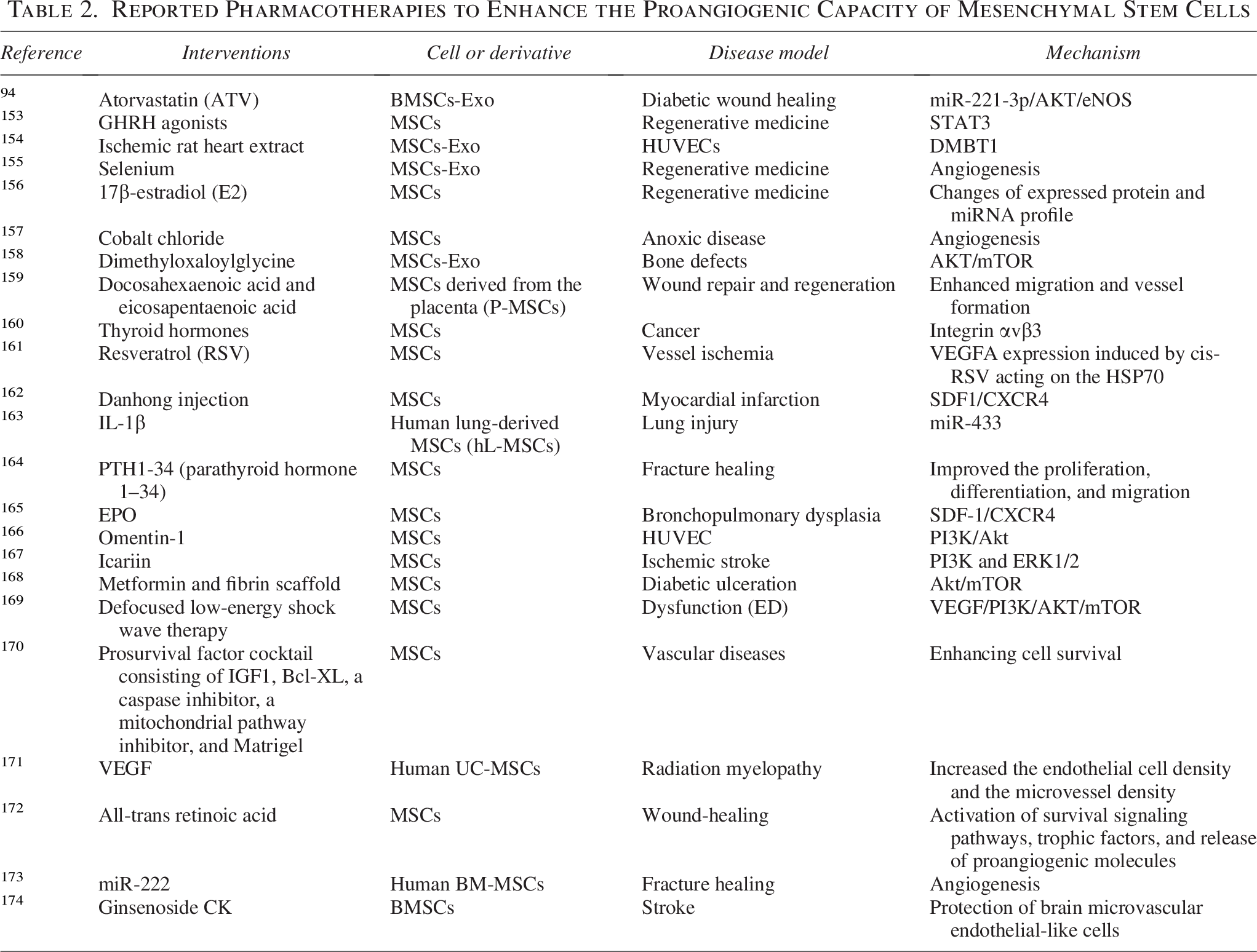
该方法最为直接——将MSCs在体外与特定药物共孵育一段时间,实现“预激活”。例如,DMOG刺激可增强MSCs外泌体的促血管生成能力;促红细胞生成素则通过激活SDF-1/CXCR4轴间接促进血管新生。该策略操作简单、成本低廉,不依赖复杂基因操作设备,多数实验室均可开展。
但其短板同样突出:药效短暂。药物一旦代谢清除,细胞迅速恢复原态,移植后长期疗效难以保证。本质上,这更像一剂“短效兴奋剂”,而非“底层改造”。
5.2、基因修饰:底层编辑,效果最强但风险最高。
基因修饰是最常用的修饰方法,通常使用逆转录病毒、慢病毒或腺相关病毒对间充质干细胞(MSCs)进行基因编辑。研究者可将HIF-1α、VEGF、miR-126等功能基因整合至MSCs基因组,使其持续高表达目标蛋白。并增强其分泌治疗性细胞因子、归巢或存活的能力(表3)。
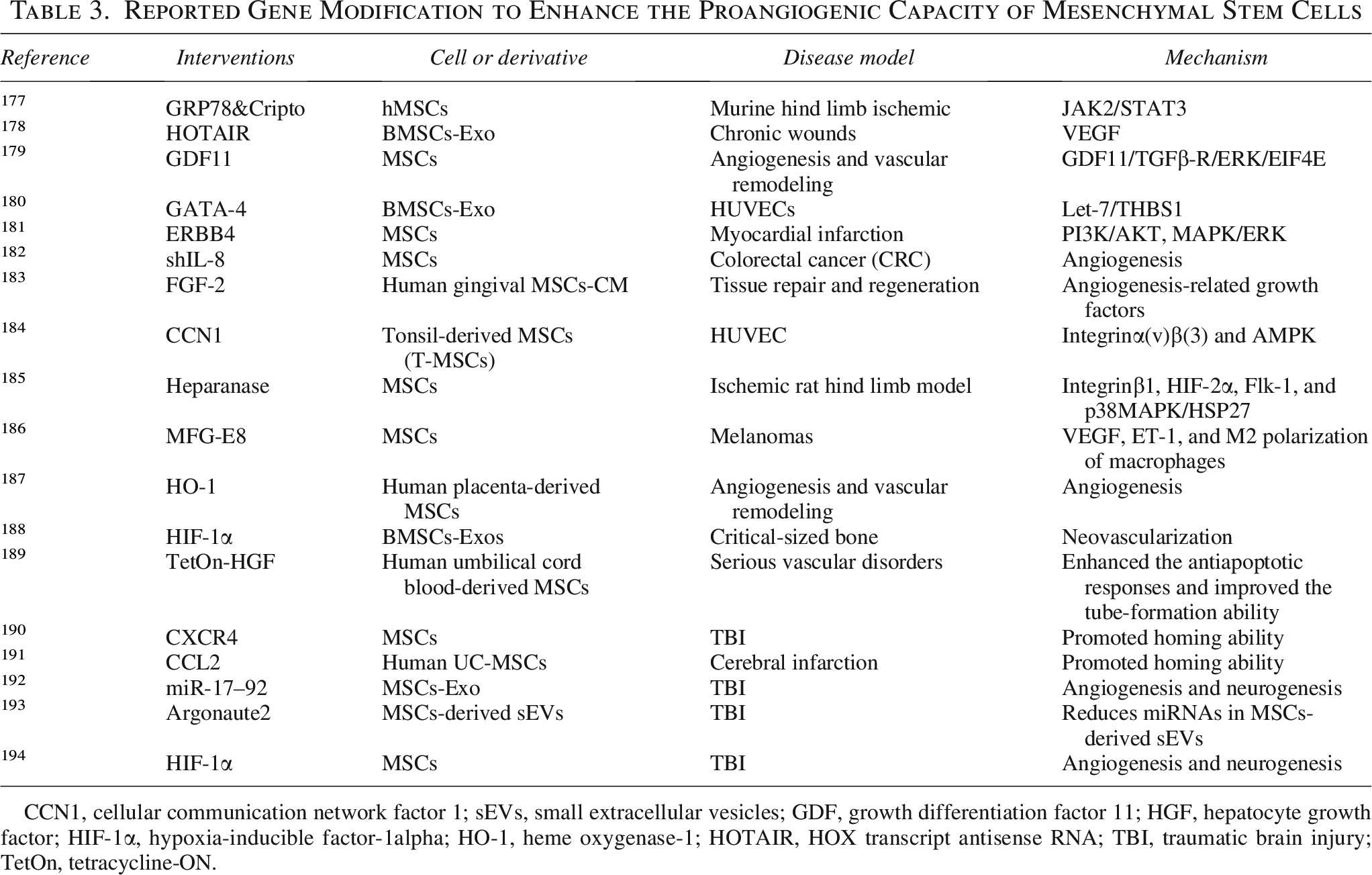
效果显著:过表达HIF-1α的MSCs外泌体在心肌梗死模型中能显著保护心脏功能;上调CXCR4则增强MSCs向脑损伤区域的归巢能力。
然而,“永久性改动”伴随隐忧——脱靶突变、插入位点不可控、潜在致瘤风险,令临床转化格外谨慎。一个折中策略正在兴起:不再移植基因编辑后的MSCs本身,而是仅取用其分泌的外泌体,以保留增强功能的同时规避活细胞移植的安全风险。
5.3、培养环境调控:贴近生理,温和有效。
培养环境对间充质干细胞(MSCs)的功能有显著影响。在常规实验室环境下,MSCs通常在21%的氧浓度下培养,但这显然无法模拟MSCs在人体内的实际生存环境,因为MSCs在体内生存的氧浓度约为5%。因此,大量研究探讨了不同培养环境对MSCs功能的影响(表4)。

将MSCs置于低氧(甚至1%氧)条件下培养,其分泌的外泌体促血管生成能力显著提升。同样,传统的二维贴壁培养与体内的三维生存环境相去甚远。采用三维培养(如球状体或支架培养)后,MSCs分泌抗炎因子和生长因子的能力明显增强,其外泌体促内皮细胞增殖、迁移的效果优于二维培养。
此外,循环拉伸应变、模拟脑脊液脉动等机械力干预,也被证实可上调VEGFA表达。该方法不涉及基因层面改动,相对安全,且更贴近生理状态,在转化研究中受到日益广泛的关注。
5.4、联合生物材料:解决存活与靶向难题。
MSCs移植后存活率低是长期痛点——细胞注入体内后,大部分在短期内凋亡或流失。将MSCs负载于水凝胶、藻酸盐支架或层粘连蛋白微载体上再行移植,可显著提高细胞的驻留与存活。更重要的是,这些材料可设计为缓释平台,例如预加载VEGF等信号分子,在体内形成趋化梯度,引导宿主自身修复细胞向损伤区迁移(表5)。
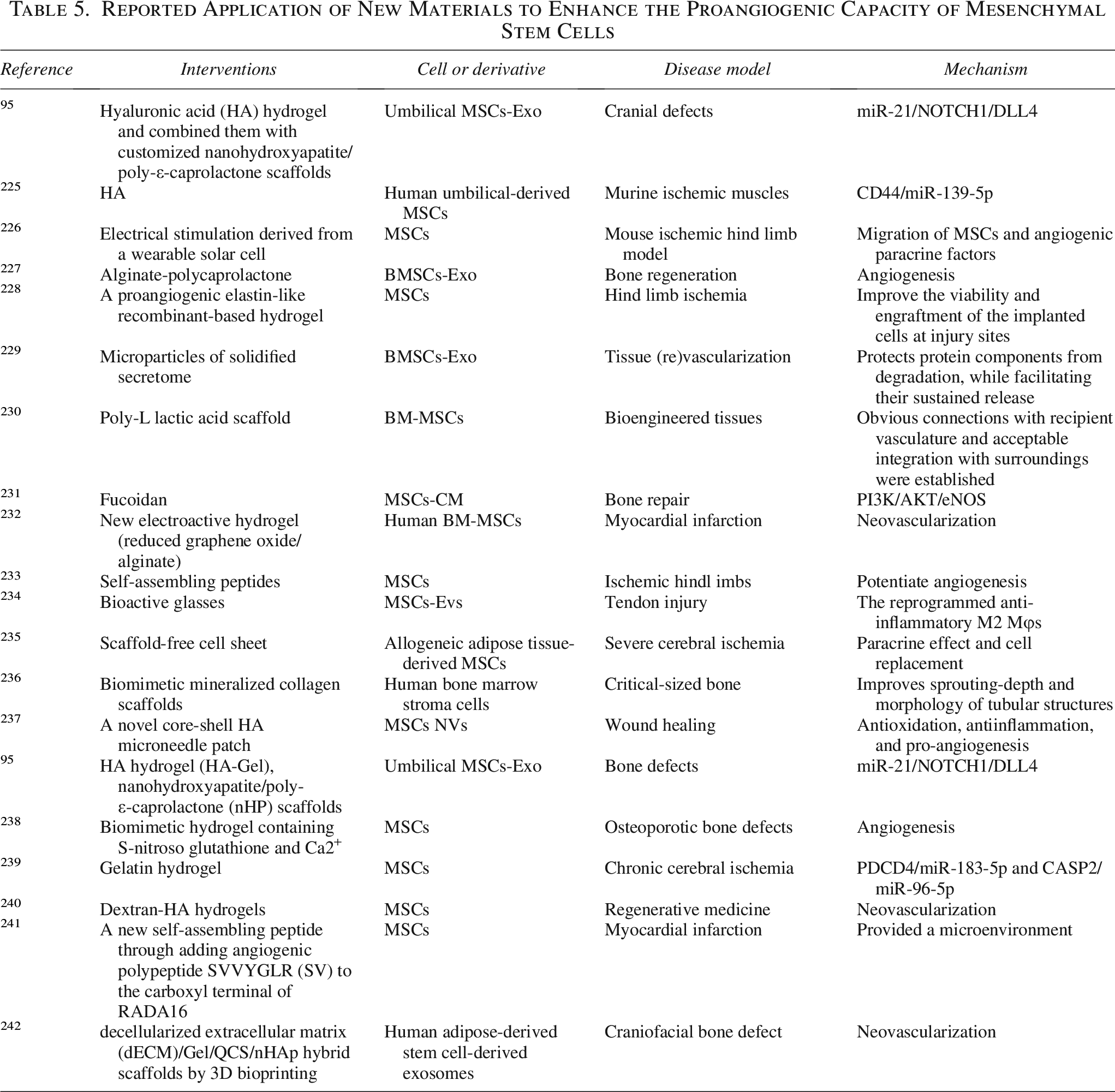
近年还涌现出更精巧的设计:给外泌体加上磁性纳米颗粒,在外部磁场引导下使缺血区域的富集度提高数倍;或利用可穿戴太阳能电池产生的电刺激,引导MSCs定向迁移。这些技术的共同思路是:不再将MSCs视为孤立的“药丸”,而是将其嵌入一个可控的递送系统。
四大策略并非互斥。实际研究中常组合使用——例如先对MSCs进行基因修饰,再在低氧环境下培养,最后装载于水凝胶中联合移植。选择何种策略或组合,取决于具体疾病模型、安全考量以及对“疗效”与“可控性”的权衡。药物预处理胜在简单快捷,基因修饰效果最强但风险最高,环境优化温和而有效,生物材料则聚焦于解决移植后的存活与靶向问题。尚无一种方法能兼顾所有需求——这正是该领域持续活跃的根本动力。
六、四大策略对比:怎么选?
| 策略 | 原理 | 优点 | 缺点 | 适合场景 |
|---|---|---|---|---|
| 药物预处理 | 短时激活细胞信号 | 简单、便宜、易操作 | 药效短暂 | 快速增强,实验室常用 |
| 基因修饰 | 永久性改变基因表达 | 效果最强、持久 | 脱靶、致瘤风险 | 基础研究,外泌体来源改造 |
| 培养环境调控 | 模拟生理条件 | 安全、温和 | 需要专门设备 | 临床转化潜力大 |
| 生物材料 | 提高存活和靶向 | 解决移植后流失 | 材料生物相容性需验证 | 联合移植,局部给药 |
实际研究中常组合使用——比如先对MSCs进行基因修饰,再在低氧环境下培养,最后装载于水凝胶中联合移植。没有一种方法能兼顾所有需求,这正是该领域持续活跃的动力。
七、总结与展望
MSCs促血管新生的核心机制是旁分泌,而不是分化成内皮细胞。它分泌的VEGF、FGF、HGF以及富含miRNA的外泌体,共同构成了促血管新生的分子网络。
四种修饰策略——药物预处理、基因修饰、培养环境调控、生物材料——各有优劣,殊途同归:让MSCs从“天生我才”走向“更强、更准、更安全”。
未来有几个方向值得关注:
- 外泌体作为标准化产品:无细胞疗法将规避活细胞的安全风险,更容易通过监管审批。
- 组合修饰:低氧培养+基因修饰+水凝胶递送,多管齐下。
- 精准递送:磁性导航、超声控释、电刺激引导,让细胞和外泌体精准到达缺血区。
对于缺血性脑卒中等神经系统疾病,MSCs及其外泌体有望开辟一条新的“血管搭桥”之路——不是开颅搭桥,而是用细胞和纳米囊泡在微观层面重建血流通道。
八、常见问题解答(FAQ)
参考资料:
[1]:Zhang X, Kang H, Liu Y, et al. Proangiogenic Mechanisms and Modifications of Mesenchymal Stem Cells with a Focus on Neurological Disorders. Stem Cells and Development. 2026;35(3-4):47-66. doi:10.1177/15473287251413995
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信