阿尔茨海默病(AD)存在巨大的未满足医疗需求,目前尚无有效的治疗方案。现有的药物治疗仅能缓解症状,无法阻止持续的神经退行性变。间充质干细胞(MSCs)疗法因其治疗AD的潜力而受到广泛研究,但其疗效仍未得到证实。
干细胞治疗阿尔茨海默病,到底有没有效?一项基于17项临床研究的综述给出了答案
为了证实间充质干细胞治疗阿尔茨海默病的临床可行性,近日,《组织工程与再生医学》杂志发表了一篇“间充质干细胞(MSCs)治疗阿尔茨海默病疗效:临床结果综述”的论文。该研究旨在通过回顾17项临床试验和4篇相关论文来评估MSCs对AD患者的治疗效果[1]。

最终对17项临床试验和5项相关临床结果的初步分析表明,间充质干细胞治疗阿尔茨海默病患者中总体可行且安全,部分患者的认知功能或生活质量显示出改善迹象,提示其具有潜在的治疗价值。然而,确切的疗效仍需进一步验证。
这些临床探索建立在MSCs多靶点治疗潜力的理论基础之上。与单靶点药物不同,MSCs被认为能通过多种协同机制干预AD的复杂病理过程,这构成了其临床研究的主要依据:
间充质干细胞治疗阿尔茨海默病的潜在机制
间充质干细胞有望通过多模式作用机制干预AD的复杂病理过程,这与多数单靶点药物形成鲜明对比,也是其临床研究的理论基础。主要机制包括:
- 神经营养支持:MSCs分泌脑源性神经营养因子(BDNF)、胶质细胞系衍生神经营养因子(GDNF)等多种因子,促进神经元存活并刺激内源性神经发生。
- 抗炎与免疫调节:MSCs能将中枢神经系统内的小胶质细胞和星形胶质细胞从促炎表型(M1/A1)转化为神经保护表型(M2/A2),从而减轻慢性神经炎症。
- 促进Aβ清除:MSCs可增强小胶质细胞对Aβ斑块的吞噬作用,并分泌或诱导脑啡肽酶等降解酶,帮助减少脑内Aβ负荷。
- 抗凋亡与抗氧化:通过旁分泌信号调节细胞存活通路,抑制神经元凋亡,并分泌抗氧化物质以减轻氧化应激损伤。
- 促进血管新生与修复:分泌VEGF、FGF-2等血管生成因子,有助于改善脑血流灌注和血管功能,针对AD中常见的血管功能障碍。
研究目的与方法
尽管临床前研究显示了MSCs治疗AD的潜力,但由于临床试验数量有限且多处于早期阶段,其在患者中的实际获益仍不明确。本综述旨在从循证医学角度,系统评估MSCs治疗AD的当前临床疗效并展望其前景。
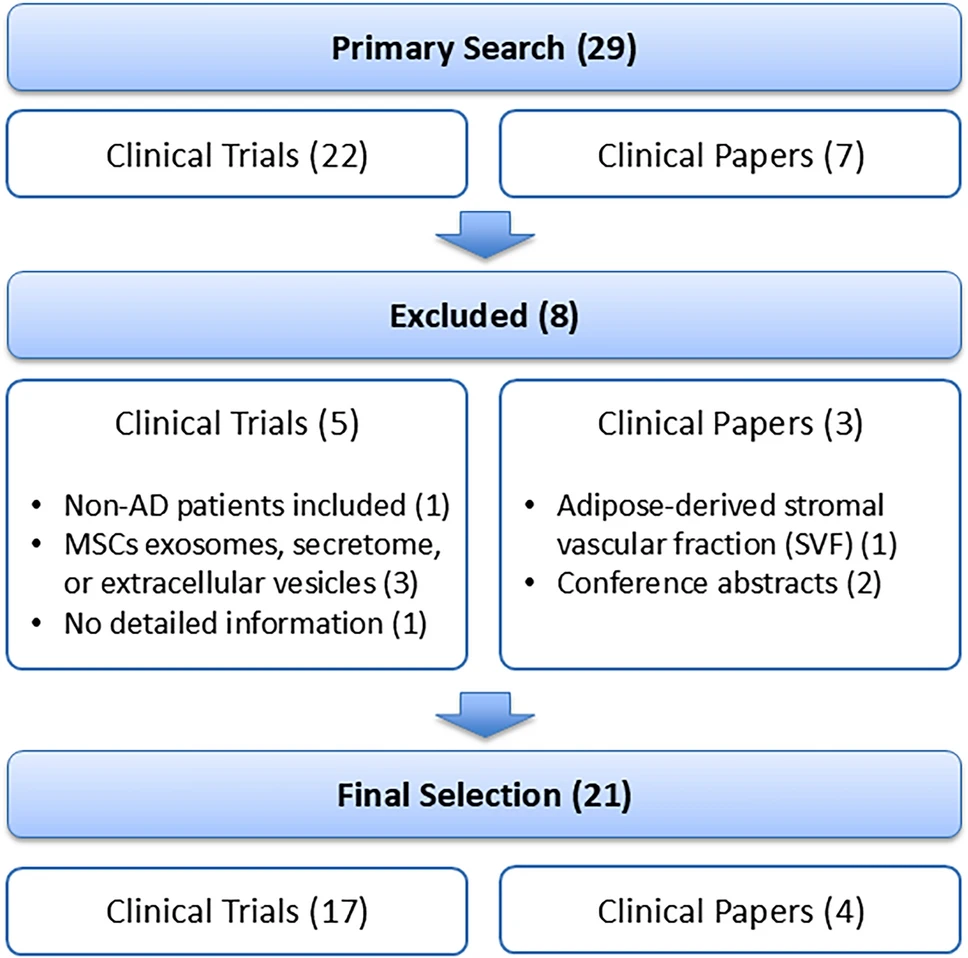
我们系统检索了2011年1月至2025年6月期间,收录于ClinicalTrials.gov、PubMed、Web of Science和SCOPUS数据库的文献与注册试验,关键词包括“阿尔茨海默病”、“间充质干细胞”和“临床试验”。经筛选,最终纳入17项临床试验及4篇相关论文进行深度分析(图1)。
基于现有数据的间充质干细胞治疗阿尔茨海默病的临床试验深度分析
试验时间线与地理分布明细:在明确提及年份的17项试验中,研究活动呈持续但低量的分布。具体而言,2011年有1项,2025年计划有2项,其余年份(介于其间)每年约有0至3项试验启动或进行,表明这是一个长期但未形成爆发式增长的研究领域。从地理分布看,美国主导了超过一半(9项,52.9%) 的研究,韩国贡献了超过三分之一(6项,35.3%),中国进行了2项(11.8%)。与此相关的4篇临床论文发表于2015年(2篇)、2021年和2023年,印证了该领域超过十年的持续关注度(图2)。
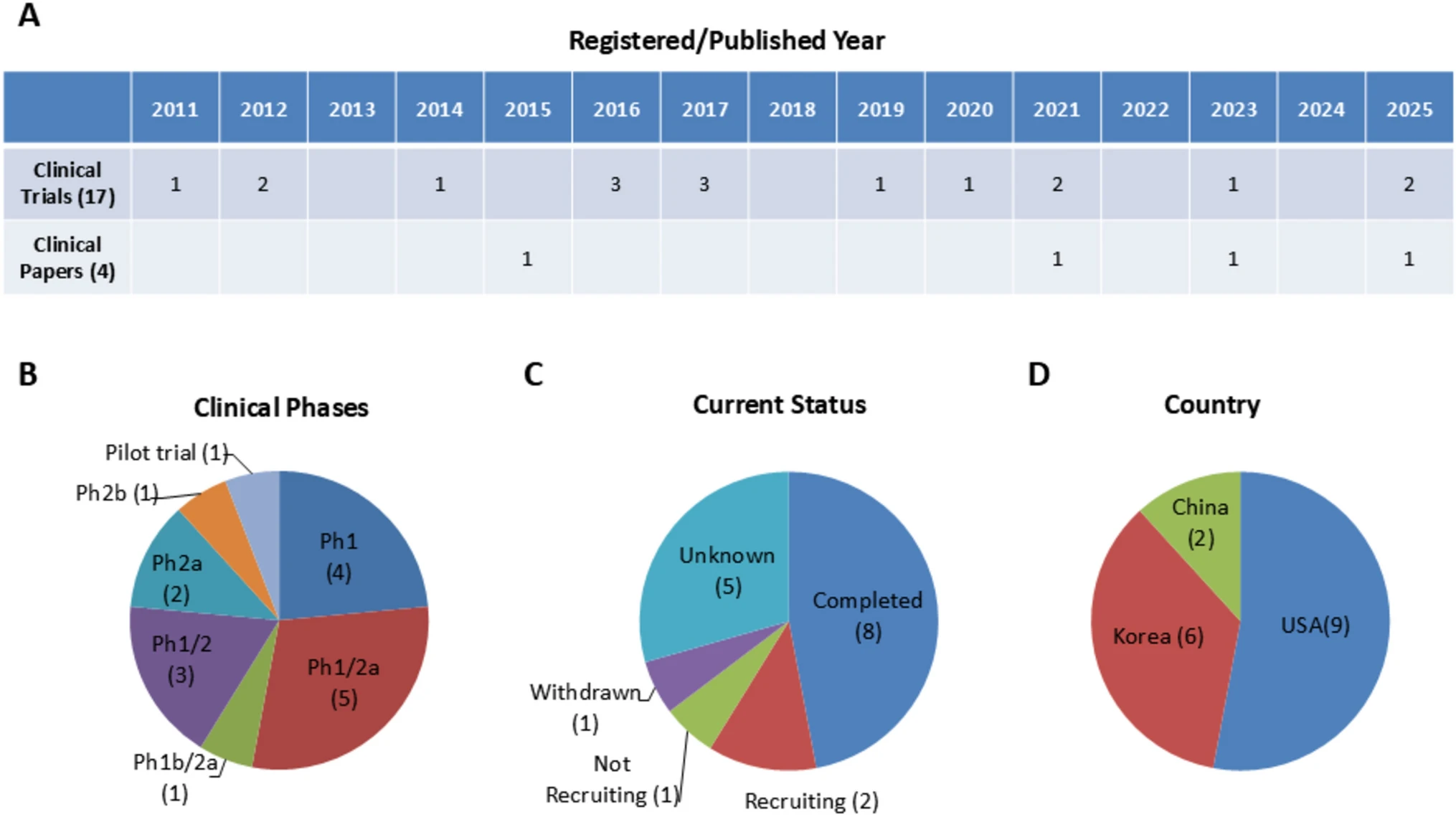
研发阶段、状态与细胞来源具体构成:所有试验均处于早期研发阶段,其具体构成如下:I期4项(23.5%),I/IIa期5项(29.4%),I/II期3项(17.6%),IIa期2项(11.8%),Ib/IIa期、IIb期及“试点”阶段各1项(各占5.9%),确无III期试验(表1)。

关于试验状态,已完成的项目最多,共8项(47.1%);进行中3项(17.6%,其中2项招募中,1项已停止招募);1项因新冠疫情终止(5.9%);剩余5项状态未知(29.4%)。
所使用的MSC来源多样,具体为:异体脐带血(UCB)来源最多,共5项(29.4%),自体脂肪组织来源4项(23.5%),异体骨髓(BM)来源3项(17.6%),异体胎盘来源1项(5.9%),另有1项来源不明。
给药途径、剂量与受试方案的详细差异:给药途径与细胞来源高度关联:所有5项使用脐带血MSC的试验均采用直接脑部注射(其中2项为立体定向注射,3项为经Ommaya储液囊脑室内注射)。其余12项使用其他来源MSC的试验则全部采用静脉注射。
在治疗方案上,单次注射细胞剂量范围很宽,为3×10^6至2×10^8个细胞。大多数试验采用多次注射方案(最多达9次),仅4项试验为单次注射。随访时间最短为10周,多数集中在12至52周之间,其中一项随访时间最长,为65周。受试者年龄范围主要集中在50至85岁。
间充质干细胞治疗17项阿尔茨海默病的临床试验总结
以下内容逐一总结了17项临床试验的详细信息 。每项试验的条目包括NCT编号、细胞类型、试验阶段/设计、年份和当前状态、受试者人数、剂量、给药方案、随访期以及结果(如有)。下文还根据所用细胞类型总结了每项临床试验的关键信息。
同种异体脐带血间充质干细胞(hUCB-MSCs)的5项试验
这组试验主要由韩国的“NEUROSTEM-AD”系列研究构成,采用脑部局部给药。
NCT01297218 (1期):开放标签,单中心。2015年完成,9名患者。分为低(3×10⁶细胞)高(6×10⁶细胞)剂量组,经立体定向注射至海马和楔前叶。24个月随访显示安全,并观察到潜在疗效信号。
NCT01696591 (观察性随访):作为上一试验的长期随访,2015年完成,随访至24个月,并纳入3名未治疗者作为对照。
NCT02054208 (1/2a期):双盲,单中心。2021年完成。分两阶段:开放标签1期(低1×10⁷、高3×10⁷细胞/次)和随机2a期(高剂量组 vs 安慰剂组)。通过Ommaya囊脑室内(ICV) 注射,共3次。结果显示安全,高剂量组部分认知评分有改善趋势。
NCT03172117 (长期随访):上一试验的延伸随访,2021年完成,计划进行36个月电话随访。
NCT04954534 (探索性疗效研究):单臂研究,计划让之前试验的安慰剂组交叉接受高剂量(3×10⁷细胞/次,ICV注射3次)治疗。状态与结果未知。
自体脂肪间充质干细胞(AdMSCs)的4项试验
这组试验主要采用静脉注射,以“AstroStem”为代表,探索多次给药的方案。
NCT03117738 (I/II期):随机双盲,安慰剂对照。已完成(结果发布于网站)。31名患者(21治疗,10安慰剂),每次静脉注射2×10⁸个细胞,共9次,随访52周。
NCT04482413 (2b期):随机双盲,安慰剂对照。状态未知。计划招募约100人,方案类似(静脉注射9次),计划随访至40周。
NCT04228666 (1/2a期):开放标签。因新冠疫情在招募前已撤回。原计划招募24人,静脉注射4次(2×10⁸细胞/次)。
NCT06775964 (1b/2a期):开放标签,单组。正在招募,预计2026年完成。计划招募12名前驱期患者,静脉注射4次(2×10⁸细胞/次),随访48周。
同种异体脐带间充质干细胞(UC MSCs)的3项试验
这三项试验均采用静脉注射,但方案设计差异较大。
NCT01547689 (I/II期):开放标签,自身对照。已完成但结果未发表。30名中重度患者,接受8次静脉输注(2×10⁷细胞/次,疗程复杂),随访仅10周。
NCT02672306 (I/II期):随机双盲,安慰剂对照。状态与结果未知。计划招募16名轻中度患者,静脉注射8次(2×10⁷细胞/次),随访48周。
NCT04040348 (I期):前瞻性开放标签。已完成治疗(2021年),结果未发表。6名轻度患者,接受4次静脉输注(间隔13周),随访期未明确。
同种异体胎盘间充质干细胞的1项试验
NCT02899091 (1/2a期):随机双盲,安慰剂对照。状态为“进行中,不再招募”。计划招募24名轻中度患者,进行单次或两次静脉输注(具体剂量未明确),随访48周。结果未公布。
同种异体骨髓间充质干细胞的3项试验
这组以“Lomecel-B”为代表,采用静脉注射,研究设计较为精细。
NCT02600130 (I期):随机双盲,安慰剂对照。2023年发表结果。33名患者,分单次低剂量(2×10⁷)、高剂量(1×10⁸)及安慰剂组,随访52周。证实安全,并显示部分生物标志物改善。
NCT05233774 (2a期):双盲,安慰剂对照。2025年发表结果。48名患者,分4组,比较了单次 vs. 4次(低剂量2.5×10⁷细胞/次或高剂量1×10⁸细胞/次)静脉输注方案。
NCT02833792 (IIa期):随机单盲,安慰剂对照交叉设计。状态不明。计划招募40人,单次静脉输注(按体重1.5×10⁶细胞/kg),交叉期6个月,总随访18个月。
细胞类型未知的1项试验
NCT06781333 (试点研究):开放标签,单组。截至2025年5月仍在招募。8名伴有严重行为症状的AD患者,接受单次静脉输注(来源与剂量均未明确),作为辅助治疗,随访12周。结果未公布。
从选定部分的临床试验验证其安全性和有效性
在纳入综述的17项临床试验中,共有7项试验的结果发表在4篇临床论文中,另有1项试验的结果发布于ClinicalTrials.gov网站(汇总于表3)。为提供关键证据概览,下文将首先概要介绍这5项已发表数据的主要结果,其详细分析与讨论将在明天的文章中展开。
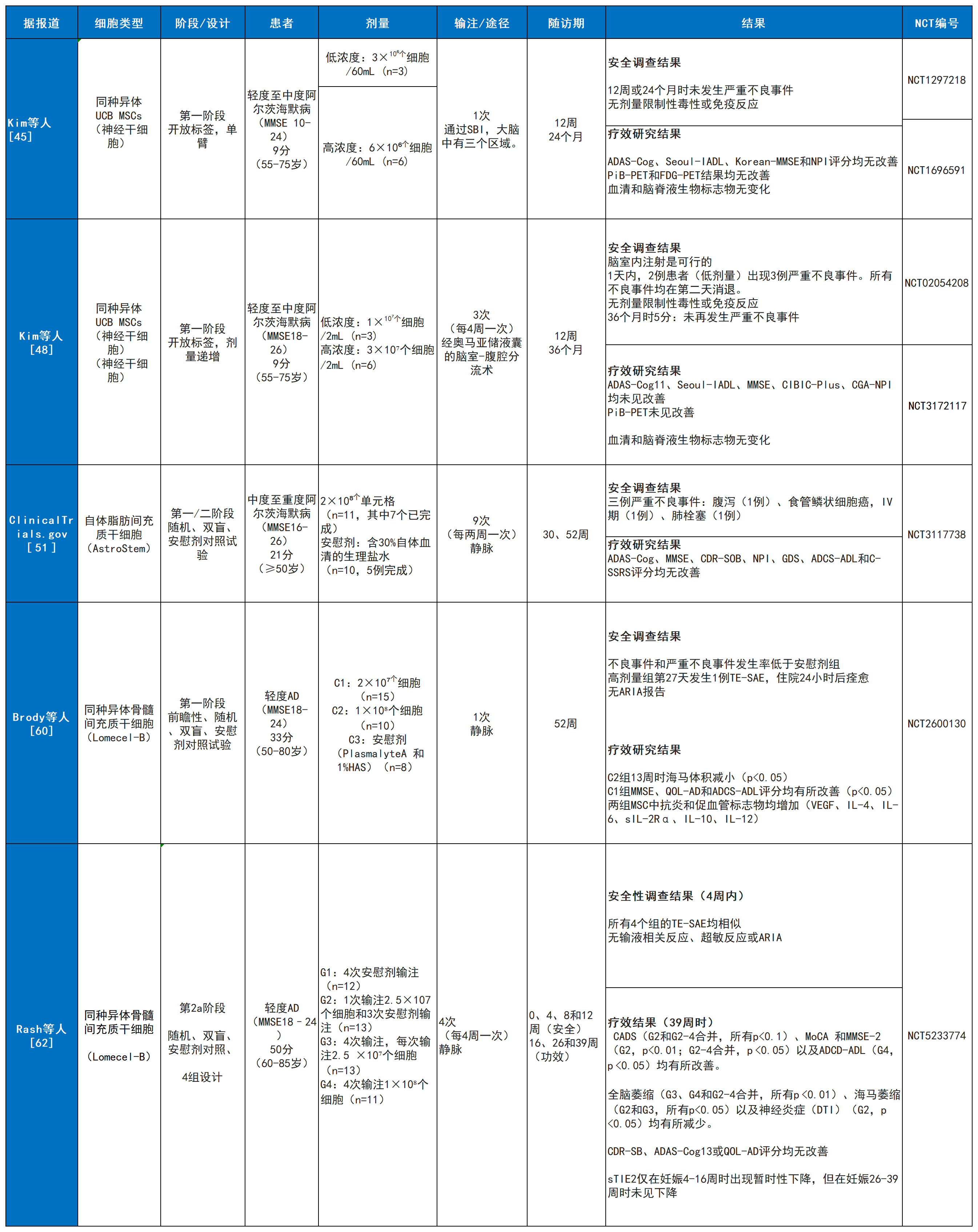
安全性总结(涵盖所有已公布结果的7项试验)
综合所有已公布数据的试验,间充质干细胞疗法在阿尔茨海默病患者中表现出良好的安全性。具体而言:
- 采用脐带血MSCs(产品NEUROSTEM-AD) 的4项试验(采用立体定向海马注射的NCT01297218与NCT01696591,以及采用脑室内注射的NCT02054208与NCT03172117)均报告治疗安全,仅出现暂时性严重不良事件。
- 采用骨髓MSCs(产品Lomecel-B)的2项试验(NCT02600130与NCT05233774)同样证实其安全性。
- 采用脂肪MSCs(产品AstroStem) 的试验(NCT03117738)结果也显示安全性良好。
有效性总结(结果存在差异)
在有效性方面,不同细胞来源的产品结果不一致:
- 骨髓MSCs(Lomecel-B)显示积极信号:试验NCT02600130和NCT05233774报告了在AD病理生理或认知功能方面的显著改善。
- 脐带血与脂肪MSCs未显示显著疗效:采用NEUROSTEM-AD的4项试验(NCT01297218NCT01696591,NCT02054208, NCT03172117)及采用AstroStem的试验(NCT03117738)均未观察到明显的治疗效果。
这种差异表明,疗效可能与特定的细胞类型、产品制备工艺或给药途径密切相关。
核心问答与未来展望
当前核心结论:安全初证,疗效待明
综上所述,间充质干细胞疗法治疗阿尔茨海默病已从实验室步入临床探索阶段,其短期安全性已获初步支撑,为后续研究奠定了基础。然而,关于其疗效的决定性证据仍然缺乏。MSCs的核心价值在于其多靶点作用机制,为应对AD的复杂性提供了新思路。当前领域的首要任务是跨越“证据鸿沟”。
未来5-10年,通过推进大规模确证性临床试验,并同步探索外泌体等创新策略,将最终明确MSCs在AD治疗格局中的定位。无论结果如何,这一探索过程所积累的深刻见解,都将对神经退行性疾病治疗领域产生重要影响。
参考资料:
[1]:Kim, AL., Lee, W.K., Kwon, S. et al. Therapeutic Efficacy of Mesenchymal Stem Cells (MSCs) on Alzheimer’s Disease: Review of Clinical Results. Tissue Eng Regen Med (2026). https://doi.org/10.1007/s13770-025-00782-1
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信