描述:2025年《自然》等多顶刊发表三项里程碑临床试验:iPSC及hESC衍生多巴胺能神经元移植治疗帕金森病,首次在人体证实安全性、可行性和剂量依赖性运动功能改善。本文系统解读胎儿组织移植教训、现代细胞疗法设计原则、三项干细胞治疗帕金森病的关键试验数据及未来挑战。
跨越数十载阵痛,2025年3项里程碑研究证实:干细胞治疗帕金森病已触手可及
引言:帕金森病再生医学的转折时刻
帕金森病(PD)再生医学已步入转折时刻。经过数十年的临床前积淀,近期首次人体试验证实,利用干细胞衍生的多巴胺能神经元进行细胞替代不仅安全可行,更显现出令人鼓舞的疗效。
人类多能干细胞——包括人胚胎干细胞(hESC)与诱导多能干细胞(iPSC)——在理论上为制备所需的多巴胺能神经元提供了无限、标准化且伦理可接受的细胞来源。伴随着分化方案的持续优化,发表于《自然》的首个同种异体iPSC衍生多巴胺能祖细胞I/II期临床试验,以及同期其他试验,共同提供了安全性、可行性和早期疗效的关键证据,使干细胞疗法从遥远的构想走向触手可及的现实,由此掀开了神经修复学的新篇章。

本文以发表于《Translational Neurodegeneration》上的综述“治疗帕金森病的新曙光:关于干细胞疗法兴起的评论”为框架[1],系统梳理三项2025年里程碑研究,回顾胎儿组织移植的历史启示,阐释现代细胞疗法的设计原则,并审视当前挑战与未来方向。
一、历史基石:从胎儿组织移植中汲取的教训
1.1 早期成就:概念验证的奠定
胎儿组织移植的早期开放标签试验首次令人信服地证明:移植的多巴胺能神经元能够在人脑中长期存活、整合入宿主神经回路,并持续改善临床症状。这确立了细胞替代策略治疗神经系统疾病的可能性。
1.2 失败中揭示的根本局限
随后的双盲、安慰剂对照试验未达到主要终点,还暴露出较高的移植物诱导的运动障碍(GIDs) 发生率,迫使领域从“能不能做”转向“如何做得更安全、更一致”。
1.3 核心教训
| 教训 | 具体内容 | 现代对策 |
|---|---|---|
| 细胞纯度 | 胎儿组织中混杂的血清素能神经元是GIDs的关键因素 | 生成高纯度、标准化的多巴胺能祖细胞,剔除脱靶细胞 |
| 患者选择 | 年轻、早期患者获益更大,病理环境影响移植效果 | 严格筛选合适时间窗的患者 |
| 免疫抑制 | 过去方案不充分,隐匿性排斥导致疗效波动 | 强效、标准化免疫抑制(他克莫司约15个月) |
| 移植分布 | 壳核“斑片状”神经支配形成局部多巴胺热点 | 多通道注射模式,实现更均匀覆盖 |
二、干细胞治疗帕金森病的核心原则
帕金森病细胞治疗的目标是通过移植能够发育为真正的、具有功能的A9型中脑多巴胺能神经元的细胞,从而重建受损的神经回路——而A9型多巴胺能神经元正是帕金森病中丧失的神经元亚群。这些A9型多巴胺能神经元专门投射至背侧壳核,即纹状体的运动区。
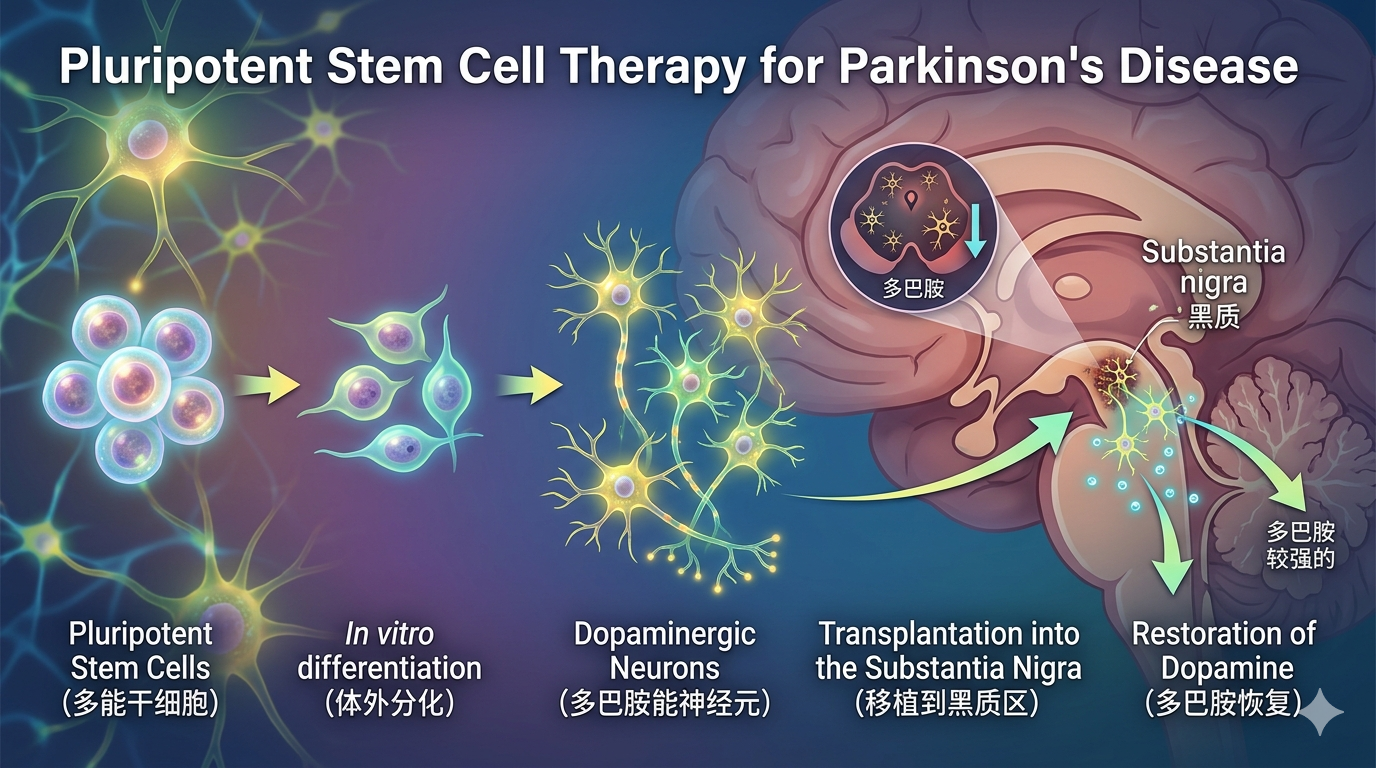
2.1 精确重建A9型中脑多巴胺能神经元命运
干细胞疗法的首要原则,是通过模拟胚胎发育信号,将人多能干细胞定向分化为功能性A9型多巴胺能神经元。这一过程包括:通过双重SMAD抑制阻断BMP等非神经通路,完成神经定向诱导;利用音猬因子提供腹侧化信号,并时序性调控Wnt通路以确立中脑身份;诱导表达底板中间阶段标志物LMX1A与FOXA2,并共表达OTX2、EN1,以锁定真正的A9祖细胞身份;移植后,祖细胞在宿主环境中历经数月终末分化,实现突触形成和功能性多巴胺释放,最终重建受损神经回路。
2.2 精准靶向壳核进行解剖学重建
治疗策略的核心原则是将祖细胞立体定向移植至壳核,尤其是背侧运动区,以达成异位但功能性的多巴胺能神经支配。直接绕过失退化的黑质,将产多巴胺细胞递送至纹状体运动区室,旨在恢复运动环路功能。
手术上,采用多针道、多点沉积“突触小体”的方式,确保广泛而均匀的神经支配,避免斑片状多巴胺水平;同时使用专用微型套管以减轻宿主组织机械损伤与局部炎症,提高细胞存活率。此外,转向同种异体HLA纯合供体iPSC系,可推动标准化生产、剂量一致性与可扩展性,迈向即用型细胞产品。
2.3 应对异体移植的免疫挑战
针对同种异体“即用型”细胞产品,须恪守免疫抑制与未来免疫逃逸的原则。移植后需使用他克莫司等药物约15个月,抑制T细胞活化,降低因血脑屏障破坏和外源性HLA标记所引发的免疫攻击。选用常见HLA单倍型供体细胞系可缩小免疫距离,但临床数据显示,匹配与否对安全性及疗效影响并不显著。
当前实践通常在术后1至1.5年停用免疫抑制剂,然而慢性低度炎症或延迟排斥的风险依然存在,成为领域内悬而未决的核心问题。未来,借助CRISPR/Cas9编辑MHC分子,开发“免疫逃逸”或通用供体细胞,有望彻底免除长期全身免疫抑制,使再生疗法真正可及。
三、2025年三项里程碑临床试验详解
2025年是神经修复学领域的一个里程碑,标志着三项地域和技术各异的临床试验结果几乎同时发表。这些研究共同确立了安全性是帕金森病干细胞疗法的一项基础性里程碑(图1)。为了对这三项具有里程碑意义的2025年临床试验进行全面阐述,下文将总结每项研究的试验设计、安全性结果和疗效信号(表1)。
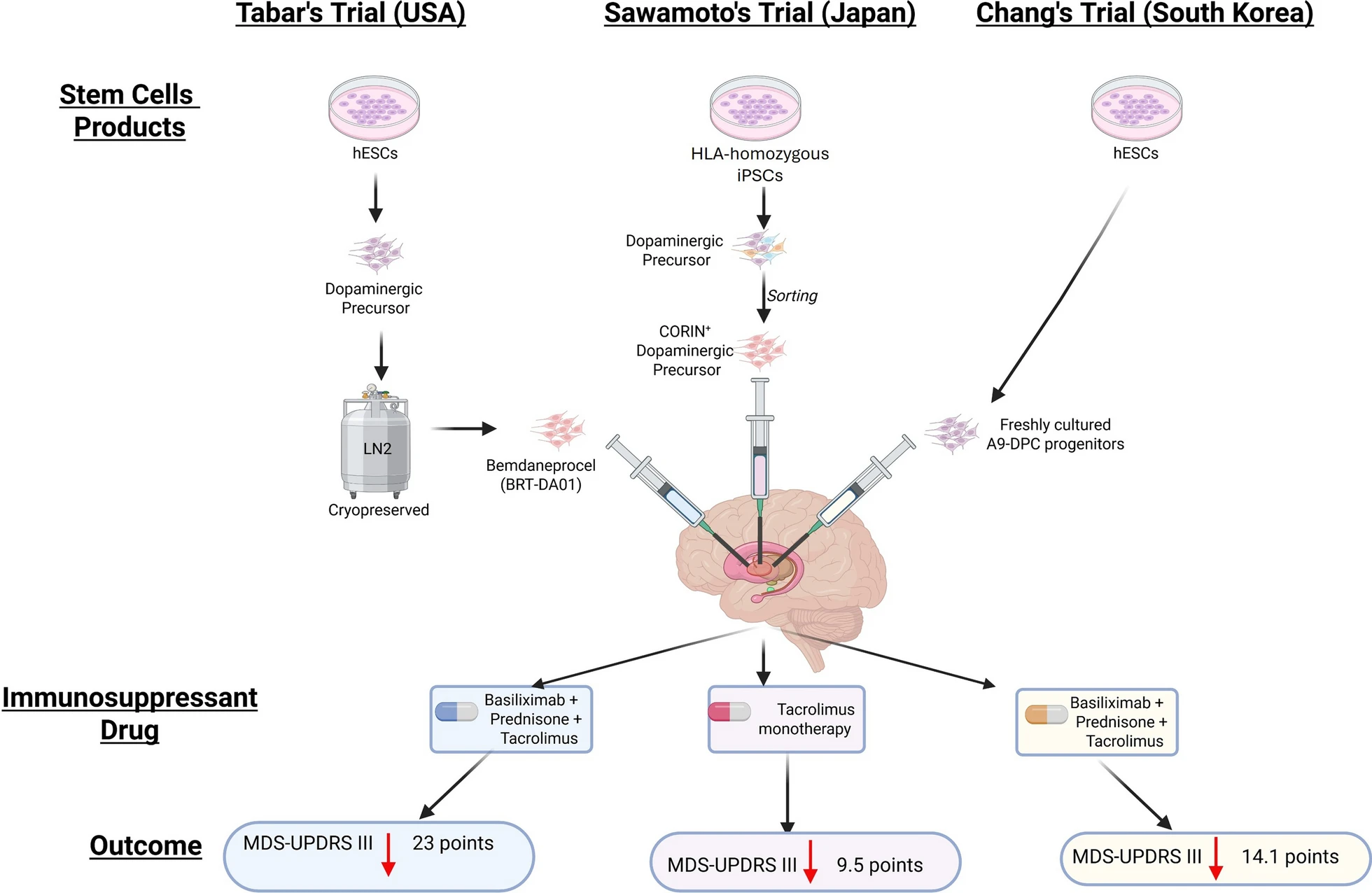
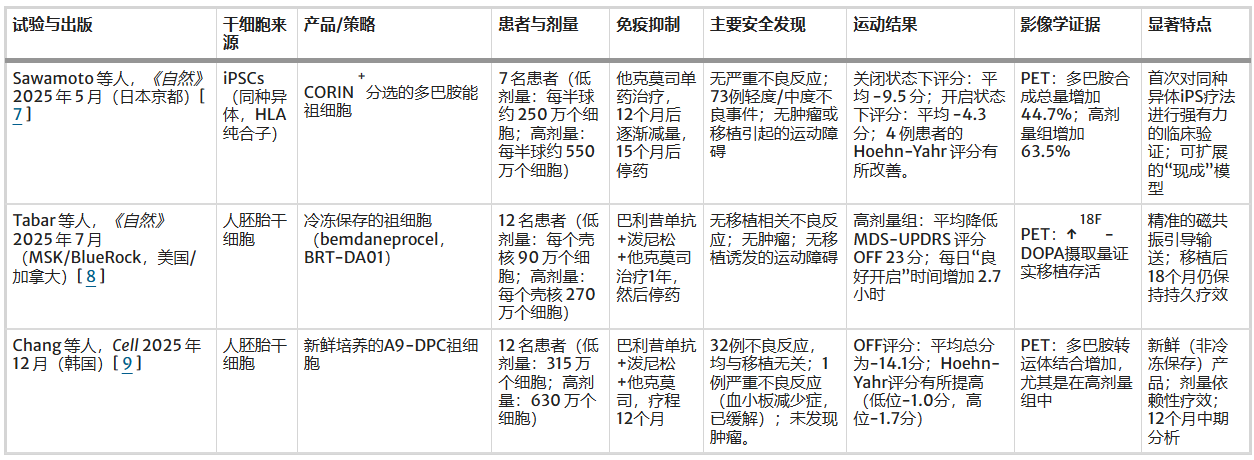
3.1 试验一:日本iPSC源多巴胺能细胞I/II期试验(Sawamoto等,《自然》2025)
这项里程碑式研究使用了源自临床级iPSC细胞系的新鲜多巴胺能祖细胞。为兼顾可扩展性与低排斥风险,研究人员采用一名健康供体的同种异体细胞,该供体携带常见HLA单倍型的纯合子,与约17%的日本人群相匹配。试验采用剂量递增设计,低剂量组3例(每侧半球2.1–2.6×10⁶个细胞),高剂量组4例(每侧半球5.3–5.5×10⁶个细胞),术后均维持他克莫司15个月。值得注意的是,无论患者与供体细胞系HLA匹配与否,均被纳入研究[2]。

24个月的安全性结果极为积极:无移植物相关严重不良事件,无死亡、肿瘤或移植物过度生长。连续磁共振成像及¹⁸F-FLT PET均未发现增殖信号。尤为关键的是,未报告任何移植物诱导的运动障碍,这被归功于高纯度CORIN阳性祖细胞以及血清素能神经元的剔除。疗效信号同样令人鼓舞:6例可评估患者中,4例在“停药”状态下MDS-UPDRS第三部分出现改善,平均降低9.5分(20.4%)。¹⁸F-L-DOPA PET显像提供了移植物功能的客观证据,并呈现显著的剂量依赖性效应——高剂量组多巴胺合成增加63.5%,而低剂量组仅增加7.0%。
3.2 试验二:美国/加拿大人胚胎干细胞源多巴胺能神经元I期试验(Tabar等,Bemdaneprocel)
BlueRock Therapeutics公司的试验(研究bemdaneprocel,常以首席外科医生命名称为“Tabar试验”)使用了源自人胚胎干细胞(hESC)的多巴胺能神经元前体细胞。这项多中心、开放标签研究共纳入12名参与者,分为两个队列:低剂量组每侧壳核接受90万个细胞,高剂量组每侧壳核接受270万个细胞。与iPSC试验类似,参与者接受了为期一年的免疫抑制治疗以促进移植物存活[3]。

试验达到了证明安全性和耐受性的主要终点,在随访期间未报告与细胞产品相关的严重不良事件。连续影像学和临床评估证实了无肿瘤或移植物诱导的运动障碍(GIDs)。探索性疗效数据非常令人鼓舞,尤其是在高剂量组中,该组患者在一年时的MDS-UPDRS第三部分“停药”状态下平均改善了23.0分。运动获益在移植后18个月仍得以维持,且高剂量组在免疫抑制停药后观察到持续改善。PET显像证实了这些临床发现,显示了细胞存活和功能性移植物整合的持续证据。
3.3 试验三:韩国人胚胎干细胞源多巴胺能前体细胞1/2a期试验(Chang等,TED-A9)
该项在韩国开展的单中心、剂量递增试验,评估了同样源自人胚胎干细胞的高纯度A9型多巴胺能前体细胞TED-A9,共纳入12例中重度帕金森病患者,行双侧壳核移植。患者分为低剂量组(315万个细胞)和高剂量组(630万个细胞),并接受标准化一年免疫抑制方案[4]。

安全性结果与其他里程碑试验一致:无剂量限制性毒性,无移植物相关严重不良事件,无肿瘤形成或过度生长证据。12个月时,MDS-UPDRS第三部分“停药”状态下平均降低14.1分,高剂量组获益更为显著。
尽管改善幅度较Tabar试验18个月时的23分降幅略显温和,但仍属三项研究中最为突出的疗效之一。¹⁸F-FP-CIT PET显像显示后壳核多巴胺转运体摄取显著增加,为移植物存活和再神经支配提供了客观确认,进一步巩固了移植细胞数量与临床改善程度之间的剂量依赖性关系。
小结:三项试验汇集出一系列共识:干细胞来源的多巴胺能前体细胞安全,能在宿主脑内存活、产生多巴胺,并以剂量依赖性方式改善运动症状。尽管细胞来源、生产方法与地域各不相同,这些结果共同标志着领域已跨越胎儿组织移植的历史局限,为更大规模对照研究铺平了道路,后者将进一步明确该治疗策略的长期有效性与持久性。
三项试验汇总对比表
| 维度 | Sawamoto(日本,iPSC) | Tabar(美/加,hESC) | Chang(韩国,hESC) |
|---|---|---|---|
| 细胞类型 | iPSC源CORIN+祖细胞 | hESC源前体(Bemdaneprocel) | hESC源A9-DPCs(TED-A9) |
| 细胞剂量(高剂量组) | 5.3-5.5×10⁶/侧 | 2.7×10⁶/侧 | 6.3×10⁶/侧(总量) |
| 免疫抑制时长 | 15个月 | 12个月 | 12个月 |
| 随访时间 | 24个月 | 18个月 | 12个月 |
| MDS-UPDRS III改善 | 20.4%降幅(约9.5分) | 23.0分降幅 | 14.1分降幅 |
| PET证据 | 高剂量组多巴胺合成↑63.5% | 移植物存活 | 多巴胺转运体摄取↑ |
| GIDs | 无 | 无 | 无 |
四、前瞻与挑战:驶向更广义的修复
4.1 核心技术瓶颈:再神经支配不均
当前PET显像常显示仅形成局灶性“热点”,远未实现全纹状体均匀覆盖。后续需探索:
- 更高细胞剂量
- 更精细的多轨道立体定向注射
- 明确最佳移植部位与细胞数量
4.2 疗效需超越现有疗法
未来试验必须在临床改善程度上实现对现有药物及深部脑刺激(DBS) 的明确超越,而不仅是重复早期开放标签研究的效应幅度。
4.3 联合治疗体系的构建
单纯的多巴胺能细胞替代无法阻止疾病本身的持续进展。需要:
- 神经保护剂和抗α-突触核蛋白疗法协同保护新生神经元
- 专门的物理康复促进新神经回路的功能性整合
4.4 技术迭代方向
| 方向 | 目标 |
|---|---|
| CRISPR/Cas9编辑 | 制造“低免疫原性”或“通用”供体细胞,摆脱长期免疫抑制 |
| 下一代分选方案 | 提高前体细胞向功能性多巴胺能神经元的成熟效率 |
| 精细患者筛选 | 将宿主因素和脑微环境纳入考量,确保安全整合 |
4.5 长期安全性
最大的底线问题:确证iPSC来源前体细胞与分化神经元的长期安全性(致瘤风险、异常整合等),这需要长期随访和大规模验证。
五、常见问题解答(FAQ)
问1:干细胞治疗帕金森病目前成熟吗?我/家人能用上吗?
答:尚未成熟。2025年发表的三项临床试验是首次人体I/II期研究,证实了安全性和初步疗效,但尚未成为常规临床治疗。目前全球无任何干细胞产品正式获批用于帕金森病。患者可通过参加正规临床试验(免费)获得治疗。任何声称“成熟应用”并收费的机构均属违规。
问2:这三项试验的结果到底有多好?能治好吗?
答:结果令人鼓舞但有局限性:
- 安全性:三项试验均未报告移植物诱导的运动障碍(GIDs)、肿瘤或严重不良事件,这是重大进步。
- 疗效:在“停药”状态下,运动症状评分(MDS-UPDRS III)平均改善14-23分(最佳达23分),且呈剂量依赖性。但这不是治愈——患者仍需继续服用常规药物,且非运动症状(如认知障碍、自主神经功能紊乱)改善有限。
- 长期效果:随访仅12-24个月,持久性尚待验证。
问3:iPSC和hESC有什么区别?哪个更好?
答:
| 维度 | iPSC | hESC |
|---|---|---|
| 来源 | 重编程成体细胞(如皮肤、血细胞) | 胚胎囊胚期内细胞团 |
| 伦理争议 | 无(不破坏胚胎) | 有(传统来源存在争议,但已建立细胞系可豁免) |
| 个体化 | 可自体(但成本极高),也可异体 | 仅异体 |
| 致瘤风险 | 理论更高(需严格质控) | 较低(但仍需关注) |
| 标准化 | 需每个供体重建 | 可建立稳定细胞系 |
目前尚无头对头比较。三项试验中iPSC和hESC均显示了良好安全性和疗效。
问4:治疗过程是怎样的?需要开颅吗?
答:需要立体定向神经外科手术,但属于微创操作:
- 术前影像定位壳核靶点
- 局部麻醉或轻度镇静
- 颅骨钻一小孔,通过微型套管将细胞悬液缓慢注入壳核(多针道、多点沉积)
- 手术时间约2-4小时,住院3-7天
相比深部脑刺激(DBS)需植入永久电极,细胞移植不留置异物,创伤更小。
问5:治疗后还需要吃药吗?免疫抑制剂要服多久?
答:
- 抗帕金森病药物:术后仍需要。移植物产生的多巴胺是局部的,无法替代全身性药物,但部分患者可能逐渐减少剂量。
- 免疫抑制剂:异体移植需要。目前方案为术后使用他克莫司约12-15个月,之后停药。未来若采用“免疫逃逸”通用细胞,可能完全免除。
问6:治疗费用多少?医保能报销吗?
答:目前仅限临床试验阶段,完全免费(包括细胞产品、手术、相关检查)。正式上市后,价格预计昂贵(可能数十万美元)。短期内无法进入医保。建议关注正规临床试验招募信息。
问7:哪些帕金森病患者适合参加这类临床试验?
答:根据历史经验和现有试验入排标准,通常要求:
- 年龄:一般50-70岁
- 病程:通常≥5年,且对左旋多巴反应良好(证明多巴胺能系统仍存在)
- 疾病阶段:Hoehn-Yahr分期2-3期(中度,非卧床困难或严重残疾)
- 无严重认知障碍:MMSE或MoCA评分达标
- 无活动性肿瘤、严重感染、免疫缺陷
早期患者和晚期患者通常不是最佳候选者。具体需咨询研究团队。
问8:预计什么时候能在中国开展临床试验或上市?
答:
- 国内临床试验:已有多个干细胞治疗帕金森病项目在国家备案(可查询中国临床试验注册中心),但多为MSCs或其它类型细胞,尚未有iPSC/hESC源多巴胺能神经元移植的I/III期试验公开招募。预计未来2-3年可能出现。
- 上市:若III期试验顺利,至少还需5-8年(欧美可能更早)。请理性看待,不要轻信商业机构宣传。
问9:试验中提到的“移植物诱导的运动障碍(GIDs)”是什么?为什么这次试验没有?
答:GIDs是过去胎儿组织移植中出现的严重并发症——移植物中混杂的血清素能神经元释放过多血清素,导致不自主的舞蹈样或肌张力障碍性运动。现代方案通过高纯度分选(如CORIN阳性选择) 剔除血清素能细胞,从根本上避免了GIDs。三项试验均未报告GIDs,是重大安全进步。
问10:国内患者如何获取最新信息?有推荐的医院或专家吗?
答:
- 关注官方平台:国家卫健委干细胞临床研究备案系统、中国临床试验注册中心(www.chictr.org.cn)
- 搜索关键词:“帕金森病 + 干细胞 + 临床试验”
- 建议咨询的顶尖中心:北京宣武医院、上海瑞金医院、中山大学附属第一医院、空军军医大学西京医院等(均有帕金森病细胞治疗研究方向)
- 重要提示:切勿使用搜索引擎中“干细胞治疗帕金森病”的商业广告,这些多为非正规机构。
六、结语:从可能迈向更优
细胞替代疗法已从概念验证迈入临床可行性阶段。以京都大学试验为代表的同种异体iPSC源性多巴胺能前体细胞移植,提供了首个强有力的同行评审证据,证实该干预手段安全且可行——未见致瘤性,未现GIDs,并观察到剂量依赖性运动功能改善和PET影像上的移植物存活证据。与此同时,旨在通过自体iPSC消除免疫抑制的ASPIRO试验(NCT06344026),以及探索剂量递增的STEM-PD试验(NCT05635409),正从不同维度同步推动领域前行。
然而,当前结果仍须谨慎解读:临床改善程度尚未明确超越现有药物和DBS,且长期安全性始终是悬而未决的首要问题。领域的核心命题已从 “是否可能”推进为“如何做得更好并惠及所有患者”。
尽管挑战重重,这些试验已将替换丧失神经元这一修复性治疗的梦想,从概念转化为一种具体且初见成效的临床策略,预示着一个充满希望的新黎明。
参考资料
[1] Elvira, R., Chooi, W.H., Wang, H. et al. A new dawn for Parkinson’s disease: commentary on the emergence of stem cell-based therapies. Transl Neurodegener 15, 20 (2026). https://doi.org/10.1186/s40035-026-00556-2
[2] Sawamoto, N., Doi, D., Nakanishi, E. et al. Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease. Nature 641, 971–977 (2025). https://doi.org/10.1038/s41586-025-08700-0
[3] Tabar, V., Sarva, H., Lozano, A.M. et al. Phase I trial of hES cell-derived dopaminergic neurons for Parkinson’s disease. Nature 641, 978–983 (2025). https://doi.org/10.1038/s41586-025-08845-y
[4] Chang et al. Cell (2025). https://www.cell.com/action/showCitFormats?pii=S0092-8674(25)01041-4
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议或治疗推荐。本文内容不能替代医生或药剂师的专业建议。所有治疗决策请咨询正规医疗机构专科医生。杭吉干细胞所发布的信息仅供参考。如有版权等疑问,请随时联系。




 扫码添加官方微信
扫码添加官方微信