脑瘫 (CP) 是儿童中最常见的运动功能障碍,在中低收入国家,每1000名儿童的患病率为2.3至3.7名。脑瘫可由先天性或后天性原因引起。物理治疗是脑瘫的标准治疗方法,然而,由于物理治疗无法修复脑损伤,其疗效有限。2013年,首例细胞疗法应用于一名因心脏骤停导致脑缺血的2.5岁儿童。此后,细胞疗法已应用于众多脑瘫病例,并显示出良好的疗效。然而,该方法的关键方面,例如适应症、细胞类型、剂量和给药途径,仍需进一步研究。
干细胞移植技术重塑治疗脑瘫的方式?通过解答9大疑问证明其可行性
本章结合文献和我们自身的经验,分析了脑性瘫痪(CP)细胞疗法的各个方面。我们介绍了我们利用细胞疗法治疗CP患者的研究成果,并探讨了围绕该治疗方法的争议及其未来前景。
1、什么是脑性瘫痪,脑瘫命名的由来?
“脑瘫”一词源于希腊语和拉丁语。“Cerebral palsy”源于“cerebrum”,意为“大脑”。“Palsy”源于“palsis”,意为“瘫痪”。
脑瘫 (CP) 是指发育中的胎儿或婴儿大脑中出现的一组永久性运动和姿势发育障碍。脑瘫是儿童最常见的运动功能障碍,在中低收入国家,每1000名儿童中患病率为2.3至3.7人,在高收入国家,每1000名儿童中患病率为1.6至2.9人。
根据CP发生的时间,CP可分为以下两类:
- 围产期脑性瘫痪,是指在出生后28天内围产期出现脑损伤/发育不良或病因不明。
- 新生儿后脑性瘫痪,是由新生儿期(出生后28天)之后、2岁之前发生的已知脑损伤事件引起的。
根据临床特征,脑性瘫痪可分为痉挛性脑性瘫痪、运动障碍/肌张力障碍性脑性瘫痪或共济失调性脑性瘫痪。
脑性瘫痪最常见的运动障碍是痉挛(肌肉僵硬)。80%的脑性瘫痪患儿受此影响,根据受影响的肢体,可分为双瘫、偏瘫或四肢瘫痪(图1)。
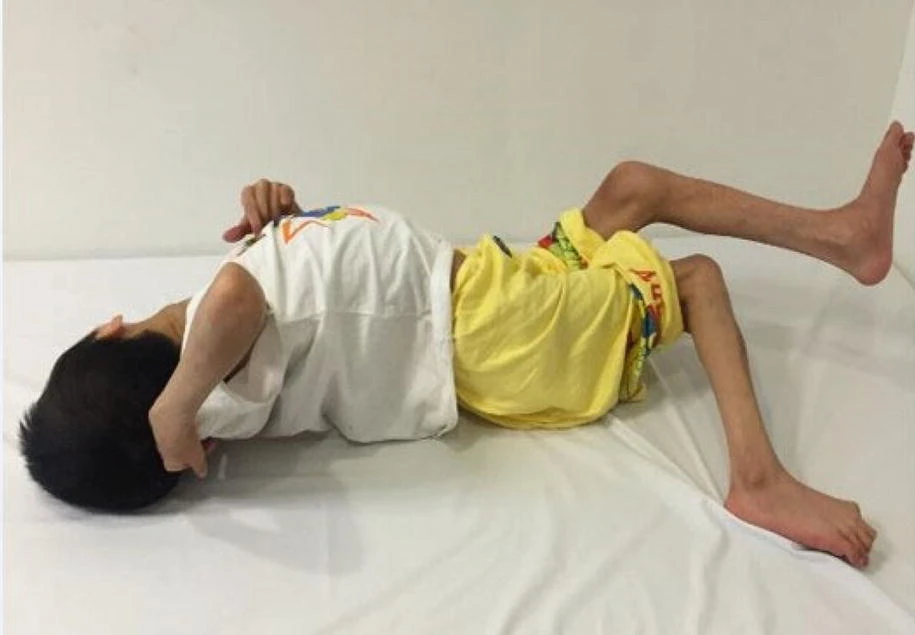
运动功能障碍是脑性瘫痪的一个显著特征;然而,值得注意的是,也经常观察到各种其他障碍:
- 失禁:85%
- 认知障碍:77%
- 疼痛:75%
- 智力障碍:50%
- 睡眠障碍:40%
- 步态障碍:33%
- 髋关节放置:33%
- 癫痫:25%
- 行为障碍:25%
- 言语问题:25%
- 视力障碍:10%
- 听力障碍:9%
脑性瘫痪的治疗需要多学科方法,例如康复、药物、营养和心理学。虽然脑性瘫痪的治疗已取得显著进展,但传统方法仍然存在局限性,因为它们没有解决潜在的脑损伤。
近年来,细胞疗法已应用于脑性瘫痪,并取得了初步成功。
2013年,细胞疗法首次应用于治疗脑瘫,患者是一名2.5岁男孩,因心脏骤停出现脑缺血。心脏骤停后第五天进行的神经儿科检查显示,患者出现全身缺氧缺血性脑损伤,并处于持续性植物状态。脑损伤经脑MRI确诊。患者接受了91.7mL冷冻保存的自体脐带血输血,其中含有5.75×10^8个单核细胞。输血后,患者的精神运动发育显著改善[1]。
2、干细胞疗法治疗脑瘫的作用机制是什么?
细胞疗法(尤其是干细胞治疗)在脑瘫治疗中的核心作用机制是多维度、多靶点的,主要围绕神经修复、免疫调节、微环境改善等方面展开。以下是基于现有临床研究证据的关键机制分析:
一、神经修复与细胞替代
- 分化为神经细胞:干细胞(如神经干细胞、间充质干细胞)可定向分化为神经元、少突胶质细胞等,直接替换因缺氧或炎症损伤的神经细胞,重建受损的神经通路。例如,神经干细胞移植后分化为功能性神经元,改善运动信号传导。
- 促进髓鞘再生:少突胶质细胞的再生修复髓鞘结构,加速神经电信号传递,缓解运动障碍。动物实验证实,干细胞移植后白质完整性显著提升,与运动功能改善直接相关。
二、免疫调节与抗炎作用
- 抑制炎症因子释放:间充质干细胞(MSCs)通过分泌抗炎因子(如IL-10、TGF-β),抑制TNF-α、IL-1β等促炎因子,减轻脑部慢性炎症对神经的持续损伤。
- 调节免疫细胞活性:干细胞可调节小胶质细胞和巨噬细胞向抗炎表型(M2型)转化,减少神经毒性微环境,为修复创造有利条件。
| 分泌因子 | 靶向细胞 | 功能效果 |
|---|---|---|
| IL-10 | 巨噬细胞 | 抑制炎症反应 |
| TGF-β | T细胞 | 调节免疫耐受 |
| PGE2 | 小胶质细胞 | 促进修复表型 |
三、神经保护与营养支持
- 营养因子分泌:干细胞分泌神经营养因子(如BDNF、GDNF、VEGF),支持神经元存活、轴突生长和突触重塑。例如,BDNF增强神经可塑性,改善脑瘫患儿的运动学习能力。
- 抗凋亡作用:通过激活PI3K/Akt等信号通路,抑制受损神经元的程序性死亡,保留残余神经功能。
四、血管新生与微循环改善
- 促进血管生成:干细胞分泌VEGF、IGF-1等因子,刺激新生血管形成,增加缺血脑区的血供和氧气输送,缓解局部缺氧。
- 修复血脑屏障:通过减少炎症损伤和增强内皮细胞连接,修复血脑屏障完整性,防止毒性物质渗入脑组织。
五、干细胞类型与机制差异
不同来源的干细胞作用机制各有侧重:
- 间充质干细胞(MSCs):以旁分泌效应为主(占疗效80%以上),强于免疫调节和血管新生,安全性高。
- 神经干细胞(NSCs):直接分化为神经细胞,更适合结构性神经修复,但移植技术要求更高。
- 脐带血干细胞:含多种干细胞亚群,兼具免疫调节和神经分化潜力,尤其适合早产儿脑损伤早期干预。
| 干细胞类型 | 核心机制 | 临床优势 |
|---|---|---|
| 间充质干细胞(MSC) | 旁分泌、免疫调节、血管新生 | 安全性高,易获取 |
| 神经干细胞(NSC) | 神经分化、髓鞘再生 | 结构修复更直接 |
| 脐带血干细胞 | 多向分化、抗炎、营养支持 | 免疫原性低,适合早期治疗 |
六、移植途径与疗效优化
移植方式直接影响干细胞归巢效率和作用靶向性:
- 鞘内注射:突破血脑屏障,细胞直接进入脑脊液,适用于MSCs和NSCs,改善运动功能最显著。
- 静脉输注:依赖炎症趋化归巢,适合全身性免疫调节,但脑部靶向性较低。
- 鼻腔给药:无创途径,通过嗅神经通路入脑,大连医科大学团队应用该技术使80%患儿运动功能提升。
小结:细胞疗法通过神经替代、免疫稳态重建、营养支持及血管再生的综合机制改善脑瘫症状,其中旁分泌效应是核心(占主导作用而非直接细胞替代)。当前挑战包括最佳剂量标准化(如大剂量UCBCs疗效更优)、治疗时间窗(急性期干预效果更佳)以及长期安全性验证。未来需结合外泌体、基因编辑技术提升靶向性,并通过多中心随机试验确立个体化方案。
3、干细胞疗法治疗脑瘫的适应症与禁忌症是什么?
目前针对脑瘫(CP)细胞疗法的适应症与禁忌症尚未形成共识。Sharma研究中纳入的42名CP患者(年龄17个月至22岁)未明确区分先天性与获得性脑瘫;Huang研究的CP患者(3-12岁)同样未说明病因。而其他研究则明确标注了CP病因,并提供了详细的纳入与排除标准。
推荐方案:细胞疗法适用于获得性脑瘫患者,排除遗传异常病例。若病史与脑部MRI无法排除遗传异常,需进行全外显子测序。早期干预对预防关节畸形及改善运动功能至关重要。具体标准如下:
适应症
- 确诊的获得性脑瘫
- 粗大运动功能分级(GMFM)II-IV级
- 年龄1-15周岁
禁忌症
- 遗传异常相关的脑瘫
- 活动性感染、HIV
- 凝血功能障碍
4、干细胞疗法治疗脑瘫的细胞主要来源是?
CP细胞治疗常用四种来源:自体骨髓单核细胞(BMMNCs)、脐带血单核细胞(UCB-MNCs)、骨髓间充质干细胞、脐带间充质干细胞(UCMSCs)。
BMMNC采集流程:全身麻醉下于手术室行双侧髂前上棘骨髓抽吸(图2)。
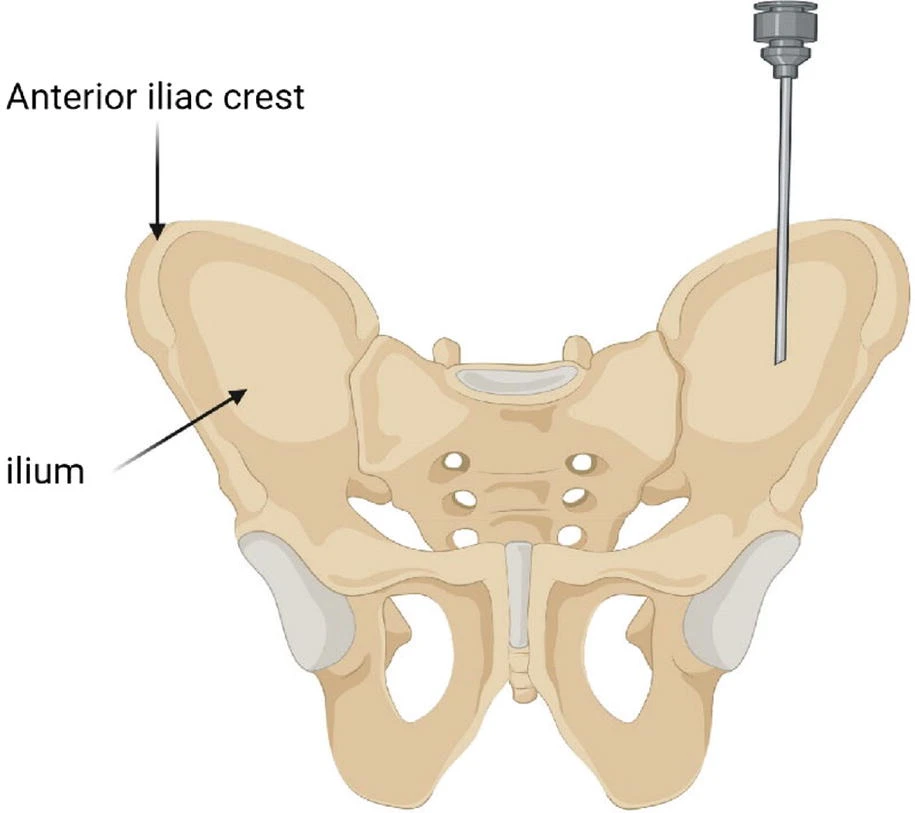
骨髓采集量根据患者体重确定:<10kg者按8mL/kg采集,>10kg者按7mL/kg采集,总量不超过250mL。
在洁净室中,通过Ficoll-Paque梯度离心法从骨髓抽吸液分离单核细胞。BMMNCs经磷酸盐缓冲液(PBS)洗涤两次后,用10mL生理盐水重悬备用。输注前需进行细胞质控检测。
5、不同类型的细胞疗法治疗脑瘫的细胞剂量是什么标准?
| 细胞类型 | 剂量方案 |
|---|---|
| BMMNCs | Sharma方案:80–100mL/例;Liem方案:7–8mL/kg |
| 脐带血单核细胞 | Zarrabi方案:5×10⁶/kg;Sun方案:1–5×10⁷/kg |
| 骨髓间充质干细胞 | Huang方案:5×10⁷细胞/疗程×3疗程(间隔7天) |
| 脐带间充质干细胞 | Gu方案:4.5–5.5×10⁷细胞 |
6、细胞递送途径有哪些?
可通过外周静脉或鞘内注射输注。
鞘内注射流程:全身麻醉下,经L4-L5椎间隙行18G脊髓穿刺针鞘内置管。先自然引流出3mL脑脊液,随后在30分钟内缓慢输注含BMMNCs的生理盐水10mL。两次治疗间隔3个月(图3)。
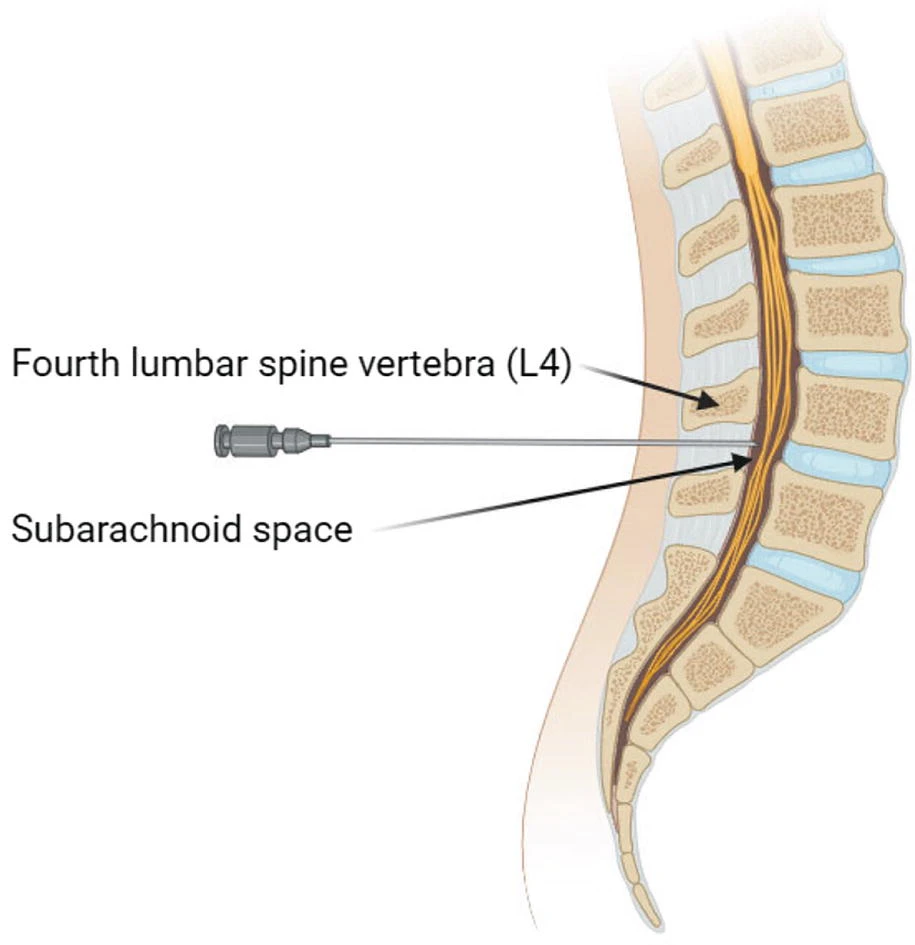
7、细胞疗法治疗脑性瘫痪是否有副作用和并发症?
细胞疗法治疗脑性瘫痪是安全的。已发表的研究中均未发现严重并发症。轻微不良事件可自行缓解或通过药物治疗缓解。
8、评估细胞治疗脑性瘫痪的疗效指标有哪些?
粗大运动功能量表(GMFM-88) 作为标准化运动功能评估工具,包含5个维度的88个项目:
(a) 卧位与翻身;(b) 坐位;(c) 爬跪位;(d) 站立位;(e) 行走跑跳位。
GMFM-88评分可转化为GMFM-66百分位值,该值反映患者相对于同年龄、同粗大运动功能分级系统(GMFCS)水平儿童的运动能力,可排除年龄增长对疗效的干扰。
功能分级系统:
- 儿童运动功能采用GMFCS分级(5级标准)
- 肌张力评估采用改良Ashworth量表
通过这些指标评估细胞疗法治疗脑瘫的结果
2022年,赣南医学院第一附属医院干细胞临床转化分中心联合赣南医学院康复医学院等报道了一项关于干细胞治疗脑瘫的疗效和安全性:系统评价和荟萃分析的研究结果,该研究纳入了9项临床试验的数据,涉及317例接受细胞疗法的患者和329例对照组患者[2]。

这些研究的结果证明了细胞疗法治疗CP的安全性,细胞疗法组和对照组的不良事件发生率无显著差异。亚组分析显示,细胞疗法在3、6和12个月时均显著提高了GMFM评分。此外,GMFM评分的提高更为显著,尤其是在脐带间充质干细胞和鞘内注射的情况下。
9、细胞疗法能治疗哪些不同原因导致的脑瘫?
与脑缺氧相关的脑性瘫痪
自2015年12月至2016年12月,将自体BMMNC鞘内输注给30例2-15岁患有脑缺氧相关脑性瘫痪的患者。所有患者的脑瘫类型均为痉挛型(29例为双瘫,仅1例为偏瘫)[3]。
根据GMFCS,严重程度为II级1例(3%),III级1例(3%),IV级13例(43%),V级15例(50%)。骨髓采集量为每1kg体重7至8mL。第一次移植每1kg体重平均单核细胞和CD34+细胞数分别为23.0×10^6和1.9×10^6。第二次移植的相应数量分别为15.6×10^6和1.3×10^6。

细胞输注期间和之后均未出现严重不良事件。轻微不良事件,例如轻度发热、呕吐和拔牙部位局部疼痛,可自行缓解或通过药物治疗缓解。细胞输注六个月后,粗大运动功能和GMFM-66百分位数与基线相比有显著改善。
具体而言,GMFM-88总分从21.7显著增加到40.0(配对t检验,p<0.001),而GMFM-66百分位数从30%增加到75%。肌张力有所改善,平均改良Ashworth评分从3.8降至2.1。此外,脑性瘫痪儿童的生活质量 (QOL) 评分 在除服务获取机会外的所有领域均有显著提高(p<0.001)。
新生儿期颅内出血所致脑性瘫痪
2015年12月至2017年5月,4例新生儿期因颅内出血而患脑性瘫痪的患儿,经鞘内途径输注自体骨髓单个核细胞。输注细胞后,所有患儿运动功能均得到改善,肌肉痉挛减少[4]。

与新生儿黄疸相关的脑性瘫痪
该试验于2014年7月至2017年7月期间进行,纳入了25名患有与新生儿黄疸相关的CP且GMFCS水平在II级至V级之间的患者。从患者的髂嵴中提取BMMNC。通过鞘内途径进行两次BMMNC输注:第一次移植在基线时进行,第二次移植在第一次移植后6个月进行[5]。

使用粗大运动功能测量 (GMFM) 和改良Ashworth量表测量粗大运动功能和肌张力。观察到粗大运动功能显著改善和肌张力显著下降。88项GMFM (GMFM-88) 的总分、每个GMFM-88领域的得分和66项GMFM (GMFM-66) 百分位数在第一次移植后6个月和12个月均显著高于相应的基线测量值。此外,细胞输注后观察到肌肉张力显著降低。
争议要点和未来方向
尽管大量临床试验和荟萃分析已证实细胞疗法治疗脑性瘫痪 (CP) 的安全性和有效性,但争议依然存在。其中,CP应使用哪种细胞类型仍是一个有争议的话题。
细胞类型选择争议:最常用的BMMNCs、脐带血单核细胞及各类间充质干细胞(MSCs)各存优劣。脐带血单核细胞虽易获取且可多次输注,但细胞数量有限且个体差异显著;BMMNCs采集成本低且无需体外处理,但需麻醉操作且难以重复采集;MSCs(尤其脐带来源)支持规模化培养与现成储存,但生产成本高昂。因此,细胞类型需个体化选择,尚无普适方案。
| 细胞类型 | 优势 | 局限 |
|---|---|---|
| 脐带血单核细胞 | •来源便捷,可多次输注 •自体/异体均可应用 | • 细胞数量有限且个体差异大 |
| 自体骨髓单核细胞(BMMNCs) | •随时获取,无需培养扩增 •成本效益高 | • 需麻醉下采集 •难以重复操作 |
| 间充质干细胞(MSCs) | •可大规模培养•支持”现成储存” • 脐带组织来源丰富 | • 培养成本高昂(需GMP设施及昂贵试剂) |
输注途径争议:静脉输注操作简便但超过70%细胞会滞留于肺/脾/肠道,导致疗效受限;鞘内注射虽需腰椎穿刺,却能靶向中枢神经系统且疗效显著优于静脉途径。故推荐首次治疗优先选择鞘内注射,后续必要时补充静脉输注。
| 途径 | 特点 | 缺陷 |
|---|---|---|
| 静脉输注 | • 操作简易安全 | •>70%细胞滞留肺/脾/肠道 •疗效显著低于鞘内注射 |
| 鞘内注射 | • 靶向中枢神经系统 •临床疗效更优 | • 需腰椎穿刺操作 |
未来方向
需开展头对头研究,直接比较不同细胞来源(如BMMNCsvsMSCs)与输注途径的疗效差异,同时优化MSCs培养工艺以降低成本,并建立>5年的长期随访体系验证治疗持久性。未来十年应聚焦临床转化,推动标准化治疗方案形成。
主要参考资料:
[1]:https://onlinelibrary.wiley.com/doi/10.1155/2013/951827
[2]:https://www.frontiersin.org/journals/bioengineering-and-biotechnology/articles/10.3389/fbioe.2022.1006845/full
[3]:Nguyen, T.L., Nguyen, H.P. & Nguyen, T.K. The effects of bone marrow mononuclear cell transplantation on the quality of life of children with cerebral palsy. Health Qual Life Outcomes 16, 164 (2018). https://doi.org/10.1186/s12955-018-0992-x
[4]:https://www.frontiersin.org/journals/pediatrics/articles/10.3389/fped.2019.00543/full
[5]:Thanh, L.N., Trung, K.N., Duy, C.V. et al. Improvement in gross motor function and muscle tone in children with cerebral palsy related to neonatal icterus: an open-label, uncontrolled clinical trial. BMC Pediatr 19, 290 (2019). https://doi.org/10.1186/s12887-019-1669-2
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信