脑瘫是一种影响产后和产前儿童的神经系统疾病,由大脑运动皮质损伤引起,可分为痉挛型、运动障碍型和混合型三种。
干细胞治疗脑瘫的安全性与有效性再评估:基于13项随机对照试验的荟萃分析
近期,国际知名干细胞杂志《Stem Cell Res Ther》发表了一项题为“评估干细胞/间质细胞移植对确诊为脑瘫儿童的安全性和有效性:随机对照试验的系统回顾和荟萃分析”的研究。该研究旨在系统评估干细胞或基质细胞疗法对脑瘫儿童的疗效和安全性[1]。

结果表明,干细胞治疗显著提高了脑瘫患儿的粗大运动功能测量(GMFM)评分,证实该疗法安全有效。
流行病学与危险因素:脑性瘫痪(Cerebral Palsy, CP)在新生儿和婴幼儿中表现出一系列异质性症状,其患病率受孕周、出生体重等因素影响,总体合并患病率约为每千名活产儿2.11例。妊娠期糖尿病(GDM)等多种因素可能与脑瘫相关,但早产仍是最重要的危险因素。

临床表现与生活影响:脑瘫涵盖偏瘫、四肢瘫痪及运动协调障碍等一系列残疾,显著降低患者生活质量,并为儿童及其照护者带来沉重心理负担。早期神经发育评估对及时发现功能障碍、延缓残疾进展至关重要。然而,部分评估方法(如4月龄前“扭动期”的全身运动观察GMs)在脑瘫早期预测方面的价值仍有限。
诊断工具与分级标准:粗大运动功能分级系统(GMFCS)将脑瘫儿童运动功能损伤分为五级,临床诊断主要依赖体格检查,现代神经影像学则有助于识别脑结构损伤。磁共振成像(MRI)可在约86%的患者中发现脑部异常,神经生物学与病理学结合有助于深入理解病因。
常规与辅助治疗:缺血缺氧性脑激活治疗(HBAT)和高压氧治疗(HBOT)可显著改善粗大运动功能测量(GMFM)评分。痉挛型脑瘫常采用A型肉毒毒素(BoNT-A)注射治疗,但重复注射需间隔不少于六个月,且多次治疗可能限制肌肉功能恢复。此外,微活检研究显示,脑瘫患儿内侧腓肠肌中的肌源前体细胞仍具分化潜力。
干细胞治疗小儿脑性瘫痪的临床研究进展
过去15年间,干细胞移植在脑瘫治疗中显示出多方面的潜在益处。其作用机制可能包括旁分泌效应及信号通路调控,从而抑制炎症、促进血管生成,并引导神经干细胞向损伤区域迁移和增殖。
体内研究表明,CD34+造血干细胞(HSCs)及CD34−细胞可能减轻脑损伤。鼻腔移植细胞红蛋白(CYGB)也可能增强人脐带源间充质干细胞(CYGB-HuMSCs)在缺氧缺血性脑损伤(HIBD)模型中的疗效。
评估干细胞/间充质干细胞移植治疗脑瘫儿童的安全性和有效性的方法
纳入标准:所有针对脑瘫患者的随机对照试验(RCT)均被纳入,不限种族、地区、性别与文化背景。主要结局指标为粗大运动功能测量(GMFM),亚组分析包括干预后3、6、12个月的效果评估,以及给药途径、干细胞类型和安全性相关不良事件。
排除标准:排除评论、动物实验、体外研究、综述、社论、书籍章节、回顾性研究、队列研究、非随机试验、数据不可用或未报告GMFM结局的文献。
表1详列检索策略与各数据库语法。图1PRISMA流程图展示文献筛选与纳入过程。最初从Embase(n=160)、Web of Science(n=669)、Scopus(n=581)和 PubMed(n=85)共检索出1064篇文章。

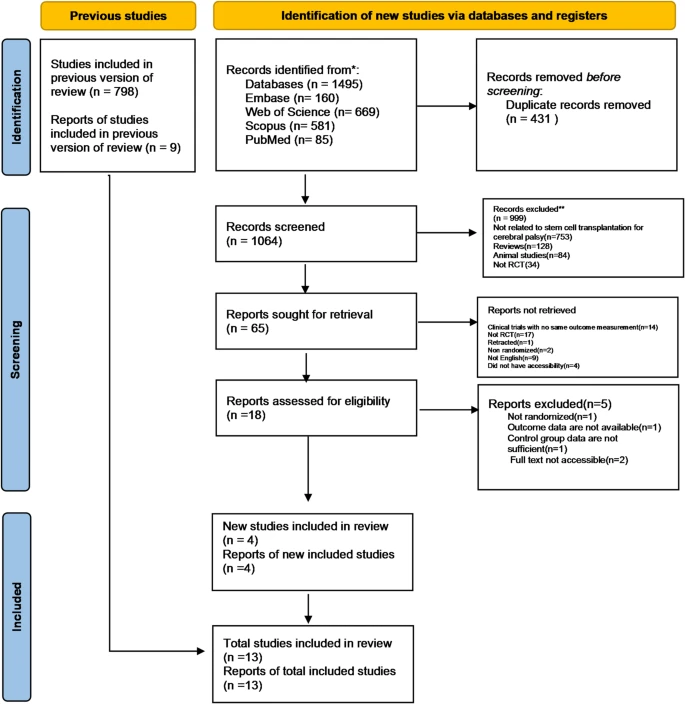
经筛选,对65项研究进行全文评估,最终排除47项。排除原因包括非RCT设计、结局指标不一致或与研究主题无关等。另有14项因数据缺失或无法获取全文被排除,最终13项研究纳入系统评价与荟萃分析。
研究特点:纳入的13项研究中,4项来自韩国,5项来自中国,2项来自伊朗,美国及美洲各1项。所有研究均为RCT,其中一项同时研究骨髓间充质干细胞(BMMSC)和骨髓单核细胞(BMMNC),另一项研究涉及同种异体脐带血和人脐带组织源间充质干细胞。各类干细胞的分析结果见表2。
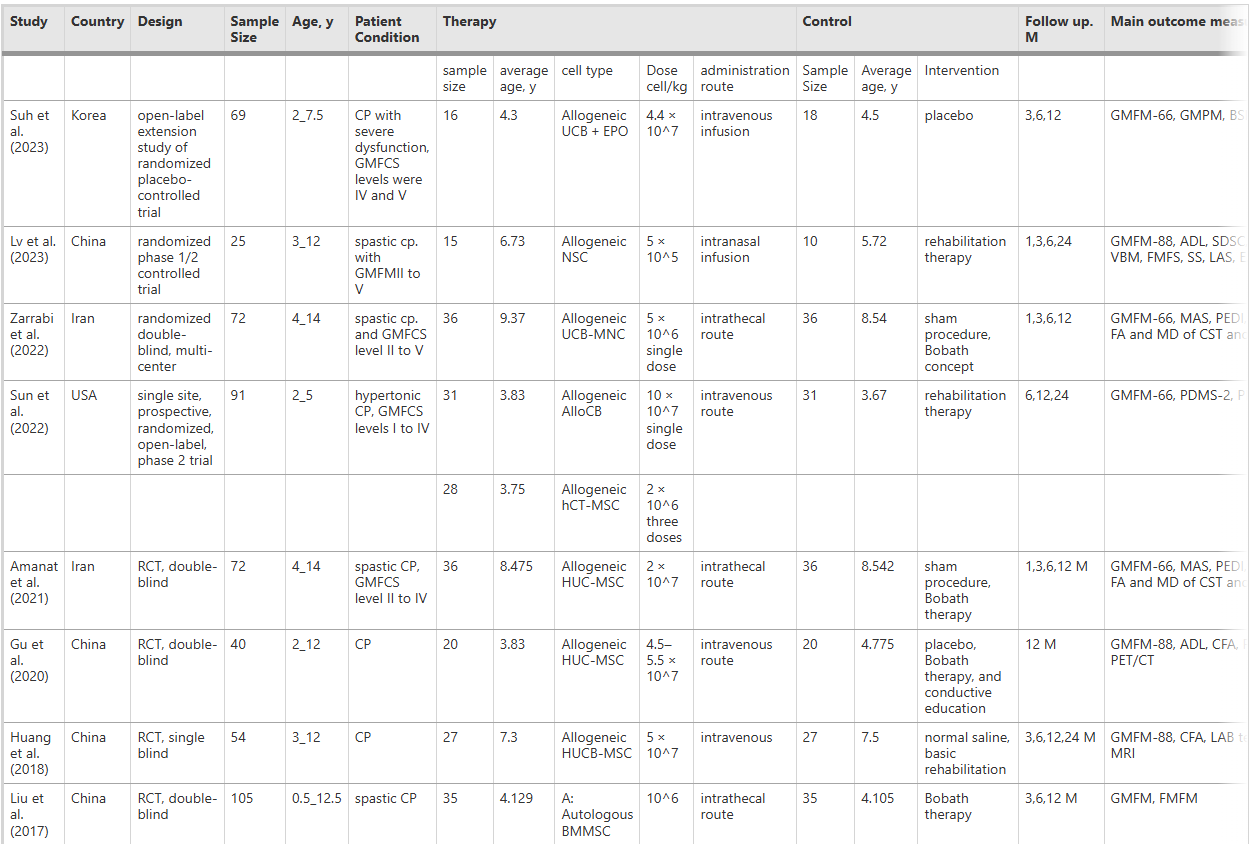
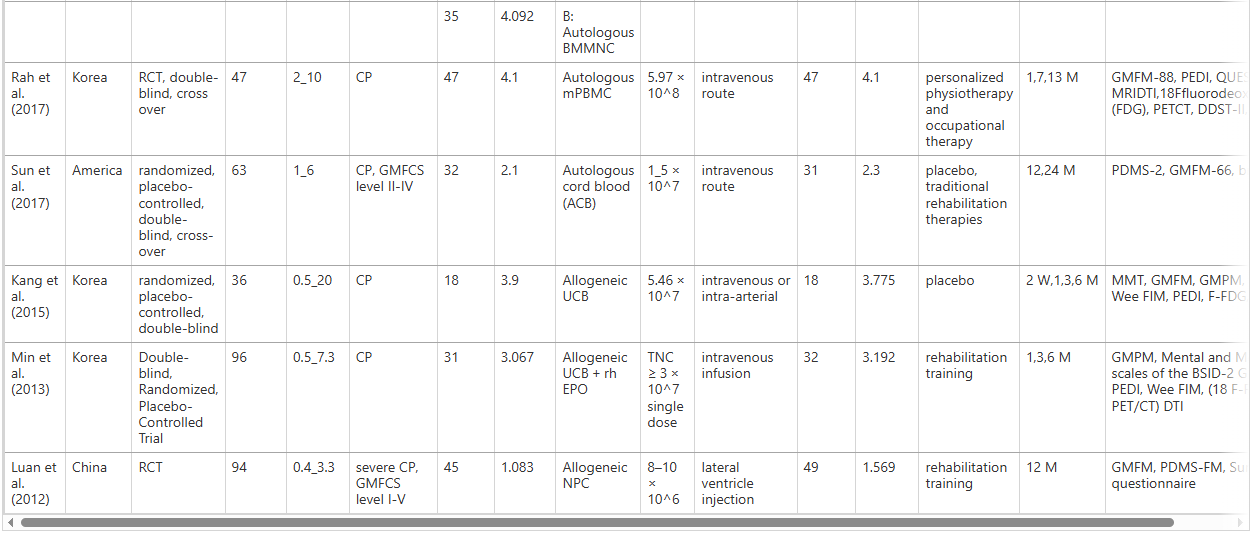
Meta分析干细胞/间质细胞移植对治疗脑瘫儿童的安全性和有效性
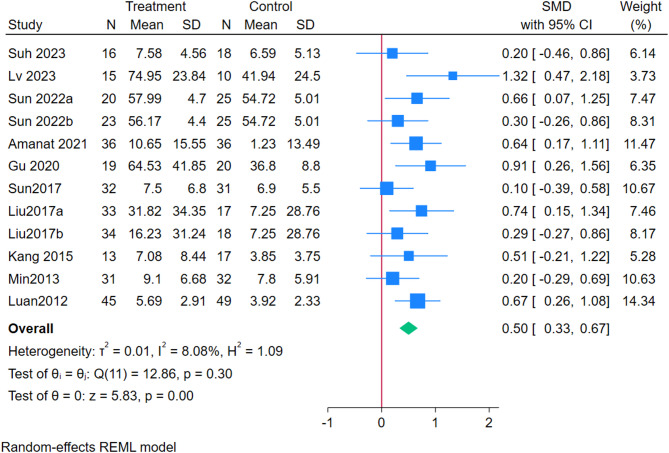
采用随机效应模型对13项研究进行Meta分析,以GMFM为主要疗效指标,不良事件为安全性指标。结果显示,干细胞治疗组疗效显著优于对照组(SMD:0.82;95%CI)(图2)。部分研究间存在显著异质性(I²=91.37%),[29]、[31]、[32]号研究为主要异质来源。经敏感性分析剔除上述文献后异质性显著降低(I²=8.08%),森林图显示SMD:0.50(95%CI [0.33,0.67])(图3)。
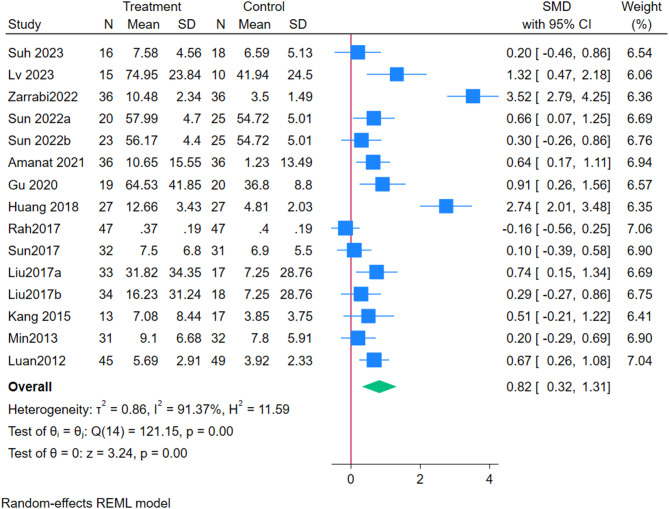
亚组分析
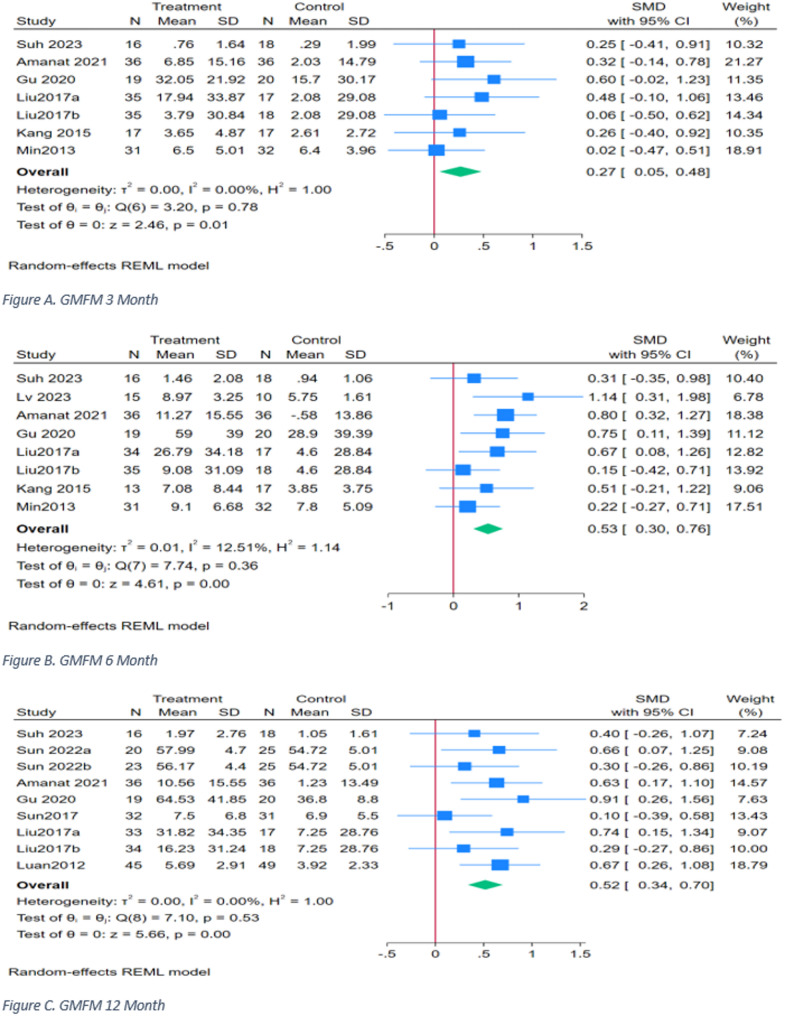
时间亚组分析:在不同随访时间点上,干细胞治疗对脑瘫儿童的粗大运动功能测量(GMFM)均显示积极效果。合并分析表明,治疗组在3个月时已有显著改善(SMD=0.27),6个月时进一步提升(SMD=0.53),并在12个月时依然保持稳定改善(SMD=0.52)。这些结果均基于随机效应模型,提示干细胞治疗在短期和中期均能带来持续的功能获益(图4)。
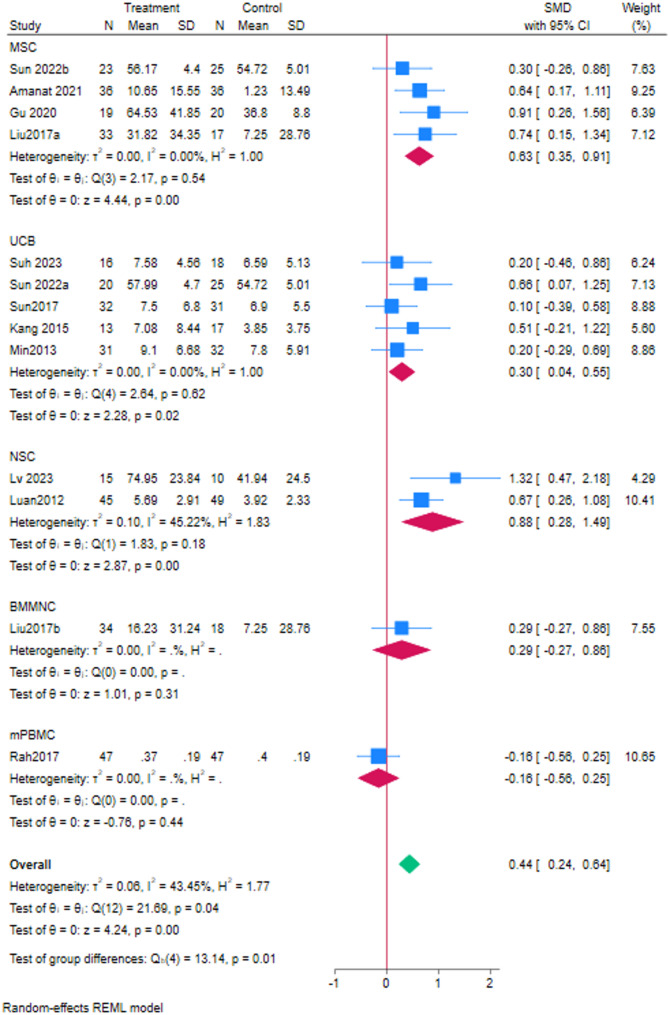
干细胞类型亚组分析:间充质干细胞(MSCs)和脐带血干细胞(UCB)是研究最广泛的类型。MSCs来源包括脐带沃顿胶和骨髓,分析显示GMFM改善显著(SMD=0.63)。UCB组同样带来功能提升(SMD=0.30)。神经干细胞(NSCs)的研究有限,但结果也显示出较强疗效(SMD=0.88)。总体来看,不同类型干细胞均能改善运动功能,其中MSCs的效果更为突出(图5)。
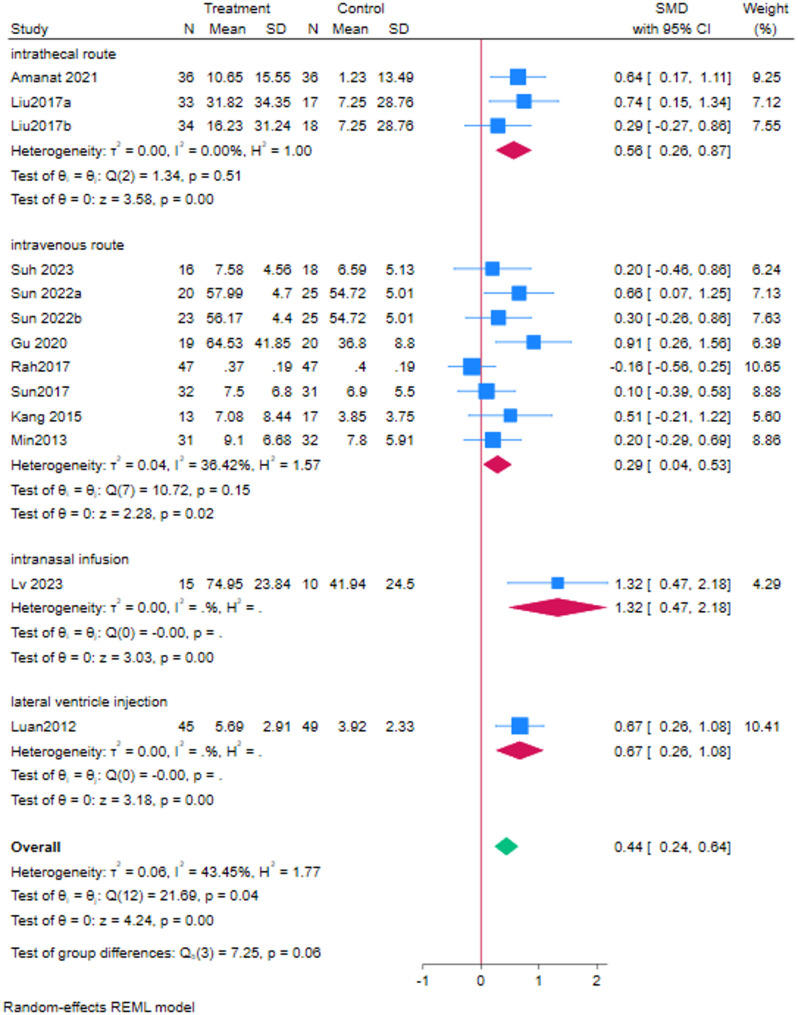
给药途径亚组分析:干细胞移植的主要途径包括鞘内注射、静脉注射、鼻腔输注及侧脑室注射。统计结果显示,鞘内注射带来的改善幅度最大(SMD=0.56),静脉途径也有积极效果(SMD=0.29)。总体汇总结果提示,不同途径的给药方式均能带来 GMFM 的显著提升,其中鞘内途径可能更具优势(图6)。
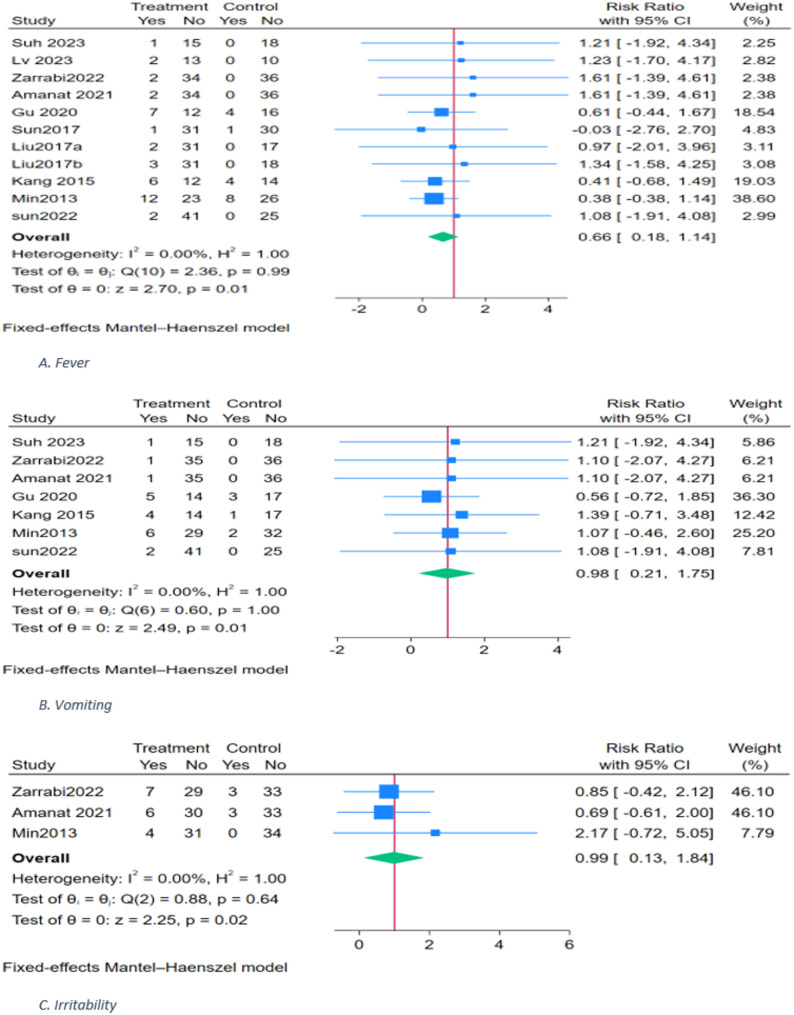
安全性分析:不良事件的评估显示,干细胞治疗总体安全。最常见的三类不良反应为发热、呕吐或恶心以及烦躁不安。亚组分析表明,这些事件在治疗组和对照组之间的发生率差异均无统计学意义(发热RR=0.66,呕吐RR=0.98,烦躁RR=0.99)。这提示干细胞移植并未显著增加治疗相关风险(图7)。
综合结论:综合各类亚组分析,干细胞治疗能够在随访3–12个月内显著改善脑瘫患儿的粗大运动功能,并在不同类型干细胞与不同给药途径中均展现出疗效。同时,安全性分析显示并未增加明显不良反应。整体结果支持干细胞作为一种潜在有效且安全的脑瘫干预手段,但仍需更多大规模、长期的随机对照试验验证。
讨论:干细胞在治疗脑损伤与脑瘫中的潜力
干细胞在脑损伤修复中展现出显著优势,如促进中风后的运动功能恢复、保护皮质脊髓束等。脐带血(UCB)和间充质干细胞(MSC)被认为是最安全的来源。自体细胞不会引发免疫排斥,而异体细胞可能触发免疫反应。研究表明,UCB细胞可减少CD4+T细胞迁入脑内,减轻炎症反应。
干细胞治疗脑瘫的主要机制
神经保护与抗炎作用:干细胞通过分泌抗炎因子(如IL-10)抑制过度炎症反应,改善脑部微环境,例如无限制体细胞干细胞(USSCs)即通过该机制发挥疗效。
免疫调节:干细胞可调节免疫细胞如CD4+ T细胞的迁移与活性,减轻免疫介导的脑组织损伤。
神经营养与神经再生支持:干细胞分泌多种神经营养因子,支持神经元存活、促进突触生长、刺激内源性神经发生和髓鞘修复,增强神经环路可塑性。
促进血管新生:通过分泌血管生成因子,干细胞改善损伤区血液供应,为神经修复提供支持。
协同增强机制:干细胞与促红细胞生成素(EPO)等因子联用可通过Wnt/β-catenin等信号通路发挥协同抗炎和神经保护效应。
综上,干细胞治疗脑瘫的核心机制为多途径协同的“细胞赋能”,通过抗炎、免疫调节、神经营养和血管新生等综合效应,激发脑内修复与可塑性,从而实现运动等功能改善。
通过影像学监测评估干细胞治疗小儿脑性瘫痪的临床价值
脑瘫的体征和残疾包括肌张力低下或运动障碍、智力障碍、癫痫和四肢瘫痪模式。出生后颅脑超声检查有助于检测潜在的脑损伤,而扩散磁共振成像 (DMRI) 可以评估受损白质的神经可塑性变化。基于扩散张量成像 (DTI) 束的QSM (定量磁化率映射) 方法在确定接受干细胞治疗的脑瘫儿童的白质改变方面发挥着至关重要的作用。
整体疗效显著
系统综述与荟萃分析表明,干细胞治疗脑瘫比对照组更有效,可显著提高粗大运动功能测量(GMFM)评分(SMD:0.50,95% CI [0.33, 0.67])。亚组分析进一步显示,在治疗后3、6、12个月,患者的运动功能均有改善,且12个月随访时效果最为显著(SMD:0.52)。这一结果在自体和异体干细胞中均得到了验证。
不同类型和给药方式
在干细胞类型方面,间充质干细胞(MSCs)疗效最为突出(SMD:0.63),来源于骨髓或脐带的MSCs均有效。脐带血(UCB)也显示积极作用(SMD:0.30)。其他如神经干细胞(NSC)、骨髓单个核细胞(BMMNC)和动员外周血单个核细胞(mPBMC)虽然研究数量有限,但整体分析仍呈现改善趋势。给药途径方面,静脉注射最常见(SMD:0.29),鞘内注射效果更佳(SMD:0.56),而经鼻或侧卧位注射的研究较少。
安全性与不良反应
安全性分析显示,干细胞治疗总体耐受性良好。主要不良事件包括发热、恶心/呕吐和易激惹,但与对照组相比差异不显著。森林图分析结果提示,干细胞移植并未显著增加不良反应风险,说明其在改善运动功能的同时具备较高安全性。
总结
研究结果表明,干细胞移植治疗脑瘫安全有效。然而,仍需开展更多采用标准化方案的高质量随机对照试验,以探究其他干细胞类型治疗脑瘫的疗效。
参考资料:[1]:Fatahi R, Heydarpour F, Motlagh SM, Mansouri K. Evaluation of stem/stromal cell transplantation safety and efficacy in children diagnosed with cerebral palsy: A systematic review and meta-analysis of randomized controlled trials. Stem Cell Res Ther. 2025 Aug 29;16(1):468. doi: 10.1186/s13287-025-04550-9. PMID: 40877893; PMCID: PMC12395659.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信