近年来,干细胞疗法,尤其是间充质干细胞(MSCs)干预策略,在肾移植受者中展现出独特的免疫调节潜能,为实现移植肾长期存活乃至免疫耐受提供了新的技术路径。与传统免疫抑制方案相比,干细胞疗法有望减轻药物相关毒性、降低感染与肿瘤发生风险,进而改善受者生活质量与卫生经济学效益。当前,该领域正从基础探索加速向临床转化迈进。
基于47项临床试验的实证:干细胞疗法或将终结肾移植后的长期“药罐子”生活
近期,《Asian Journal of Surgery》发表了一篇题为《肾移植中干细胞疗法的临床试验概况及文献计量分析》的综述。该研究整合了临床试验注册数据与文献计量学方法,系统描绘了该领域的研究现状、演进脉络与前沿趋势,以期为后续研究与临床决策提供参考[1]。

研究团队对Trialtrove数据库进行系统检索,纳入2000年1月至2025年8月间注册的干细胞在肾移植中应用的临床试验,共筛选出47项合格研究。分析指标涵盖试验的时间趋势、阶段与状态、地域分布、申办方与资助类型及作用机制。由两名研究人员独立完成数据提取与交叉核对,对非结构化信息进行标准化处理,确保数据质量。
同时,基于Web of Science核心合集数据库开展文献计量分析,检索时段为2005年1月至2025年7月,经两轮人工筛选共纳入1457篇相关文献。
趋势解析:发文量趋稳,试验渐入后期
时间序列分析显示,自2005年以来,相关出版物的数量呈快速上升趋势,并在2015年达到峰值102篇(图1A(a))。随后,年产量稳定在70至100篇之间,表明该领域的研究活动持续活跃。
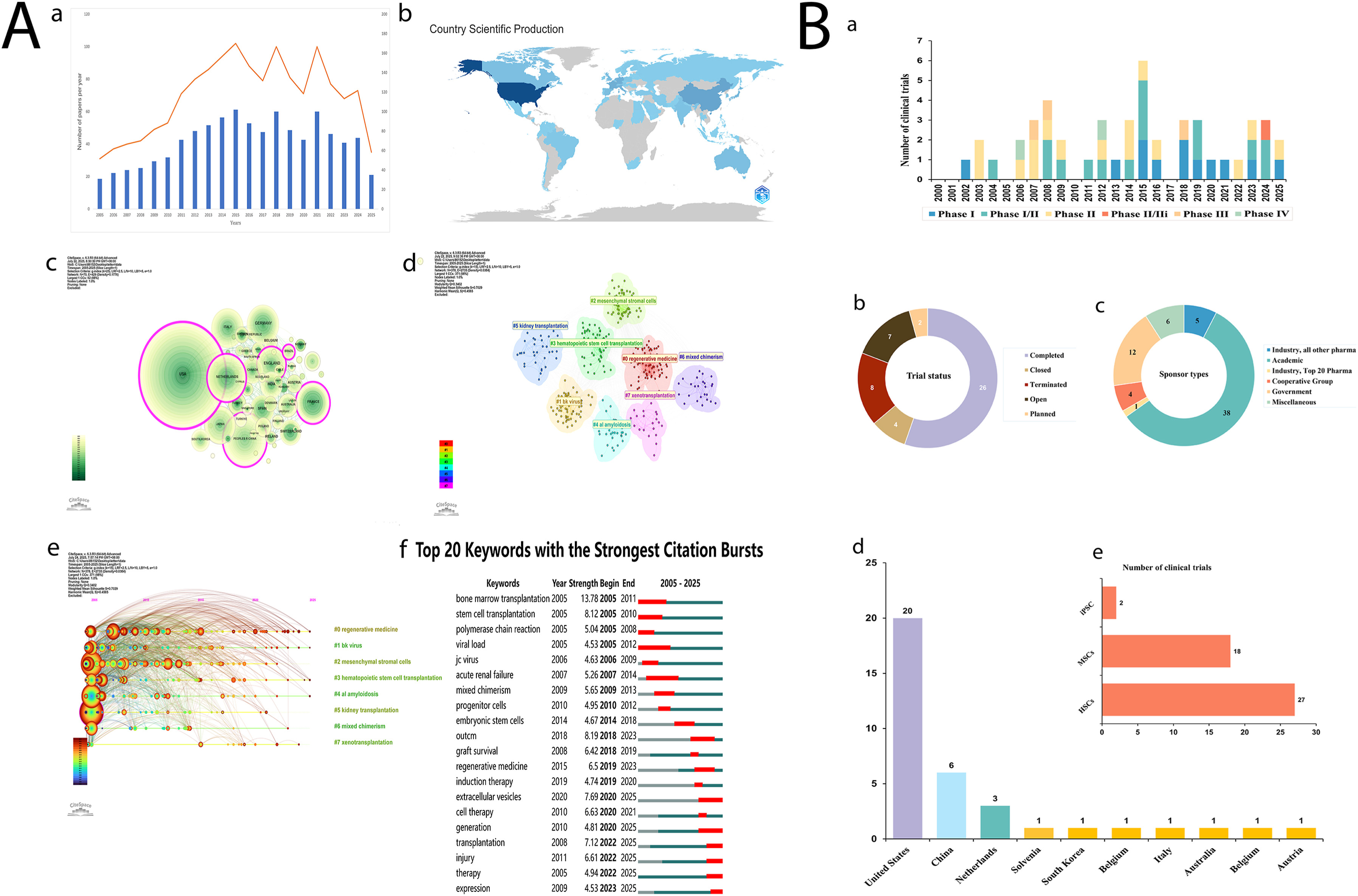
a.过去25年全球年度出版量及趋势;b.按国家/地区划分的出版物地理分布;c.出版国家/地区的分布图;d.关键词主题聚类分析;e.关键词热点的时间演变;f.新兴关键词(前20个)。(B)肾移植干细胞疗法临床试验概览。a.按启动年份划分的临床试验时间趋势;b.临床试验的试验状态分布;c.临床试验资金来源分布;d.按国家/地区划分的临床试验分布;e.干细胞疗法类别分布;
与此同时,II期至IV期临床试验的数量显著增加(图1B(a)),表明研究重点已从基础探索转向临床验证和应用。在纳入的47项试验中,超过一半(26项,55.3%)已完成(图1B(b))。研究经费主要来自学术机构(36项试验),政府资助12项试验(图1B(c))。
地域版图:美中领跑,科研基础驱动转化
地理分析显示,美国是主要的研究中心(图1A(b和c))。如图1B(d)所示,美国以20项临床试验位居榜首,其次是中国和新西兰。这表明,拥有雄厚科学基础和完善监管体系的国家更有可能推进干细胞疗法在肾移植领域的应用。就作用机制而言,造血干细胞(HSCs)应用最为广泛,已有27项临床试验涉及其在诱导免疫耐受和减少对免疫抑制药物依赖方面的应用(图1B(e))。
热点迁移:从基础免疫学到细胞治疗
关键词共现网络和时间趋势分析表明,2005年至2014年(图1A(e和f)),研究主要集中在“骨髓移植”、“混合嵌合体”和“祖细胞”等基础免疫学问题上。2015年以后,研究热点逐渐转向转化医学领域,包括“再生医学”、“胚胎干细胞”、“移植存活”和“诱导治疗”。
这表明干细胞研究已逐步从探索基础机制转向临床转化研究。尤其在2020年以后,“细胞治疗”和“细胞外囊泡”等关键词频繁出现,表明这些领域已成为当前的研究前沿。
临床进展:免疫耐受与再生修复的突破
值得关注的是,近年多项临床研究已初步验证干细胞策略的可行性与潜力。2025年,梅奥诊所领衔的一项III期临床试验显示,MDR-101方案(通过供体造血干细胞诱导免疫混合嵌合体)使多数肾移植受者在移植后成功停用常规免疫抑制药物,实现功能性免疫耐受。这一突破性进展为干细胞介导的耐受策略提供了迄今最有力的临床证据。

2025年10月,韩国开展的一项单臂研究纳入7例慢性活动性抗体介导排斥反应(cABMR)受者,接受同种异体骨髓来源间充质干细胞输注(4次,每两周1次,1×10⁶cells/kg)。结果显示,治疗后估算肾小球滤过率(eGFR)下降斜率由−16.6%减缓至−2.4%,蛋白尿减少,供体特异性抗体(HLA-DSA)平均荧光强度(MFI)降低,T细胞亚群分析提示免疫调节向保护性方向偏移。该研究首次在cABMR人群中证实MSCs不仅安全,且具备延缓功能恶化的潜力。

2024年12月,日本学者尝试将自体CD34+细胞经肾动脉分次注射于慢性进行性肾病患者(eGFR15–28 mL/min/1.73m²),结果显示月eGFR斜率由治疗前−1.36±1.1升至治疗后+0.22±0.71mL/min/1.73m²/月,肾内阻力指数与剪切波速度亦有显著改善。尽管样本量有限,该研究首次证实重复经肾动脉干细胞输注在进展性肾病中的可行性与功能改善趋势。

2024年7月,由维也纳医科大学牵头的一项国际研究探索了一种联合细胞治疗策略:在肾移植同时,向受者输注来自同一供体的骨髓细胞和自体多克隆调节性T细胞(Tregs)。
该研究证实,这种疗法能够在无需维持性三联免疫抑制治疗的情况下,选择性清除供体特异性的T细胞克隆,同时保留整体T细胞受体库的多样性,从而有效降低针对移植肾脏的免疫反应。相关成果已发表于《柳叶刀》旗下子刊eBioMedicine。这一策略为在器官移植中实现“免疫耐受”提供了新的组合范式。

前景展望:多中心协作与长期随访驱动转化
总体而言,干细胞疗法在肾移植领域的研究正稳步推进,临床试验数量持续增长,研究重点正从基础免疫机制向临床转化转移。MDR-101、MSCs治疗cABMR、CD34+细胞再生治疗及Tregs联合输注等代表性研究,初步展示了干细胞在免疫调节与组织修复中的多元应用前景。
然而,当前大多数研究仍处于早期阶段,III/IV期试验匮乏,行业参与度不足,细胞产品标准化与质控体系尚未统一,监管路径仍待明晰。此外,全球供肾短缺的现实进一步凸显了开发新型免疫调节策略以提升移植器官长期存活率的紧迫性。
展望未来,亟需推进多中心、随机对照试验,建立统一的监管与标准体系,并积累长期随访数据,以加速干细胞疗法在肾移植领域的临床转化与推广应用。
参考资料:
[1]:https://www.sciencedirect.com/science/article/pii/S1015958426004811?via%3Dihub#bib2
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信