描述:2026年《帕金森病杂志》综述揭示:从胎儿腹侧中脑多巴胺能神经元移植,到PSC(胚胎/诱导多能干细胞)衍生vmDA祖细胞临床试验,细胞疗法历经数十年演进。早期试验曾出现移植诱发性运动障碍(GID)及α-突触核蛋白病理蔓延,但后续研究明确了理想患者特征。当前全球多项I/II期试验显示短期安全性良好,但细胞存活率低(约5%)、¹⁸F-DOPA摄取未恢复正常。III期试验已启动,仍需优化剂量、递送及免疫抑制方案。
一、帕金森病与细胞疗法的逻辑
帕金森病(PD)是一种常见的神经退行性疾病。其病理特征有二:一是路易小体与路易神经突中α-突触核蛋白的异常积聚;二是黑质腹侧中脑多巴胺能(vmDA)神经元的进行性凋亡。后者负责调控运动机能,其丧失直接导致了震颤、僵硬与动作迟缓等典型运动障碍。
病程早期,上述症状通常可被药物有效控制。然而,随着病情进展,药效逐渐下降,并可能诱发严重副作用。多巴胺细胞疗法应运而生,通过向脑内移植外源性神经元,以替代丧失的vmDA神经元,成为极具前景的治疗策略。该领域历经数十年探索,从最初采用胎儿组织来源的多巴胺细胞,发展到近年利用干细胞制备的多巴胺细胞并进入临床试验,取得了长足进步。但与此同时,该疗法也易滋生误解。
在此背景下,2026年4月17日,国际知名期刊《帕金森病杂志》(Journal of Parkinson’s Disease)发表了一篇题为“干细胞治疗与帕金森病:科学与误解”的研究综述[1]。
本文旨在回顾该疗法的演进历程(过去、现在与未来),在辨析常见误解的基础上,建立合理预期,凸显其真正潜力,以增强学界与公众的信心与乐观态度,并对帕金森病多巴胺细胞疗法的现状做出批判性总结。
二、过去:胎儿组织移植——从希望到局限
2.1 早期探索与成功信号
早在20世纪80年代,科学家将大鼠胚胎腹侧中脑多巴胺能(hfVM)神经元移植到帕金森病模型大鼠中,移植物存活、释放多巴胺、改善运动障碍。随后的人源hfVM移植在开放标签试验中取得了令人振奋的结果:部分患者运动评分显著改善,甚至可停用多巴胺能药物。
2.2 双盲试验的冷水
然而,20世纪90年代美国国立卫生研究院资助的两项双盲安慰剂对照试验泼了冷水。疗效个体差异大,且15%至56%的患者出现了移植诱发性运动障碍(GID),部分严重到需要深部脑刺激手术来控制。
原因何在?后来分析发现,胎儿组织中混杂了血清素能神经元,它们释放的5-羟色胺可能是GID的元凶。此外,尸检报告显示,移植多年的神经元内出现了α-突触核蛋白阳性的路易小体——帕金森病的病理可以“蔓延”到移植细胞。但需要指出,这种蔓延非常缓慢(最长存活24年的病例中,绝大多数vmDA神经元仍然健康),所以“疗法必然失败”的说法并不准确。
2.3 重新评估与患者选择
后续研究认识到帕金森病的异质性:早期、年轻、对左旋多巴反应良好、下游神经环路完整的患者,移植效果远优于晚期患者。这是因为他们的脑内还保留着较好的“土壤”,移植的“种子”更容易扎根整合。
但胎儿组织移植有一个根本性死结:来源不可持续。治疗一个患者需要4-5个胎脑,无法标准化生产。TRANSEURO研究中,87例计划手术因组织短缺而取消。这直接推动了干细胞衍生移植的崛起。
三、当下:干细胞移植——从分化到临床
多能干细胞(PSC)的类型、特性与选择困境:PSC具有无限自我更新和分化为任何细胞类型(包括腹侧中脑多巴胺能神经元)两大核心特性,主要包括胚胎干细胞(ESC)和诱导多能干细胞(iPSC)。ESC来源于囊胚期内细胞团,在部分司法管辖区存在伦理争议;而iPSC通过强制表达多能性转录因子(Oct3/4, Sox2, Klf4, c-Myc)对体细胞进行重编程产生,规避了伦理问题,且可实现自体移植从而避免免疫排斥。
然而,iPSC重编程可能增加遗传或表观遗传异常的风险。目前学界尚未就使用ESC还是iPSC达成共识,因此在正在进行的临床试验中,两者均被用于衍生腹侧中脑多巴胺能神经元。
分化方案的演进——从早期失败到关键突破:早期分化尝试通过形成表达PAX6的神经中间体(如拟胚体或共培养)产生多巴胺能神经元,但这些细胞并非特异性的腹侧中脑类型,移植到6-羟基多巴胺损伤的啮齿动物后存活率差、运动改善微弱。
关键突破在于发现真正的腹侧中脑多巴胺能神经元起源于表达FOXA2和LMX1的神经中间体,据此开发了新方案:双重抑制SMAD信号通路(TGF-β和BMP),同时激活SHH和经典WNT信号通路,并添加适当生长因子。由此分化的神经元在动物模型中存活率和功能显著优于早期方案。后续研究进一步优化了生长因子的时机与浓度,并引入流式分选技术,使方案日趋成熟。
临床转化的安全性质疑、控制措施与初步试验结果:上述方案已按良好生产规范(GMP)标准改进,推动了PSC衍生的vmDA祖细胞进入早期临床试验。然而,最大隐忧在于:即使移植极少量未分化的PSC,也可能导致畸胎瘤形成。研究表明,含有1%未分化人ESC的移植物即可在免疫缺陷小鼠中致瘤。但通过严格的临床前测试与质量控制(如确保未分化细胞比例低于0.1%),可达到安全标准。目前全球至少1200名患者接受了基于PSC的细胞疗法移植,迄今未见肿瘤形成报告。
2020年,首例PSC来源的vmDA祖细胞移植患者病例报告发表。该患者接受的是自体iPSC来源的vmDA祖细胞移植。尽管¹⁸F-DOPA摄取和临床运动评分有所改善,但最显著的改善体现在生活质量上——患者自述生活质量显著提高。然而,因仅治疗一名患者,这些结果无法推广,凸显了开展涉及多名患者的早期临床试验的必要性。
此后,美国、中国、欧洲和亚洲各地开展了多项类似试验(见表1),包括由英国剑桥大学与瑞典隆德大学联合开展的STEM-PD试验。截至撰稿时,其中三项试验的结果已发表于同行评审期刊。



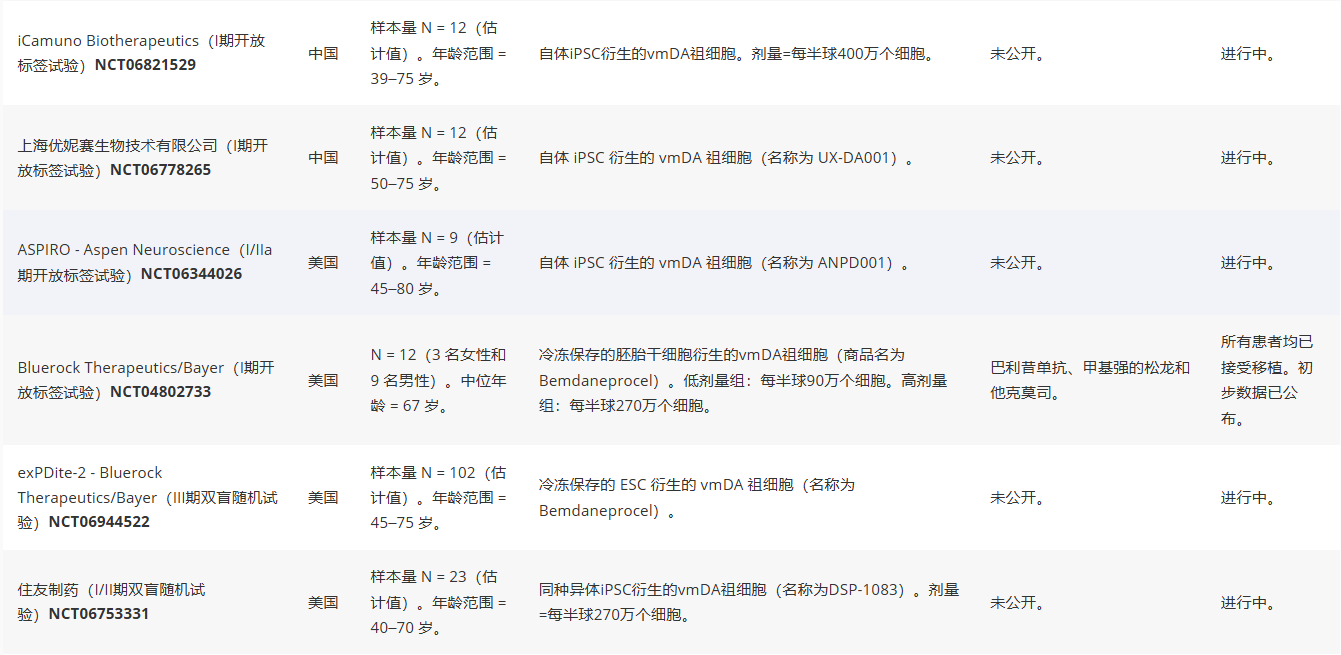
日本的一项I/II期开放标签试验中,患者接受了低剂量或高剂量的同种异体iPSC衍生vmDA祖细胞移植。所有患者均未观察到异常生长、肿瘤形成或GID。后者与早期hfVM试验中5-HT神经元污染导致GID的假设相符。然而,鉴于随访期相对较短,长期安全性尚不能完全排除。PET成像显示,所有患者的¹⁸F-DOPA摄取量均有轻微增加,高剂量组更为显著。但高剂量组的绝对¹⁸F-DOPA摄取值低于低剂量组,且两组的摄取值均远低于健康个体水平。
这表明,移植后存活并成熟为功能性多巴胺能神经元的祖细胞数量,远未达到完全修复神经网络所需的数量。耐人寻味的是,这与TRANSEURO试验的结果相似——后者同样存在个体差异,但临床运动评分改善最大的患者,其¹⁸F-DOPA摄取值已恢复至与健康对照组相当的水平。
为补充上述试验,美国(Bluerock Therapeutics/Bayer)与韩国分别开展了两项I/IIa期开放标签试验。患者接受了低剂量或高剂量hESC衍生的vmDA祖细胞移植。与日本试验类似:未见异常生长、肿瘤或GID,短期安全性良好;临床运动评分适度改善,提示潜在疗效,但PET显像中¹⁸F-DOPA摄取量仍未恢复正常。
需要审慎指出,上述三项试验均存在局限性:样本量小、缺乏对照组、开放标签设计(患者与研究者均知晓所接受的治疗)。因此,其疗效数据可能受到安慰剂效应和/或观察者偏倚的影响,须谨慎解读。尽管如此,短期安全性数据已使监管机构有信心批准更大规模的临床试验。
事实上,Bluerock Therapeutics/Bayer已于2025年9月启动一项III期随机、假手术对照、双盲试验。该试验规模远超此前的I/II期试验,旨在更严格地评估hESC衍生vmDA祖细胞移植的疗效,并期望在获得积极结果后最终取得上市许可。同样,日本试验的更大规模后续研究也正在筹划之中。
四、未来:攻坚克难——从存活率到非运动症状
尽管III期已启动,部分学者认为为时过早——因为此前试验中,尚无患者实现PET摄取正常化、PD药物减量或运动评分显著改善。因此,在开展大规模决定性试验前,需先在小规模研究中优化以下几个核心问题(图1):
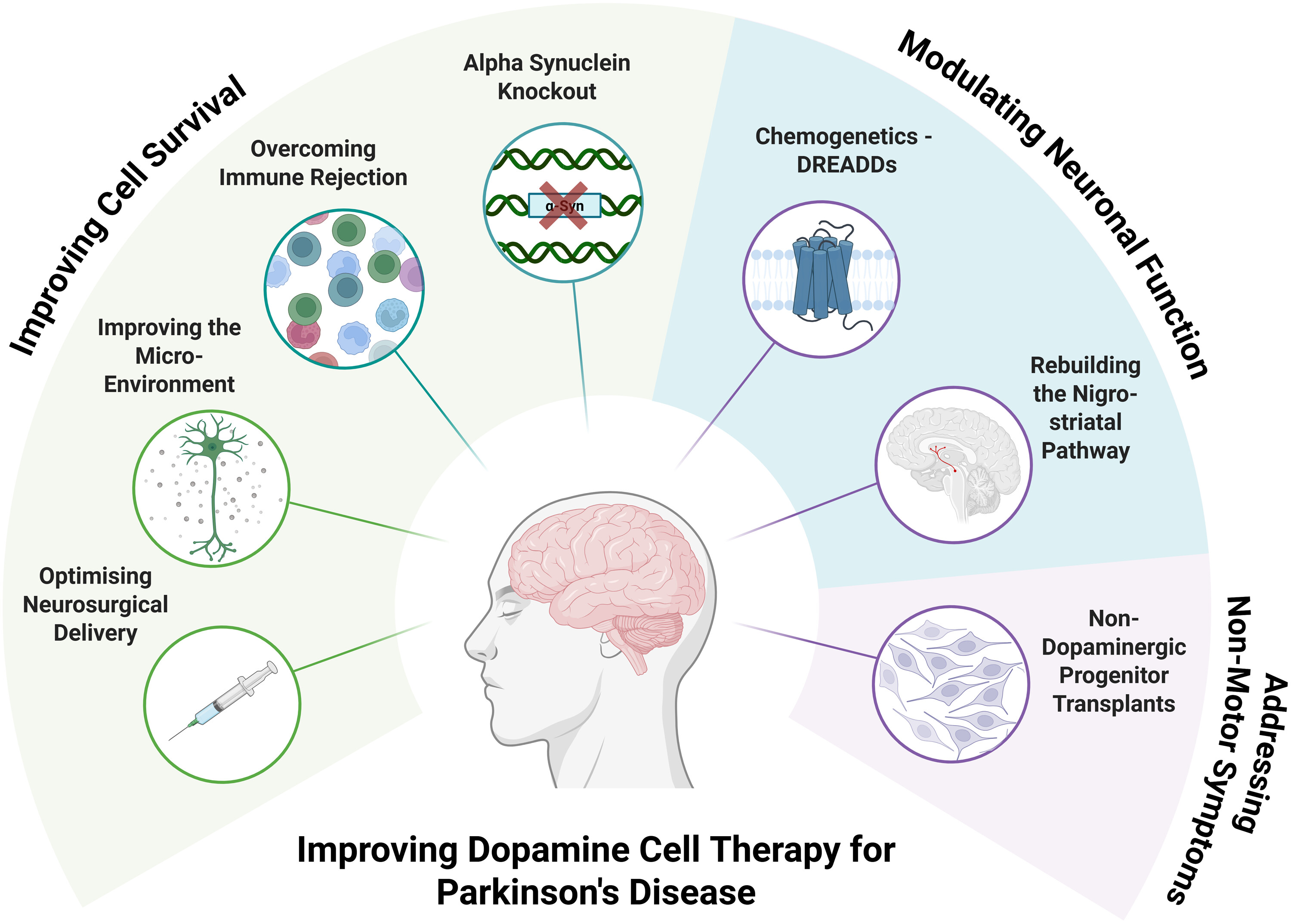
4.1 提高祖细胞存活率
目前估计移植后存活率仅约5%。增加初始剂量需要更多次脑内穿刺,每次增加约1%的血管损伤风险。亟需单次穿刺、防回流的新型注射器械。
成年大脑缺乏足够的神经营养支持。补充GDNF可提高存活率,但会降低细胞成熟度,需要优化时机;TNF-α抑制剂阿达木单抗也被证明可改善存活。
4.2 解决免疫排斥
避免免疫抑制的三种策略:
- 自体iPSC:耗时、昂贵,无法规避散发性PD风险。
- HLA匹配库:如英国需要约150条细胞系才能覆盖大部分人群,成本高昂。
- 低免疫原性PSC:敲除HLA并过表达CD47。但CD47可能使恶性细胞逃避免疫监视,需引入安全开关。
4.3 调节神经元活动——化学遗传学(DREADDs)
直接移植到纹状体无法重建上游黑质-纹状体环路。移植到黑质可重建,但需要长距离轴突生长(可用靶向直流电刺激引导)。
更前沿的策略是化学遗传学:在移植细胞中导入工程化受体(如对氯氮平-N-氧化物CNO反应的Gq偶联受体),可通过外部给药诱导去极化、增强多巴胺释放,改善运动功能。同时可用[¹¹C]CNO-PET可视化表达DREADD的神经元。但基因导入存在突变风险,同样需要安全开关。
4.4 解决非运动症状
当前疗法仅改善部分运动症状,对认知缺陷、痴呆等非运动症状收效甚微,因为这些症状源于非多巴胺能神经元(如基底前脑胆碱能神经元)的退化。未来方向是联合移植互补细胞类型——例如补充胆碱能神经元,以全面改善生活质量。
五、常见误解与事实澄清
| 误解 | 事实 |
|---|---|
| “胎儿移植试验完全失败” | 部分患者确实获益显著,但GID和病理蔓延问题限制了应用;且患者选择不当是重要原因 |
| “帕金森病病理会迅速摧毁移植细胞” | 病理蔓延极其缓慢(数年至数十年),绝大多数移植细胞长期存活 |
| “干细胞移植会致癌” | 严格质控(未分化细胞<0.1%)下,全球1200例患者尚无肿瘤报告 |
| “移植后就能根治帕金森病” | 目前仅旨在修复运动回路、缓解症状,无法阻止非多巴胺能系统的退化 |
| “所有患者都适合细胞移植” | 早期、年轻、左旋多巴反应好的患者效果最佳;晚期患者受益有限 |
六、总结与展望
从胎儿组织到多能干细胞,帕金森病多巴胺细胞疗法走过了数十年跌宕起伏的历程。早期试验的挫折促使我们更深入地理解患者选择、细胞纯度、存活率等问题;当前早期临床试验证实了短期安全性,但疗效依然有限,PET显示多巴胺能信号远未恢复正常。
未来的突破依赖于多学科协作:优化细胞存活(新型器械、生长因子联合)、解决免疫排斥(低免疫原性PSC)、重建完整环路(化学遗传学、轴突引导)、以及联合移植治疗非运动症状。
III期试验已经启动,但在此之前,我们仍需以迭代方式开展小规模优化研究,避免重蹈“过早开展大规模试验导致失败”的覆辙。正如综述作者所言:正视并克服当前方法的不足,才能防止多巴胺细胞疗法再度被弃。
七、常见问题解答(FAQ)
参考资料:
[1]:Stamper A, Bulstrode H, Barker RA. Stem cell treatments and Parkinson’s disease: Science and misconceptions. Journal of Parkinson’s Disease. 2026;0(0). doi:10.1177/1877718X261434672
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信