Meta描述:2026年4月6日,上海爱萨尔获全国首张干细胞《药品生产许可证》(沪20260315),其膝骨关节炎干细胞注射液已进入临床III期,预计2027-2028年获批上市。本文解读首证意义、818号令影响及产业格局。
核心速览
| 获证企业 | 上海爱萨尔生物医药股份有限公司 |
| 许可证编号 | 沪20260315 |
| 核发日期 | 2026年4月6日 |
| 生产范围 | IxCell hUC-MSC-O注射液(仅限注册申报使用) |
| 核心产品适应症 | 膝骨关节炎(国内首个进入临床III期的干细胞药品) |
| 预计上市时间 | 2027-2028年 |
| 政策背景 | 国务院818号令将于2026年5月1日正式实施 |
2026年首张干细胞生产许可证落沪,治膝盖的干细胞新药离上市只差最后一步
2026年4月6日,上海市药监局正式核发今年全国首张干细胞《药品生产许可证》,上海爱萨尔生物医药股份有限公司成为新年首位获证企业,许可证编号为沪20260315。许可信息显示,其生产范围包括治疗用生物制品:IxCell hUC-MSC-O注射液(仅限注册申报使用)。
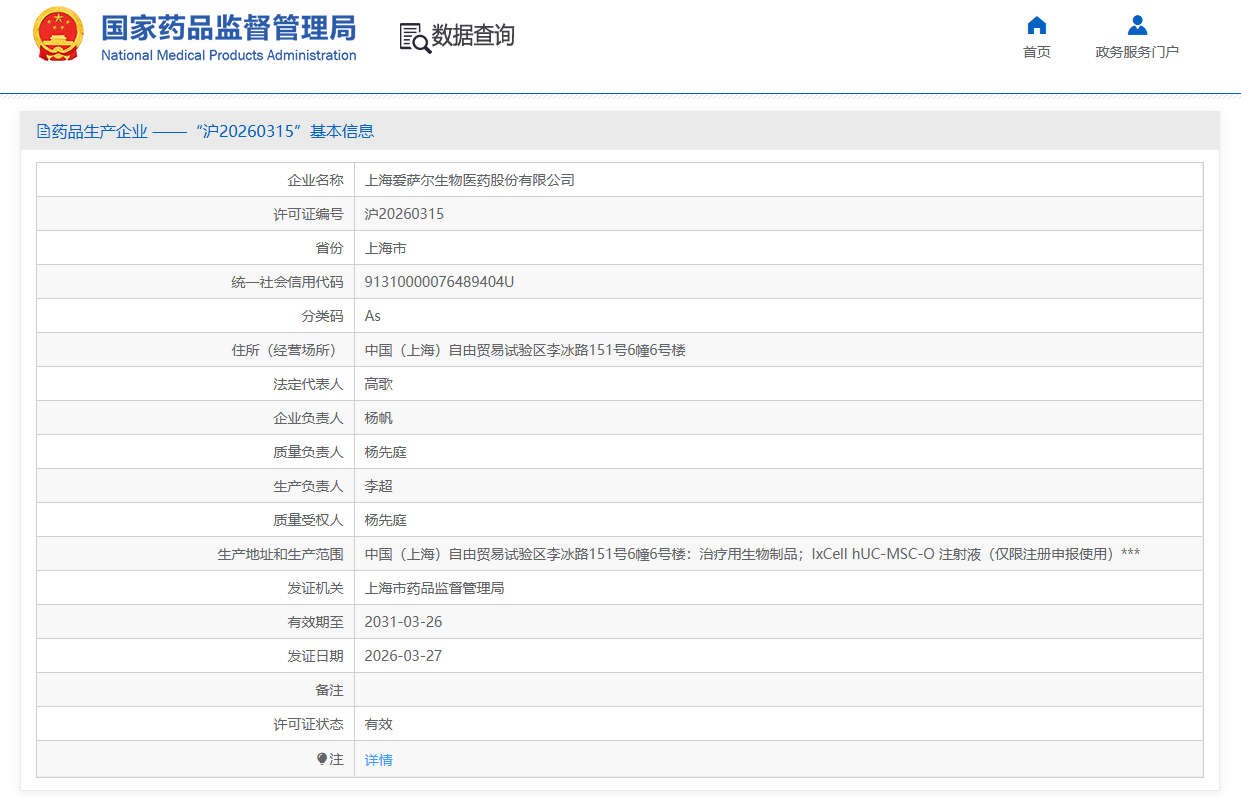
这张许可证的核发,距离国务院818号令(《生物医学新技术临床研究和临床转化应用管理条例》)2026年5月1日正式实施尚不足一个月,是中国干细胞产业从“科研备案时代”跨入“药品生产时代”的标志性事件。
一、首证之“首”:一张许可证意味着什么?
干细胞领域的监管,长期处于一种尴尬的灰色地带。过去十几年,干细胞治疗更像一个“江湖传说”——你在网上搜索“干细胞”,跳出来的大多是“返老还童”“包治百病”之类的营销话术。真正能拿到国家药监局认可、可以按药品来生产的,几乎没有。
为什么?因为监管体系一直未能完成从“科研管理”到“药品监管”的过渡。以前你可以在实验室里做干细胞,可以在医院里用干细胞做研究,但你不能像生产药片一样,在符合GMP标准的车间里批量生产干细胞注射液,然后面向患者销售。因为没证。
生产许可证,是药品上市的最后一道“准生证”门槛。它意味着企业已经通过了药品监管部门对生产条件的全面核查,具备了符合《药品生产质量管理规范》(GMP)的商业化生产能力。对于干细胞这种“活的药物”而言,生产环节的质量控制远比化学药复杂——从供者材料的采集、运输,到细胞在实验室中的分离、培养、扩增,再到成品冻存、复苏、放行,任何一个环节出现偏差,都可能影响最终产品的安全性和有效性。
正因如此,国家药监局核查中心于2026年1月发布的《细胞治疗产品生产检查指南》明确要求,细胞治疗产品的生产全过程必须实现数据可追溯、质量可管控。
爱萨尔能够成为“2026年全国首张”或“上海市首张”干细胞《药品生产许可证》获证的企业,意味着其生产体系已经通过了这一极其严苛的审查。这不仅是企业自身的里程碑,也是整个行业的一个信号:干细胞终于被当作“药品”来管了。
二、爱萨尔是谁?为什么是它?
说实话,如果不是这张证,很多人没听过爱萨尔。
它2013年在张江成立,创始团队从哈佛、耶鲁回来。头三年基本在“烧钱积累”——做iPSC分化技术、建干细胞扩增平台。那时候国内干细胞赛道还很冷,资本不看好,政策也不明朗。
转机出现在2016年底。国家药监局明确:细胞治疗产品可以按药品申报。爱萨尔是第一批反应过来的人。公司核心团队甚至参与了国内首个细胞药品指导原则的制定——这意味着他们从一开始就知道“游戏规则”怎么写。
目前爱萨尔手里最有价值的产品,是治疗膝骨关节炎的间充质干细胞注射液。
核心产品管线方面,爱萨尔覆盖了间充质干细胞(MSC)、诱导多能干细胞(iPSC)和免疫细胞三大领域,在研管线涵盖膝骨关节炎、脑卒中、肺纤维化、风湿免疫及实体瘤等多个重大疾病领域。具体而言:
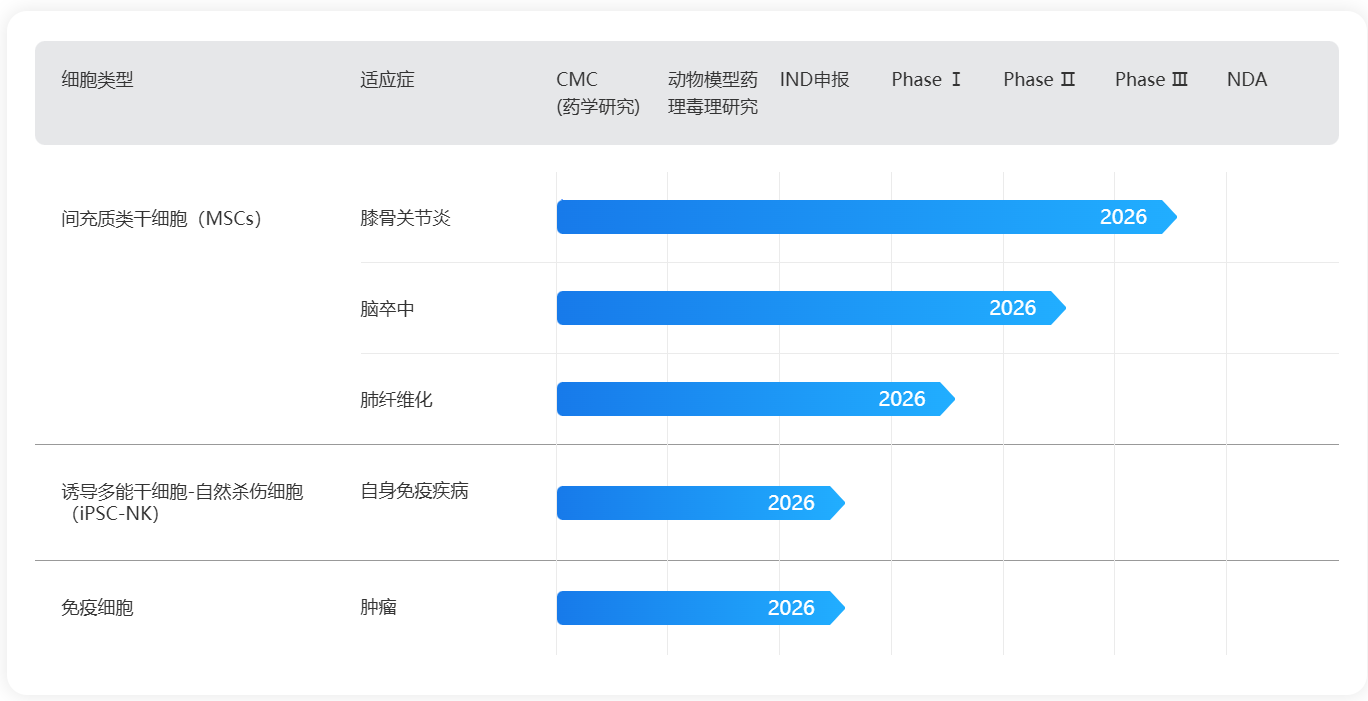
- 膝骨关节炎:间充质干细胞药品是国内首批获得临床试验默示许可的在研干细胞产品,也是目前国内首个进入临床III期的在研干细胞药品。目前该产品的III期临床试验以上海交通大学附属第九人民医院为组长单位,联合首都医科大学附属北京潞河医院、南方医科大学南方医院、深圳市人民医院、广州市第一人民医院、西安市红会医院、北京医院等多家三甲医院共同推进。
- 脑卒中:间充质干细胞治疗缺血性脑卒中已进入I期临床试验,由首都医科大学宣武医院牵头。
- 肺纤维化:间充质干细胞治疗结缔组织病相关间质性肺病处于临床前研发阶段,已完成IND申报准备。
- iPSC-NK治疗自身免疫疾病:利用诱导多能干细胞来源的自然杀伤细胞,通过清除致病性T细胞实现免疫调节,处于临床前阶段。
- 免疫细胞治疗肿瘤:来源于肝癌患者的混合免疫细胞(包括γδT细胞、NK细胞和iNKT细胞)产品,具备肝归巢和肝驻留能力,处于临床前阶段。
截至目前,公司已获得细胞治疗相关发明专利40余项,在张江建立了集研发和生产为一体的4000平方米细胞药品产业化基地,获得了国家高新技术企业、上海市专精特新中小企业等荣誉资质。
资本方面:2025年8月,上市公司吉贝尔联合华瓯创投、瓴真基金等机构共同参与了爱萨尔的新一轮融资,通过押注不同适应症与技术路径的干细胞疗法,抢占行业即将到来的商业化红利。
产业化布局方面:2026年3月,爱萨尔与南昌高新区正式签约,落地“细胞技术全景化研发与产业化基地”项目。项目分两期实施:一期重点建设干细胞治疗、免疫细胞治疗研发管线,同步搭建临床级别培养基开发平台及干细胞药品生产销售中心;二期规划建设细胞治疗产品专业化生产基地,进一步扩大产能。
临床转化应用方面:2025年4月,爱萨尔与海南帝湾医院、瑞金医院海南医院合作,在海南博鳌乐城国际医疗旅游先行区成功获批并完成了国内首例合规收费的人脐带间充质干细胞治疗膝骨关节炎临床转化应用。该项目以3%的通过率获批,采用膝关节腔内注射的货架药品(复苏即用),标志着中国细胞药物产业在合规收费临床应用方面迈出了关键一步。
三、818号令是什么?为什么大家都在提?
国务院第818号令,全称《生物医学新技术临床研究和临床转化应用管理条例》,2025年9月通过,2026年5月1日正式实施。
简单说,这部法规解决了干细胞行业最大的问题:谁来管?怎么管?
过去,干细胞监管是“九龙治水”——卫健委管临床研究,药监局管药品审批,科技部管科研项目,但谁都没有真正管住那些市场化的乱象。818号令明确了几件事:
第一,以后做干细胞临床研究,必须在三甲医院,而且要通过伦理委员会和学术委员会的双重评审。
第二,所有临床研究要向国家卫健委备案,卫健委有权随时叫停。
第三,如果想按药品上市,就走药监局的药品注册路径;如果是个性化治疗,走卫健委的医疗技术路径。
这就是业内常说的“双轨制”。
爱萨尔这张生产许可证,是药品路径上的一个重要节点。它恰好赶在818号令正式实施前不到一个月发出来,时间点很微妙——既像是给新规“献礼”,又像是在抢跑。因为一旦新规全面落地,审批流程可能会更复杂。现在拿证,等于提前锁定了合规身份。
四、行业格局:谁在领跑?谁能突围?
爱萨尔不是一个人在战斗。在干细胞药物研发的赛道上,中国的“第一梯队”已经初步成型。
从整体数据来看,截至2025年底,全国已有超过200款干细胞药物临床试验申请获得受理,其中超过150款已获准开展临床试验。地域格局上,上海、北京与广东构成了第一梯队,三地合计受理数量占据全国半数以上。2026年以来,干细胞新药研发呈现持续活跃态势——普华赛尔生物、生创科技等企业的多个干细胞产品相继获得临床试验批件。
在进入临床III期的干细胞产品方面,中国目前至少有6个产品已经进入这一冲刺阶段,爱萨尔是其中走得最靠前的之一。按照研发进度,这批产品有望在2026-2027年间陆续获批,形成国内干细胞治疗的首个上市高潮。
在国际竞争格局方面,美国的FDA通过“再生医学先进疗法(RMAT)”通道和“国家优先券”试点机制,部分药品审评周期已压缩至55天。日本则通过独特的“双轨制”监管框架,于2025-2026年推动全球首批iPSC疗法逼近商业化落地。与美日相比,中国的“双轨制”监管体系虽已成型,但在审评效率、实施细则以及供应链自主可控等方面仍需进一步完善。
据共研产业研究院预测,2026年中国干细胞药物研发市场规模将达114.91亿元,同比增长17.8%,商业化进程正全面提速。全球细胞疗法市场预计在2032年将达到1135.3亿美元,年复合增长率高达23.17%。
五、患者什么时候能用上?
从拿到生产许可证到药品正式上市,中间还需要通过NDA(新药上市申请)审批——这是一个药品从“可以生产”到“可以销售”的最终关口。以爱萨尔目前膝骨关节炎III期临床试验的推进速度来看,乐观估计在2027年到2028年,这款产品有望获批上市。
价格方面,短期内不要指望便宜。细胞药物的生产成本极高——每一批次的干细胞注射液都需要从供者材料采集开始,经过严格的质量控制、低温运输、细胞扩增、成品检测等一系列流程,且每一批次的产品都具有高度的个体化属性或复杂的质控要求。类比已经上市的CAR-T细胞疗法(价格普遍在百万元级别),干细胞药物虽然生产成本略低,但在上市初期,每针的价格大概率在数万元到十几万元之间。医保短期内不会覆盖,这符合新药上市的一般规律——先让有刚性需求且支付能力较强的患者用上,再随着工艺优化、规模化生产和竞争加剧,逐步降低价格、扩大可及性。
值得关注的是,爱萨尔的产品已经在海南博鳌乐城完成了首例合规收费的临床转化应用,说明在某些特殊政策区域,符合条件的患者已经可以提前使用。随着更多产品获批和更多地区的政策放开,干细胞药物的可及性将逐步提高。

六、一点判断
中国干细胞产业喊了十几年“春天来了”,但春天一直没有真正到来。以往每一次所谓的“政策利好”,带来的往往是概念股的一时躁动和行业内的鱼龙混杂——各种打着“干细胞治疗”旗号的民营机构遍地开花,患者花了数十万,打的却可能是没有经过严格质量控制的“不明液体”。
但2026年这个4月,情况可能真的不同了。2026年首张生产许可证的核发,加上即将正式实施的818号令,意味着干细胞终于有了一个清晰的“游戏规则”——不再是灰色地带的野蛮生长,而是有法可依、有证可查、有责可追。 当然,从拿证到产品真正进医院、进医保,还有很长的路要走。但方向已经明确,路也铺好了第一段。
接下来,我们关注两件事:一是爱萨尔膝骨关节炎药物的NDA审批结果何时落地;二是2026年的第二张、第三张干细胞生产许可证会发给谁,又有哪些适应症的产品能够走到终点。
这个赛道,终于开始变得有趣了。
七、常见问题解答(FAQ)
参考资料:(以上信息综合自上海市药监局公开信息、爱萨尔生物官网、证券时报、中国高新网、国家药监局核查中心指南、共研产业研究院报告等。全国首张干细胞生产许可证于2024年由北京铂生卓越获得。)
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信