Meta描述:神经干细胞(NSC)与间充质干细胞(MSC)如何协同促进神经再生?本文基于《细胞》杂志最新综述,系统解析NSC与MSC的生物学特性、相互作用机制(Notch信号、旁分泌)、联合移植策略及临床转化挑战,附对比表格与未来方向。
引言:神经再生的挑战与干细胞联合策略
神经系统疾病和损伤(如脑卒中、帕金森病、脊髓损伤)是再生医学领域最难攻克的堡垒之一。成年中枢神经系统(CNS)内源性修复能力极其有限,主要因为:
- 神经干细胞(NSC)数量稀少且多处于静息状态
- 损伤后微环境充满炎症因子和抑制再生的分子
- 成熟神经元无法分裂替代
干细胞移植为神经再生带来了希望。其中,神经干细胞(NSC) 因其能够分化为功能性神经元和胶质细胞,被视为最直接的细胞替代来源;而间充质干细胞(MSC) 则凭借免疫调节、旁分泌支持和低免疫原性,成为改善损伤微环境的理想辅助细胞。
神经干细胞(NSC)与间充质干细胞(MSC)协同治疗神经系统疾病:机制、策略与前景(2025年综述解读)
近期,国际期刊杂志《细胞》发表了一篇神经干细胞 (NSC) 和间充质干细胞 (MSC) 的相互作用作为大脑研究和神经再生的一种有前途的方法的综述,在这篇综述中,我们讨论了与双边MSC-NSC相互作用、环境条件下MSC向神经细胞(嵴衍生细胞亚群)分化、生物支架或通过重建与NSC共培养相关的各种治疗策略和激活机制。

一、间充质干细胞和神经干细胞合作的潜在能力
间充质干细胞可以迁移到大脑受损部位,产生神经保护和血管保护作用。此外,它们可以促进受损大脑皮层的细胞再生,而它们的分泌组对脑外伤后的神经元具有有利的影响。
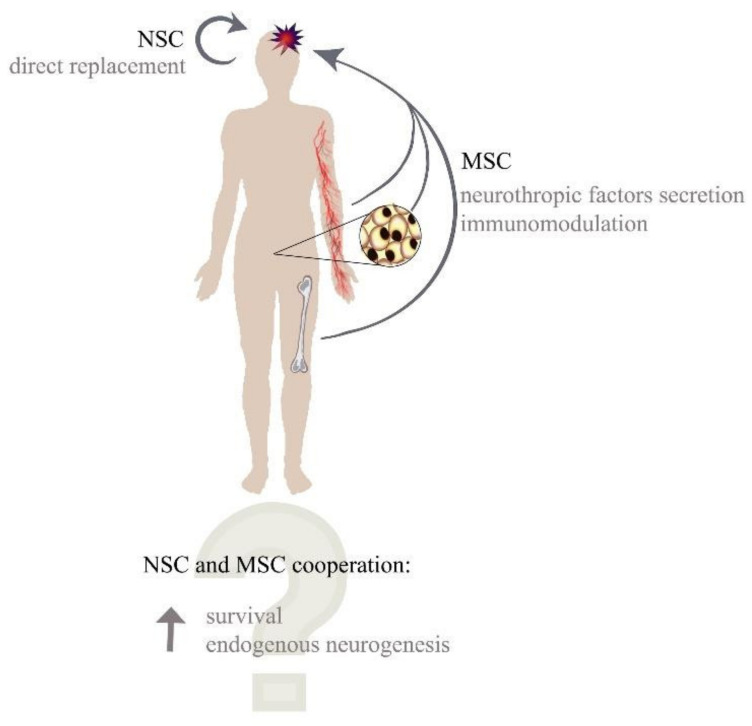
然而,关于MSC是否可以与NSC或其生态位相互作用以提高NSC分化为成熟和功能性神经元的再生能力的研究仍在进行中。间充质干细胞和神经干细胞单独在中枢神经系统中的再生潜力较低,但它们独特的功能可以建立协同关系,这对于增强治疗效果至关重要。神经干细胞移植可以提供新的神经祖细胞,而MSC可以通过佐剂效应和细胞间接触来免疫微环境并支持新生成的神经母细胞的存活和分化(图1)。
二、神经干细胞到底是什么?从分子标志物到来源困境
很多人把NSC和NPC混着用,但严格来说不一样。真正的NSC有三个特征:一是可以对称分裂(自我扩增)和不对称分裂(产生一个NSC和一个NPC);二是可以分化为三大神经谱系(神经元、星形胶质细胞、少突胶质细胞);三是在连续传代后仍能保持多向分化能力。
分子标志物上,目前公认的是Sox2、Nestin、Pax6。Sox2是维持干性的核心转录因子,敲掉它NSC就会分化。Nestin是中间丝蛋白,在神经前体细胞中高表达,成熟神经元里没有。Pax6主要调控皮层发育,在成人SVZ的NSC中也表达。
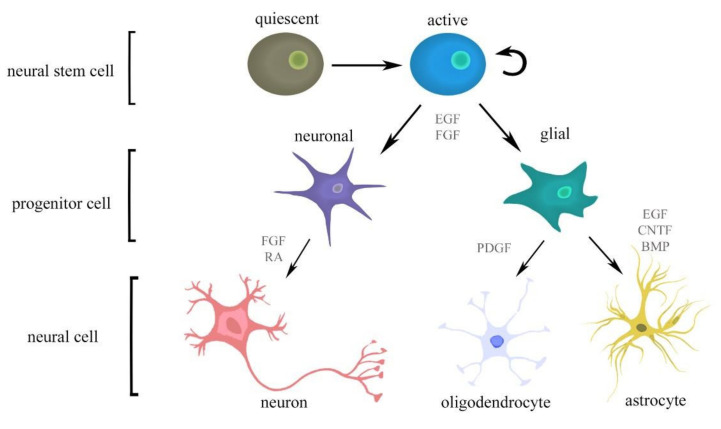
但NSC在体内的状态不是一成不变的。它有两种状态:活跃(active)和静息(quiescent)。静息的NSC高表达BMP信号通路相关基因,低表达细胞周期蛋白。当受到VEGF、BDNF、Wnt、Shh等信号刺激时,静息NSC会退出静息期,进入细胞周期。这个“唤醒”过程是神经发生的第一限速步骤(图2)。
NSC的来源主要有四种,各有各的烂摊子:
第一,胎儿/胚胎来源。这是最经典的方式。从流产胎儿或胚胎小鼠的脑组织中分离。优点是这些细胞是真的、活的NSC,分化潜能最高。缺点是伦理争议越来越大——美国NIH对胎儿组织研究已经有严格限制,国内虽然没那么严,但公众舆论压力也在增大。而且一个胎儿的量也有限,不可能工业化生产。
第二,成体脑组织来源。从SVZ或DG取一小块,体外扩增。优点是可以自体移植,没有免疫排斥。缺点是要开颅取脑组织——为了取细胞先切一刀,这种侵入性操作对患者来说代价太大。而且随着年龄增长,成人NSC的数量和功能都在下降。60岁以上患者取自己的NSC,扩增出来的细胞活力远不如年轻人。
第三,多能干细胞分化。用ESC或iPSC定向诱导为NSC。这是目前工业化生产最有希望的方向。日本京都大学已经用iPSC-NSC治疗脊髓损伤,2024年又报了帕金森病的I/II期结果(就是之前那篇Nature文章)。但问题也很实在:诱导效率不稳定(有的批次90%以上阳性,有的不到50%)、残留未分化iPSC有致瘤风险(虽然可以通过流式分选或自杀基因清除)、成本极高(一个批次几十万人民币)。
第四,直接重编程(iNSC)。用转录因子(比如Sox2、Pax6、Brn2)直接将成纤维细胞转分化为NSC,绕过iPSC中间阶段。2011年就有文章做了,但效率低得可怜,而且得到的细胞更像NPC而不是真正的NSC。这些年进展不大。
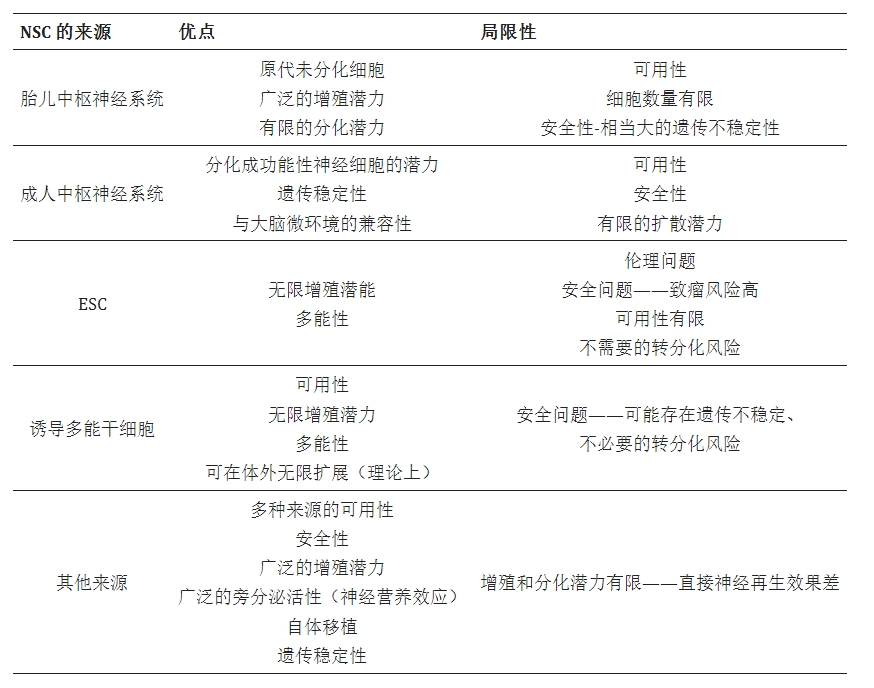
目前,在ClinicalTrials.gov上注册的临床研究多达74项。人们对应用这些干细胞治疗神经系统疾病越来越感兴趣,包括缺血性中风、帕金森病和阿尔茨海默病、肌萎缩侧索硬化症 (ALS) 或脊髓损伤 (SCI)。由于内源性神经干细胞的恢复能力无效,因此对多种来源的NSC进行了测试,包括胎儿和成人CNS衍生的NSC、来自多能干细胞的神经祖细胞以及非神经干细胞:表格1)。
到目前为止,尚未选择理想的可用来源。每个来源都有其优点和缺点,下表总结了这些优点和缺点。
三、MSC在神经修复中的角色:不是分化,是“当保姆”
MSC在神经系统疾病中的研究远远多于NSC,注册的临床试验数量是NSC的好几倍。但MSC的作用机制跟大众想象的不一样——它不是靠变成神经元来修复大脑。
2000年代初期确实有一批文章声称MSC可以在脑内转分化为神经元,表达NeuN、MAP2等神经元标志物。但后来几个实验室用更严格的谱系追踪(比如用Cre-Lox系统标记MSC然后移植)发现,那些所谓的“神经元”要么是细胞融合形成的杂合细胞,要么是自发荧光假阳性,要么是MSC内吞了周围死亡神经元的碎片。目前的主流共识是:MSC在体内基本不转分化为功能性神经元。即使有,比例也低到没有临床意义。
那MSC凭什么治脑病?靠三条腿:
第一条,免疫调节。MSC不表达MHC-II类分子(HLA-DR阴性),也不表达CD80、CD86等共刺激分子,所以不会激活CD4+ T细胞。更关键的是,MSC能主动抑制免疫反应。机制包括:分泌IDO(indoleamine 2,3-dioxygenase)消耗色氨酸,导致T细胞周期阻滞;分泌PGE2、TGF-β、IL-10等抗炎因子;直接接触诱导Treg生成;把巨噬细胞从促炎的M1型掰成抗炎的M2型。在脊髓损伤或脑卒中的动物模型中,移植MSC后,损伤部位的IFN-γ、TNF-α、IL-1β显著下降,IL-10上升。
第二条,旁分泌营养支持。MSC分泌一堆神经营养因子:BDNF(促进神经元存活和突触可塑性)、GDNF(对多巴胺能神经元尤其重要)、NGF、NT-3、bFGF、VEGF(促血管新生)、HGF(抗凋亡)。这些因子可以保护濒死的神经元,促进轴突生长,诱导血管再生。一个经典的实验是:把MSC的条件培养基(就是养过MSC的培养基,里面都是它们分泌的东西)打进中风大鼠的脑子里,效果跟打细胞本身差不多。这说明旁分泌是MSC的主要作用通路。
第三条,外泌体(EVs)介导的远程调控。最近五年的热点。MSC分泌的外泌体(30-150nm的小囊泡)里面装了miRNA、mRNA、蛋白质,可以被受体细胞内吞,从而调控受体细胞的基因表达。比如MSC外泌体里的miR-133b可以促进神经突生长,miR-17-92簇可以促进少突胶质前体细胞增殖和髓鞘形成。外泌体的优势是:没有活细胞,所以不会有致瘤或栓塞风险;可以冻干保存,不用液氮;可以通过表面修饰实现靶向递送。目前已经有一些临床前研究用MSC外泌体治疗中风、脊髓损伤、帕金森病,结果跟用MSC本身差不多。将来很可能MSC外泌体会取代MSC,变成“无细胞治疗”的主力。
但MSC也不是没有副作用。静脉输注MSC时,由于细胞体积较大(直径15-30μm),大部分会被肺部毛细血管床截留,只有一小部分能到达脑部。这种“肺首过效应”本身不是问题——被截留在肺部的MSC反而可以分泌抗炎因子,通过全身循环间接影响脑部。但有研究报道,高剂量静脉输注MSC可能引起微栓塞,尤其是在肺功能不好的患者身上。还有研究担心MSC在某些条件下可能促进肿瘤生长(比如给荷瘤小鼠打MSC,肿瘤长得更快),但这个争议很大,不同实验室结果相反。2024年FDA批准的Ryoncil(MSC治疗儿童GVHD)是基于几十个临床试验的数据,没有发现明显的促瘤信号。所以风险可能被夸大了,但也不是零。
四、MSC和NSC怎么互动?分子机制层面的事
这篇综述最有价值的部分,是系统梳理了MSC和NSC之间的相互作用机制,而不是只说“1+1>2”这种空话。
第一个机制:MSC通过Notch信号维持NSC的干性。
Notch信号在发育神经生物学里是老面孔了。当Notch受体(Notch1-4)被配体(Jagged1/2、DLL1/3/4)激活后,Notch受体会被γ-secretase切割,释放胞内段NICD(Notch intracellular domain)。NICD进入细胞核,与转录因子RBP-J结合,激活下游靶基因(如Hes1、Hes5)。Hes1和Hes5是碱性螺旋-环-螺旋转录因子,它们抑制 proneural 基因(如Ascl1、Neurogenin)的表达,从而抑制分化、维持干性。
MSC表面表达Jagged1和DLL1。当NSC和MSC共培养时,MSC通过直接接触激活NSC的Notch信号。有实验显示,在没有EGF和bFGF的培养基里,单独培养的NSC很快就会分化——细胞变得扁平,Nestin下调,βIII-tubulin(神经元标志物)上调。但跟MSC共培养的NSC,即使没有EGF/bFGF,仍然维持Nestin阳性,Hes1和Hes5的表达水平跟有EGF/bFGF时差不多。这说明MSC可以直接替代外源性生长因子的作用,通过Notch信号维持NSC的未分化状态。
第二个机制:MSC通过旁分泌因子促进NSC的存活和神经元分化。
这个听起来跟上面有点矛盾——MSC既维持NSC的干性,又促进分化?其实不矛盾,取决于微环境和时间点。
在NSC刚移植进去的时候,MSC分泌的BDNF、GDNF、HGF可以抑制凋亡通路。具体的分子通路:BDNF结合TrkB受体,激活PI3K/Akt通路,Akt磷酸化后抑制Bad和caspase-9,从而阻断线粒体凋亡途径。HGF结合c-Met受体,同样激活PI3K/Akt,还激活MAPK/ERK通路,促进细胞增殖。在氧-葡萄糖剥夺(OGD)模型中(模拟缺血性中风),与MSC共培养的NSC,凋亡细胞比例比单独培养的NSC低40-60%。
而在需要分化的时候,MSC分泌的BDNF和GDNF又可以促进NSC向神经元方向分化。具体的机制涉及:BDNF/TrkB激活下游的Ras-MAPK通路,磷酸化CREB,CREB进入细胞核促进 proneural 基因(如NeuroD1)的表达。有研究用微流控芯片做共培养,发现NSC跟MSC共培养7天后,βIII-tubulin阳性的神经元比例比对照组高出2倍以上,而且这些神经元有动作电位(电生理记录证实)。
第三个机制:MSC通过免疫调节为NSC移植创造“免疫豁免”微环境。
这是联合移植最直观的好处。异体NSC移植后,宿主的免疫系统会攻击它们——CD8+ T细胞会直接杀伤,巨噬细胞会吞噬。MSC可以通过前面说的IDO、PGE2、TGF-β等机制抑制T细胞活化,把巨噬细胞掰成M2型,减少IFN-γ和TNF-α的释放。这样一来,NSC的存活率可以大幅提升。
有一个经典的动物实验:在脊髓损伤大鼠模型中,单独移植NSC的组,8周后存活的NSC只有移植量的5-10%。而NSC+MSC联合移植的组,存活率提升到30-40%。而且联合移植组中,NSC分化为神经元的比例也更高——可能是因为MSC分泌的BDNF、GDNF提供了分化信号。
第四个机制:NSC反过来也能影响MSC——诱导MSC向神经谱系分化。
这个方向的证据比前三个弱一些,但确实有报道。有研究发现,NSC分泌的Shh(Sonic hedgehog)可以诱导MSC表达神经前体细胞标志物(Nestin、Pax6)。还有研究用transwell共培养(不让细胞直接接触,只共享培养基),发现NSC的条件培养基也能让MSC表达一些神经元样的标志物。但问题是,这些MSC到底有没有变成真正的功能性神经元?目前没有电生理证据。大多数研究者认为,即使MSC被诱导表达一些神经标志物,它们也很难形成动作电位和突触。所以这条机制在联合移植中的贡献可能不大,主要贡献还是MSC支持NSC,而不是反过来。
五、总结
干细胞与伴生/支持细胞之间的相互作用对平衡和组织再生至关重要。在许多器官中,间充质干细胞维持干细胞的存活和转运增殖细胞(TAC)的增殖,然后分化成目标细胞类型。虽然证据尚不充分,但间质作为生态位的组成部分,似乎在静止的间充质干细胞与增殖、分化和从细胞龛迁移的祖细胞之间的平衡中发挥作用。
神经干细胞和间充质干细胞之间也存在同样的相互作用。
- 由于神经干细胞可能是所有神经细胞类型的无限来源,而间充质干细胞则显示出高度的旁分泌活性,因此将它们联合用于治疗神经系统疾病似乎极具前景。
根据现有的科学文献,间充质干细胞和神经干细胞的结合似乎代表了一个有前途的治疗前景(图4)。
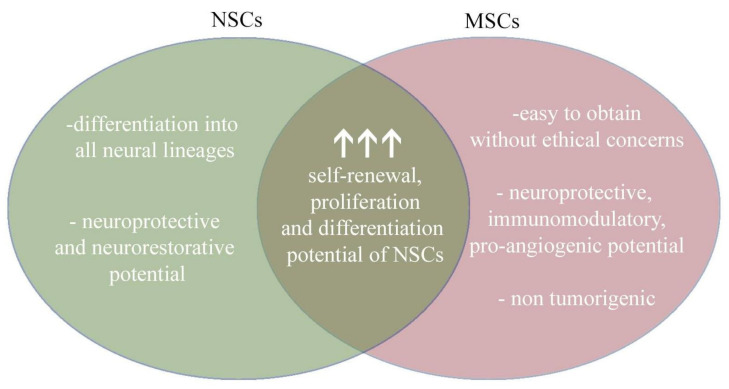
- 神经干细胞可以作为分化成成熟神经细胞和神经胶质细胞的细胞来源。
- 反过来,间充质干细胞可以通过神经保护、免疫调节和促血管生成活性支持神经干细胞的移植。使用间充质干细胞的另一个优点是易于从多个来源分离并且不产生肿瘤。
尽管这种相互作用的机制尚未被探索,但其效果已经非常有希望。尽管如此,仍然需要对这种组合的使用进行更多研究,特别是在动物模型和人体临床试验中。
六、常见问题解答(FAQ)
参考资料:Kaminska A, Radoszkiewicz K, Rybkowska P, Wedzinska A, Sarnowska A. Interaction of Neural Stem Cells (NSCs) and Mesenchymal Stem Cells (MSCs) as a Promising Approach in Brain Study and Nerve Regeneration. Cells. 2022 Apr 26;11(9):1464. doi: 10.3390/cells11091464. PMID: 35563770; PMCID: PMC9105617.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 扫码添加官方微信
扫码添加官方微信