全球约1-3%的女性受卵巢早衰(POI)困扰,干细胞治疗为这些患者带来了新的生育希望。
干细胞治疗卵巢早衰不孕:2024年最新研究现状与未来展望
日前,韩国CHA大学团队在《Biomolecules》期刊发表了一项关于干细胞治疗卵巢早衰(POI)不孕患者的权威综述,全面探讨了干细胞治疗POI的现状、临床实施的局限性及未来前景。
卵巢早衰指女性40岁前卵巢功能衰退,全球发病率约1-3%,表现为月经紊乱、雌激素缺乏和促卵泡激素(FSH)升高。传统激素替代疗法仅能缓解症状,而间充质干细胞(MSCs) 因其自我更新、多向分化和免疫调节特性,成为再生医学领域的研究热点。

01 POI的传统治疗瓶颈
POI患者通常面临月经不调和不孕问题,这些问题常在确诊前数年就会出现。对于大多数POI患者来说,生育能力至关重要,许多患者渴望拥有遗传学上的后代。
目前POI患者的自然受孕率仅为5-10%。现有治疗方法包括:
- 雌激素治疗
- 促性腺激素
- 皮质类固醇
- 免疫抑制剂
但这些方法主要旨在提高排卵率和妊娠率,既不能真正改善卵巢功能,也不能显著提高妊娠率。
2021年国内一项回顾性研究报道,POI患者通过体外受精(IVF)和冷冻胚胎移植获得了与年龄匹配正常对照组相当的累积临床妊娠率和活产率。但需要注意的是,这种积极结果仅限于有大量卵泡的POI女性,通常见于自身免疫引起的病例或早期诊断的病例。

02 干细胞治疗:POI的新希望
近年来,多种间充质干细胞(MSCs)被应用于POI的研究,如骨髓(BM)、经血、脐带(UC)、羊水、羊膜、胎盘和子宫内膜等来源的MSCs,也称为干细胞疗法(SCT),其独特的机制能促进POI患者卵巢功能恢复和卵母细胞的再生(见下图)。
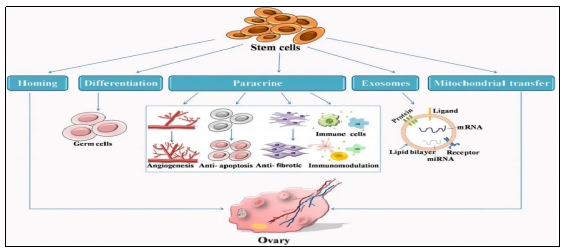
干细胞治疗的多重机制
卵泡发育调控:
- 通过miR-146a-5p等外泌体改善线粒体功能,激活PI3K/mTOR通路
- 外泌体携带miR-644-5p下调P53,抑制颗粒细胞凋亡
- 通过circBRCA1/FOXO1轴减轻氧化损伤
- 调控NR4A1通路恢复线粒体动力学平衡,促进睾酮合成
微环境改善:
- 促进巨噬细胞M2极化,抑制NLRP3炎症小体
- 上调NRF2/HO-1通路,降低活性氧(ROS)
- 抑制TGF-β1/Smad3信号,抗纤维化
- 分泌VEGF、IGF-1等生长因子,促进血管生成
03 临床研究显著成果
骨髓来源干细胞研究
2018年,Herraiz等人研究了卵巢内移植自体骨髓间充质干细胞(BM-MSCs)治疗卵巢反应不良患者的效果。治疗2周后,患者窦卵泡计数(AFC)明显改善,抗苗勒管激素水平连续两次增加,81.3%的患者卵巢功能改善,并报告了5次成功受孕。

经血来源干细胞突破
2020年,Zafardoust等进行了一项自体经血来源间充质干细胞(MenSC)治疗卵巢反应不良的I/II期临床试验。移植后3个月,MSCs组15名女性中有4名自然怀孕,对照组在同一时期没有怀孕。直至随访结束,MSCs组15例中有7例临床妊娠,5名成功分娩,对照组16例中仅有2例临床妊娠,1例名成功分娩。
脐带来源干细胞进展
2020年,国内团队在一项研究中,利用脐带来源的MSCs (UC-MSCs)治疗了61名POI患者。UC-MSCs移植后成功挽救了POI患者的卵巢功能,表现为卵泡发育增加,卵子收集改善,并获得了四次临床分娩,所有出生的婴儿都发育正常。

04 不同干细胞来源的比较
| 来源类型 | 优势 | 临床效果 |
|---|---|---|
| 脐带来源(UC-MSCs) | 增殖能力强,免疫原性低 | 可使FSH下降40% |
| 脂肪来源(AD-MSCs) | 取材便捷 | 促AMH分泌作用 |
| 经血来源(MenSCs) | 具有卵巢趋向性 | 上调卵巢中FOXL2表达 |
| 骨髓来源(BM-MSCs) | 研究历史悠久 | 改善卵巢功能,提高妊娠率 |
胎儿附属组织(脐带、羊膜、胎盘)来源的MSCs具有显著优势:增殖能力强(群体倍增次数比成人来源高3-5倍)、免疫原性低(HLA-DR阴性率>95%)、伦理争议少。
05 涉及干细胞移植治疗卵巢早衰的临床试验
ClinicalTrials.gov记录了多项SCT治疗POI的临床试验,截至2023年12月15日,共有28项注册研究。
在该队列中,2项研究被暂停,1项被撤回,1项被终止,10项试验的状态未知,其中2项被认为不重要。在明确的12项SCT治疗POI试验中,7项已经结束,2项正在积极招募参与者,2项处于预招募阶段,1项试验正在进行中,但目前尚未招募。
06 结论与展望
虽然过去几十年辅助生殖技术取得了快速进步,但POI问题仍未得到解决。干细胞具有多能性、自我更新能力和分化成各种细胞类型的能力,已成为治疗POI的有希望的途径,它能调节卵巢内分泌功能并恢复女性生育能力。
未来需要:
- 全面了解干细胞的治疗机制
- 开发耗时较少的培养方案
- 减少免疫反应和肿瘤变化的风险
- 实现干细胞的规范化生产
- 开展更大规模、长期随访的临床研究
随着精准医疗的发展,建立包含优选细胞来源(胎儿附属组织MSCs)、3D低氧培养、原位多次移植(1×10⁸细胞/次)的标准化治疗方案,结合靶向修饰技术,将推动POI治疗进入精准医学新时代。
参考资料:
【1】Zhu, X.; Ye, J.; Fu, Y. Premature ovarian insufficiency patients with viable embryos derived from autologous oocytes through repeated oocyte retrievals could obtain reasonable cumulative pregnancy outcomes following frozen-embryo transfer.
【2】Herraiz, S.; Romeu, M.; Buigues, A.; Martinez, S.; Diaz-Garcia, C.; Gomez-Segui, I.; Martinez, J.; Pellicer, N.; Pellicer, A.Autologous stem cell ovarian transplantation to increase reproductive potential in patients who are poor responders.
【3】Zafardoust, S.; Kazemnejad, S.; Darzi, M.; Fathi-Kazerooni, M.; Rastegari, H.; Mohammadzadeh, A. Improvement of Pregnancy Rate and Live Birth Rate in Poor Ovarian Responders by Intraovarian Administration of Autologous Menstrual Blood DerivedMesenchymal Stromal Cells: Phase I/II Clinical Trial. Stem Cell Rev.
【4】Long Yan | Yixuan| Wu Li Li | Jun Wu | Feiyan Zhao | Zheng Gao | Wenjing Liu | Tianda Li | Yong Fan | Jie Hao | Jianqiao Liu | Hongmei Wang. Clinical analysis of human umbilical cord mesenchymal stem cell allotransplantation in patients with premature ovarian insufficiency. DOI: 10.1111/cpr.12938.
【5】Hye Kyeong Kim and Tae Jin Kim. Current Status and Future Prospects of Stem Cell Therapy for Infertile Patients with Premature Ovarian Insufficiency. DOI:10.3390/biom14020242.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信