30%的ITP患者会发展为难治性疾病,脐带间充质干细胞治疗为这些传统治疗无效的患者带来了新的希望。
干细胞治疗难治性血小板减少症(ITP):国内团队首次揭示疗效与安全性 | 新突破
近日,国内研究团队在《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy)期刊发表了一项突破性临床研究,这是国际上首次评估脐带间充质干细胞(UC-MSCs)治疗难治性免疫性血小板减少症(ITP) 的疗效和安全性的临床试验,该试验已在ClinicalTrials.gov注册(注册号:NCT04014166)。
免疫性血小板减少症(ITP)是一种获得性自身免疫性出血性疾病,以血小板减少为主要特征。其病因是免疫耐受失衡,导致血小板破坏加速和血小板生成受损。难治性ITP是指对多种治疗(包括TPO-RA、利妥昔单抗、脾切除)无反应或复发的患者,这些患者出血风险更高,生活质量显著下降,死亡率也明显增加

01 难治性ITP的治疗挑战
ITP是一种常见的自身免疫性出血性疾病,其特征是血小板破坏增加和生成受损。尽管有多种治疗选择,但约30%的患者会发展为难治性ITP,意味着他们对现有治疗方法反应不佳。
难治性ITP患者面临更大的出血风险和生活质量下降,临床治疗非常棘手。传统治疗方法如糖皮质激素、免疫球蛋白、脾切除术、利妥昔单抗和血小板生成素受体激动剂(TPO-RA)对这些患者效果有限。
细胞治疗作为一种新兴治疗策略,通过免疫调节作用恢复免疫平衡,为难治性ITP提供了新的治疗方向。
02 研究设计与患者特征
这项前瞻性、开放性研究共纳入了18例难治性ITP患者(男3例,女15例),其中剂量递增期患者12例,剂量扩展期患者6例,年龄30~50岁,中位病程73个月。
患者既往治疗经历显示:
- 15例患者接受过5种以上常规治疗
- 10名患者接受过脾切除术
- 13名患者接受过利妥昔单抗治疗
所有患者均符合难治性ITP的诊断标准,即至少对两种常规治疗方案无效或复发。
03 治疗方法与剂量设计
研究采用剂量递增设计,在获得每位参与者知情同意后:
剂量递增阶段:患者被分为三个剂量组
- 0.5×10⁶/kg组(n=3)
- 1.0×10⁶/kg组(n=3)
- 2.0×10⁶/kg组(n=6)
治疗方案:每周输注一次UC-MSCs,共输注4次
剂量确定:根据剂量递增阶段结果确定扩展期患者的最佳剂量
这种设计允许研究人员评估不同剂量的安全性和初步疗效,为后续研究确定最佳治疗剂量。
04 安全性表现良好
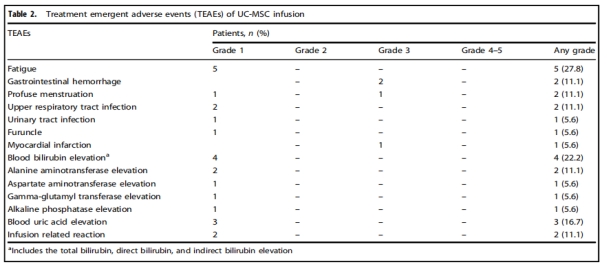
安全性分析显示(表2):
- 13例患者经历轻度副反应(疲劳、血胆红素升高、尿酸升高),经短期干预后恢复或自行恢复
- 3例患者出现3级出血表现(胃肠道出血、月经量多),被认为与基础疾病相关
- 仅1例患者出现3级不良事件,被确定为剂量限制性毒性事件
总体安全性良好,大多数不良事件为轻度且可控,表明UC-MSCs输注在难治性ITP患者中具有可接受的安全性特征。
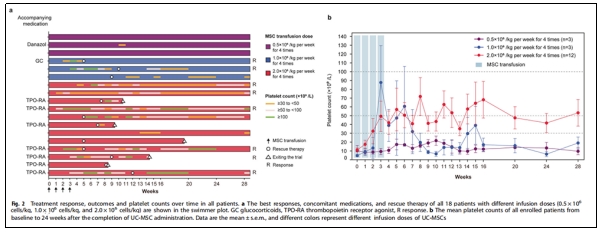
05 疗效结果令人鼓舞
效果分析(图2):术后8例患者达到了血小板反应(R,定义为血小板计数≥30×109/L,与基线计数相比至少增加2倍且无出血),其中5例患者处于剂量递增阶段,3例患者处于剂量扩展阶段,总体缓解率为44.4%(4例患者达到完全缓解),中位累积缓解持续时间为6.5周。
06 药代动力学与免疫原性分析
UC-MSCs药代动力学分析:共有8例患者接受了药代动力学测定,所有患者的外周血在30分钟开始检测到SRY基因,并且在大多数患者中可持续4小时;输注后8小时,血液中未检测到人类特异性序列,表明通过静脉输注UC-MSCs在外周血最长停留时间为8小时。
体液免疫原性分析:对12例患者细胞输注前后的抗药物抗体(ADA)分析发现,在任意时间点均未检测到ADA,这表明UC-MSCs输注后患者体内未发生ADA。
07 研究意义与临床价值
该项研究是首个评估UC-MSCs治疗难治性ITP安全性和有效性的前瞻性研究,取得了44.4%的总体缓解率,为难治性ITP提供了一种有前途的替代治疗方案。
尤其值得注意的是,这些患者都是经过多种传统治疗失败的重度难治性病例,能够获得这样的缓解率十分令人鼓舞。
研究结果支持UC-MSCs通过免疫调节作用恢复免疫平衡,减少血小板破坏,从而提高血小板计数的机制假说。
总 结:该研究是首个评估UC-MSCs治疗难治性ITP安全性和有效性的前瞻性、开放性研究,并且取得了44.4%的总体缓解率,这表明UC-MSCs为难治性ITP提供了一种有前途的替代治疗方案。鉴于本研究的样本量和扩展剂量有限,未来需通过更大样本量和更高输注剂量的临床试验进一步验证。
参考资料:
【1】Liu, Y. et al. Deciphering transcriptome alterations in bone marrow hematopoiesis at single-cell resolution in immune thrombocytopenia. Signal Transduct. Target.Ther. 7, 347 (2022).
【2】Provan, D. et al. Updated international consensus report on the investigation and management of primary immune thrombocytopenia. Blood Adv. 3, 3780-3817(2019).
【3】Miltiadous, O., Hou, M. & Bussel, J. B. Identifying and treating refractory ITP: difficulty in diagnosis and role of combination treatment. Blood 135, 472-490(2020).
【4】Yunfei Chen.et al.Efficacy and safety of human umbilical cord-derived mesenchymal stem cells in the treatment of refractory immune thrombocytopenia: a prospective, single arm, phase I trial. doi:10.1038/s41392-024-01793-5.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信