缺血性心脏病(IHD)是一种由冠状动脉粥样硬化引起的心血管疾病,常导致心肌供血不足、组织缺氧乃至心力衰竭,是全球范围内导致死亡的主要病因之一。
脂肪干细胞治疗缺血性心脏病:安全性与可行性分析获新进展 | 研究报道
近年来,基于脂肪干细胞(ASCs)的再生疗法为IHD的治疗提供了新方向。Xiao等人近期发表的一篇系统综述,全面探讨了脂肪干细胞在治疗IHD中的机制、细胞来源与特性、功能影响因素、工程化策略及临床研究进展。

一、脂肪干细胞治疗缺血性心脏病机制分析
随着时间的推移,关于使用ASCs治疗IHD的机制观点不断演变,这些理论推动了ASCs更好的管理,如图1所示,ASCs具有良好的分化能力和旁分泌潜力,使其能够从多个方面有效治疗IHD。
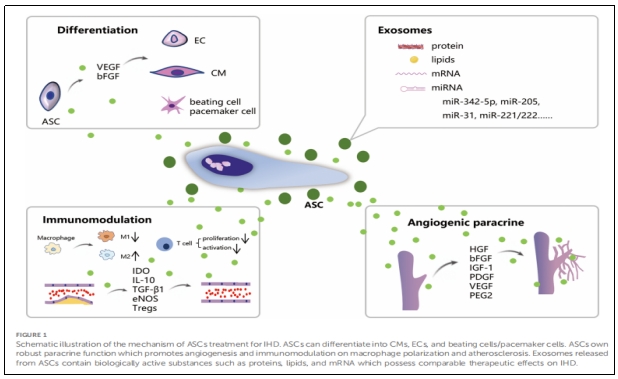
①ASCs的促血管生成作用:大量研究认为,ASCs移植之所以能促进缺血区域代偿性血管生成,其重要因素在于其强大的旁分泌作用,它能产生多种促进血管生成的细胞因子,包括VEGF、bFGF、HGF、PDGF、IGF-1等。
②ASCs的免疫调节作用:心梗后,先天免疫反应被触发,其特征是大量炎性免疫细胞的募集和浸润,如单核细胞衍生的M1巨噬细胞,最终转化为抗炎的M2巨噬细胞,并伴随着各种促炎和抗炎细胞因子释放。因此,从免疫病理学角度来看,ASCs对IHD具有积极作用。
二、脂肪干细胞的组织类型和来源选择
哺乳动物脂肪组织可分为白色、棕色和米色三种类型。研究表明,棕色脂肪来源的ASCs在增殖、分化及旁分泌活性方面均优于白色脂肪来源的ASCs,甚至具备自主分化为心肌细胞的潜力。
此外,脂肪的组织来源也显著影响细胞功能,例如心外膜脂肪来源的ASCs表现出更强的促血管生成能力。因此,在开展IHD治疗研究时,选择合适的ASC类型与来源至关重要。
三、影响脂肪干细胞的功能因素
①老化:虽然ASCs数量会随着年龄的增长而减少存在争议,但不可否认的是,衰老确实会对ASCs的生物学特征产生负面影响。研究表明,从老年动物或个体中获得的ASCs其增殖率和活率会急剧下降。
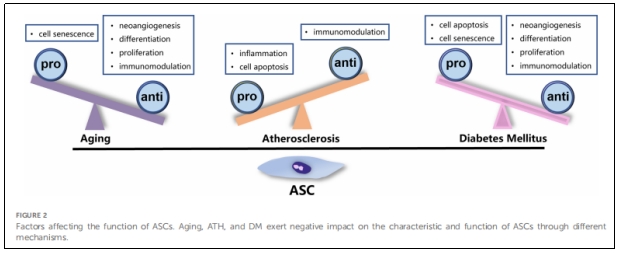
②糖尿病:患者体内的微环境,如高血糖、过度氧化应激、线粒体功能障碍、促炎细胞状态和缺氧,这些变化会在一定程度上影响ASCs。研究表明,糖尿病患者的ASCs与正常人相比,其增殖能力会随着患者病情的加重而减弱,衰老和细胞凋亡也会增加。
③动脉粥样硬化(ATH):研究发现,与从非ATH供体分离的ASCs相比,源自ATH受试者的ASCs表现出独特的特征,ATH会显著损害ASCs的免疫调节功能并对其治疗效率产生负面影响。
四、脂肪干细胞的工程化策略
为提高细胞移植后的存活率和治疗效果,研究者开发了多种生物材料封装策略,用于增强ASCs在缺血心肌中的滞留与功能发挥。这些材料可改善细胞存活情况,促进心肌细胞分化与血管生成,从而提升心脏修复效果。

五、临床研究进展
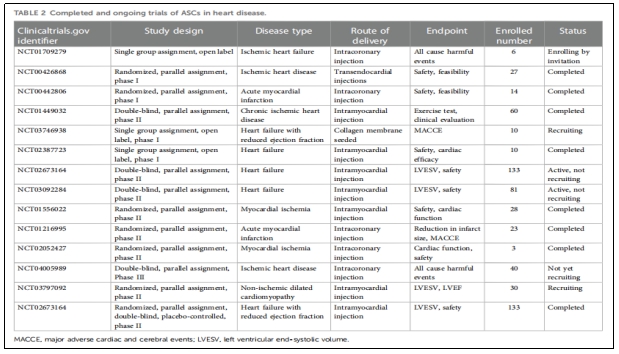
目前,ASCs已在多项针对心力衰竭或心肌梗死的临床试验中显示出良好的安全性和初步有效性(表2)。然而,受IHD疾病复杂性的影响,ASCs的临床应用仍处于早期阶段。未来仍需开展大规模、长期随访的随机对照试验,以进一步验证该疗法的可靠性与疗效。
总结:ASCs因其获取便捷、创伤小、产量高、低免疫原性且无伦理争议等优势,成为IHD再生治疗的重要候选细胞类型。它们通过多途径促进心肌和血管再生,具有广阔的临床应用前景。持续优化ASC的递送策略并明确其作用机制,将对其未来的临床转化具有重要推动价值。
参考资料:
Weizhang Xiao and Jiahai Shi, Application of adipose-derived stem cells in ischemic heart disease: theory, potency, and advantage. DOI 10.3389/fcvm.2024.1324447.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信