摘要:近日,一项发表于国际知名期刊《临床医学杂志》的随机对照试验探讨了脐带间充质干细胞(UC-MSC)及其分泌组在多囊卵巢综合征(PCOS)治疗中的应用价值。研究结果显示,该疗法有望通过改善胰岛素敏感性和调节免疫反应,为PCOS患者,尤其是伴有胰岛素抵抗的群体,提供一种全新的治疗选择。
多囊卵巢综合征(PCOS)是一种育龄期女性高发的内分泌代谢紊乱疾病,常伴随慢性低度炎症和胰岛素抵抗(IR)。研究表明,C肽水平升高(代偿性高胰岛素血症的标志物)和脂联素水平降低(一种具有胰岛素增敏作用的脂肪因子)是驱动PCOS代谢紊乱的关键因素。
人脐带间充质干细胞(UC-MSCs)及其分泌组可通过旁分泌及表观遗传机制发挥免疫调节作用,然而,其在PCOS患者中的纵向临床研究证据仍然有限。

干细胞治疗为多囊卵巢综合征带来新希望:不仅能缓解症状,还能恢复卵巢功能
为了进一步验证UC-MSCs及其分泌组对PCOS多项指标的改善作用,知名期刊 《临床医学杂志》 发表了一篇题为《脐带间充质干细胞及其分泌组对代谢组学特征(C肽、脂联素、空腹胰岛素和空腹血糖)的影响:一项随机对照试验》的研究论文[1]。该研究为PCOS的治疗开辟了新的探索方向。
什么是多囊卵巢综合征(PCOS),其诊断标准为何存在差异?
多囊卵巢综合征是育龄女性最常见的内分泌疾病,全球患病率约为6%-15%。其病因复杂,涉及遗传、环境和代谢等多种因素。
诊断率的差异主要源于采用了不同的诊断标准:根据最严格的NIH标准(需同时存在高雄激素血症和慢性无排卵),患病率约为5.5%;而根据范围最广的鹿特丹标准(满足高雄激素、稀发排卵、多囊卵巢三项中的两项即可),患病率则高达11.5%。
该综合征的核心病理特征是什么,会引发哪些主要风险?
胰岛素抵抗是该病的核心病理特征,约40%-70%的患者(尤其是肥胖者)存在此问题。胰岛素抵抗不仅会引发慢性高胰岛素血症和全身性低度炎症,干扰卵泡发育和胚胎着床,还会从代谢角度显著增加患者罹患2型糖尿病、代谢综合征和心血管疾病的风险。此外,慢性无排卵导致的雌激素持续暴露也会增加子宫内膜病变的风险。
近年来,代谢组学研究为理解PCOS提供了哪些新见解?
代谢组学作为系统生物学的重要工具,通过分析小分子代谢物,揭示了PCOS更深层的生化紊乱:
- 发现特征性代谢改变:研究发现了氧化应激标志物(如丙二醛)的改变、支链氨基酸代谢受损以及线粒体能量通路紊乱,将胰岛素抵抗与慢性炎症和卵巢功能障碍联系起来。
- 识别关键生物标志物:证实了脂联素(具有胰岛素增敏作用,在患者体内持续降低)和C肽(反映内源性胰岛素分泌)在反映代谢和激素失调中的重要作用。
当前PCOS治疗面临什么局限?本研究旨在探索什么新方向?
传统疗法的局限:以二甲双胍为代表的传统疗法主要改善胰岛素敏感性,但对PCOS病理过程中的炎症和表观遗传通路影响有限。
本研究的目的:在此背景下,该研究旨在评估脐带间充质干细胞及其分泌组这一新兴再生疗法对PCOS女性的效果。该疗法通过调节炎症、胰岛素信号传导和组织修复,有望提供一种更全面的治疗选择,并为未来基于表观遗传学的治疗策略奠定基础。
总结:PCOS是一种诊断标准多样、以胰岛素抵抗为核心的复杂疾病,可导致生殖与代谢双重风险。代谢组学技术揭示了其背后的分子机制(如线粒体功能障碍、炎症),而针对这些机制,基于脐带间充质干细胞的再生疗法正在成为克服传统治疗局限性的新研究方向。
研究方法
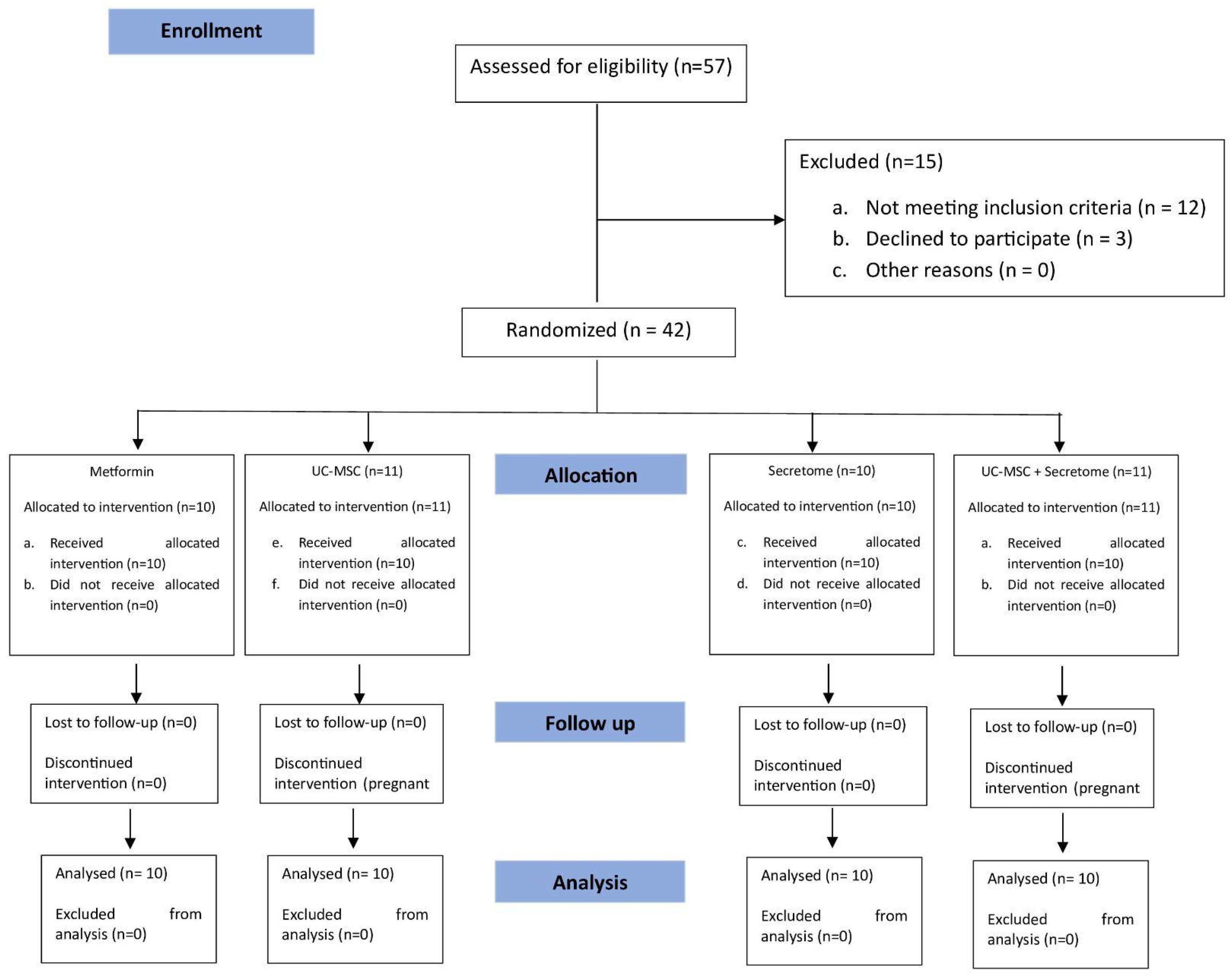
本随机对照试验(RCT)纳入40名符合鹿特丹标准的PCOS患者(图1),随机分为四组:
- 二甲双胍组:每日口服750mg二甲双胍;
- UC-MSC组:单次输注脐带间充质干细胞(0.3 × 10^6个细胞/kg体重);
- 分泌组组:使用分泌组鼻滴剂(2mL);
- 联合治疗组:UC-MSC输注(剂量同前)联合分泌组鼻滴剂(2mL)。
研究测量了基线及治疗后1、3、6个月的空腹血糖、空腹胰岛素、HOMA-IR指数、C肽和脂联素水平。采用重复测量方差分析或Friedman检验进行数据分析,并使用ROC曲线评估生物标志物对治疗反应的预测价值。
结果
基线特征
这项研究是一项随机对照试验,将40名符合鹿特丹诊断标准的PCOS女性平均分为四组:二甲双胍组、脐带间充质干细胞(UC-MSC)组、分泌组以及UC-MSC联合分泌组。所有受试者均完成了为期6个月的随访,依从性良好。
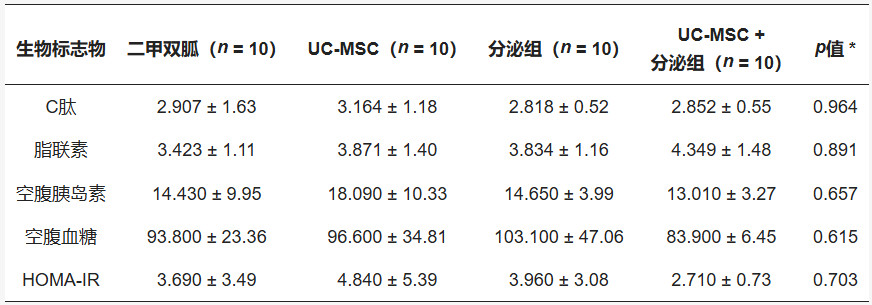
在干预开始前的基线期,四组受试者在年龄、BMI以及关键代谢指标(包括空腹血糖、空腹胰岛素、HOMA-IR、C肽和脂联素)上均无统计学差异,表明分组均衡、具有可比性(见表1)。值得注意的是,该研究队列中的PCOS患者主要为非肥胖至超重表型,这为观察干预措施在不同体重基础上的效果提供了背景。
除了对基线代谢指标进行描述性统计外,研究还专门分析了空腹胰岛素和C肽这两个反映基础代谢动态的互补指标,并通过散点图将两者在基线时的关系进行了可视化呈现(图2)。空腹胰岛素反映循环中的高胰岛素血症水平,而C肽则更稳定地指示内源性胰岛素的分泌情况。
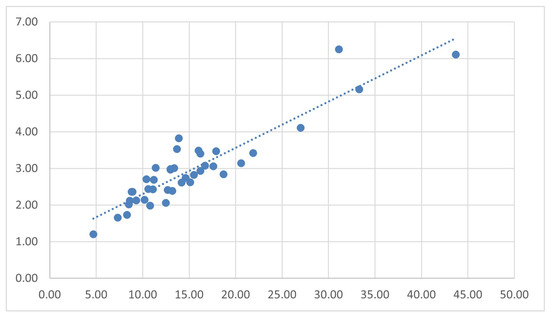
这种基线关系的建立,不仅揭示了受试者在干预前的代谢补偿特征,也为后续评估不同治疗(特别是干细胞和分泌组疗法)在随访期间所引起的纵向代谢变化提供了重要的个体化参照基准。
代谢生物标志物随时间的变化
01、不同治疗对C肽和脂联素这两种关键代谢生物标志物有何具体影响?
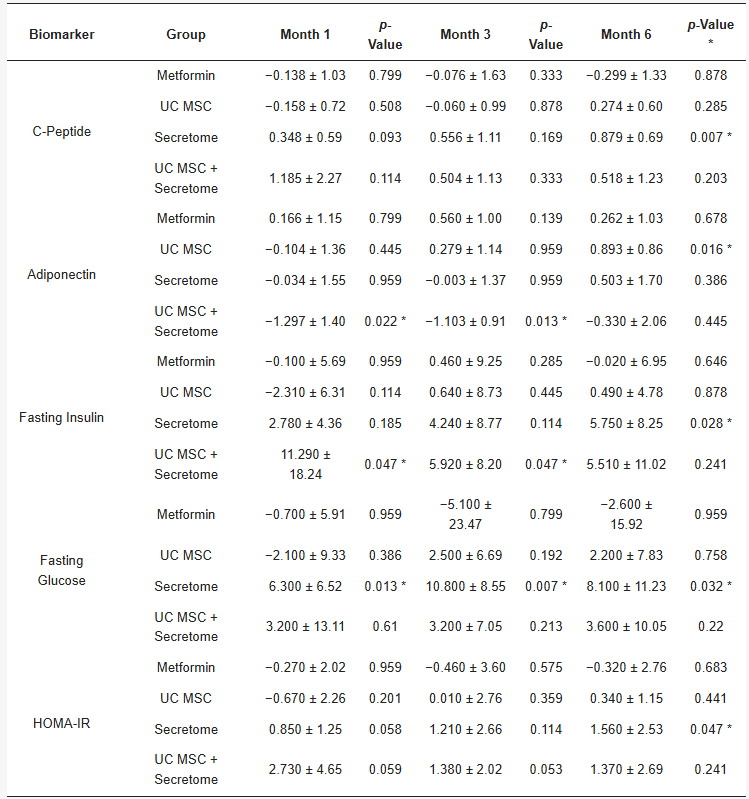
C肽(反映内源性胰岛素分泌)
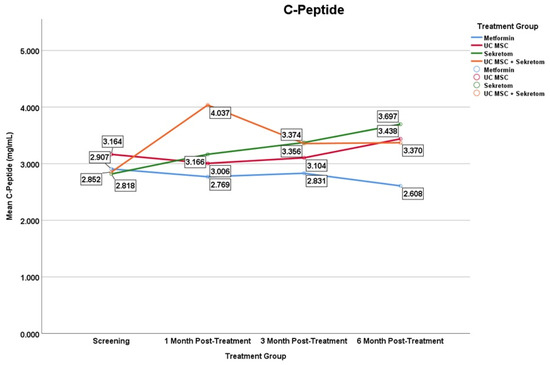
- 分泌组:在第6个月时出现显著升高(差值:+0.879±0.69;p=0.007)。这表明分泌组可能在治疗后期改变了胰岛素的分泌动力学,但由于缺乏药代动力学数据,其直接的全身效应尚无法证实(图3)。
- UC-MSC+分泌组:在治疗初期显示出较强的升高效应,但该效应未能持续至第6个月。
- 二甲双胍组与UC-MSC组:在整个随访期内均未观察到C肽的显著变化。
脂联素(具有胰岛素增敏和抗炎作用的保护性脂肪因子)
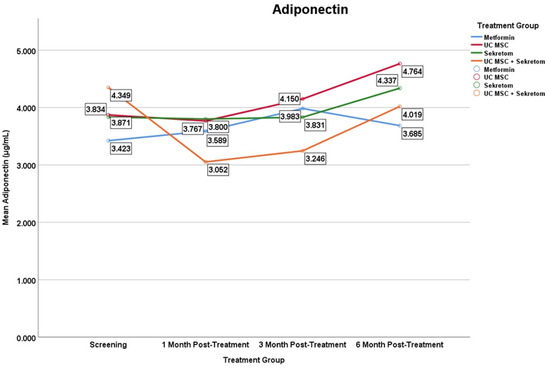
- UC-MSC组:在第6个月时观察到显著升高(差值:+0.893±0.86;p=0.016),这是代谢改善的积极信号(图4)。
- UC-MSC+分泌组:出现了相反的效应,在治疗早期脂联素水平显著降低:第1个月(差值:-1.297±1.40;p=0.022)和第3个月(差值:-1.103±0.91;p=0.013)。
- 二甲双胍组与分泌组:脂联素水平未见显著变化。
02、各组治疗在空腹胰岛素和空腹血糖指标上呈现出怎样的变化模式?
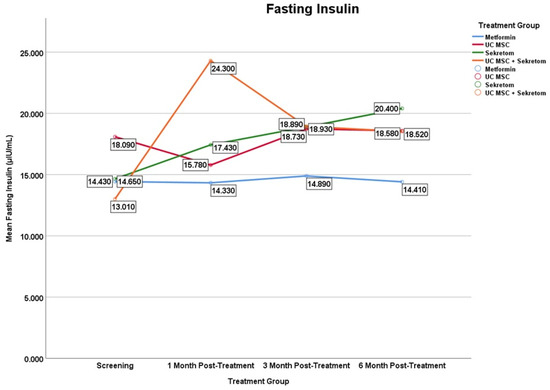
空腹胰岛素:如图5所示,分泌组治疗组和UC-MSC+分泌组联合治疗组的空腹胰岛素水平均显著升高,但起效时间点不同。分泌组在第6个月时(Δ=5750±8.25;p=0.028)达到峰值,而UC-MSC+分泌组在第1个月(11290±18.24µIU/mL ( p=0.047))至第3个月(5920±8.20;p=0.047)达到峰值。二甲双胍单药治疗组和UC-MSC单药治疗组均未观察到显著的纵向变化。
空腹血糖:在为期6个月的随访期内,各治疗组的空腹血糖水平变化呈现出不同的时间模式(图6)。
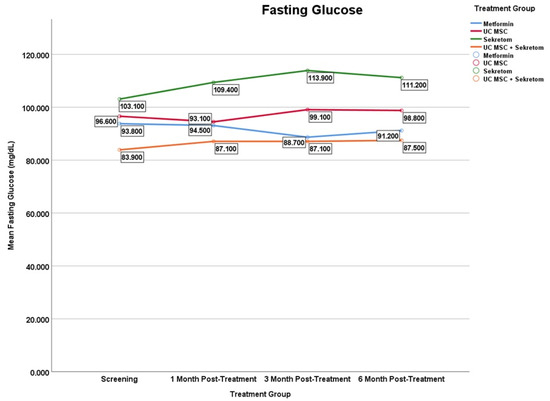
分泌组:是唯一引起血糖显著变化的干预措施,且呈现出持续性升高的趋势:
- 第1个月:显著升高(差值:+6.30±6.52mg/dL;p=0.013)
- 第3个月:显著升高(差值:+10.80±8.55mg/dL;p=0.007)
- 第6个月:显著升高(差值:+8.10±11.23mg/dL;p=0.032)
二甲双胍组、UC-MSC组及联合组:空腹血糖均未见显著变化。
03、胰岛素抵抗指数(HOMA-IR)的变化趋势与上述指标是否一致?
- 完全一致。HOMA-IR的变化进一步印证了分泌组对糖代谢的负面影响。
- 仅分泌组在第6个月出现了HOMA-IR的显著升高(差值:+1.56±2.53;p=0.047)(图7)。
- 其他所有治疗组(二甲双胍、UC-MSC、联合治疗)均未观察到HOMA-IR的显著变化。
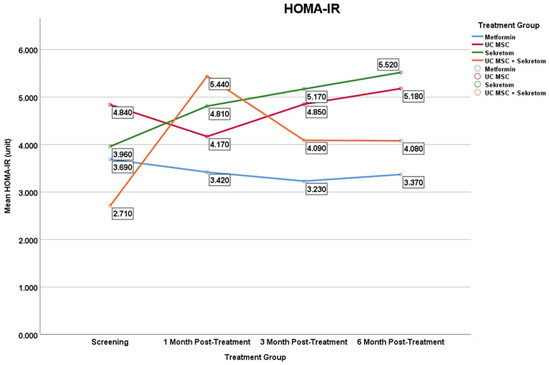
这一结果明确显示,分泌组单独使用在该研究中反而导致了胰岛素抵抗的恶化,研究者将其描述为“矛盾的代谢效应”。
04、经过6个月治疗,各组在月经规律性、排卵和妊娠等临床结局上有何详细差异?
注:以下临床结果为描述性统计,未进行组间假设检验,主要反映趋势。
根据表3,治疗6个月后的临床反应因治疗组而异。
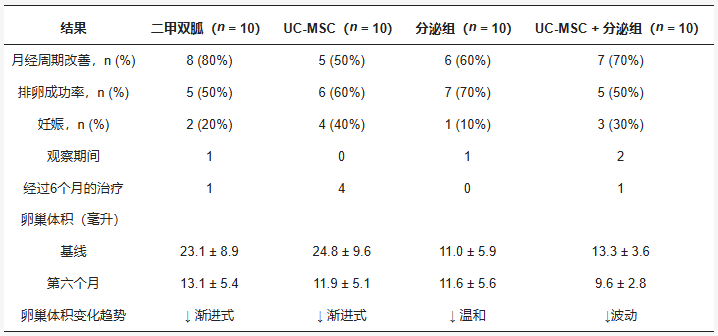
月经周期规律性改善:二甲双胍组改善比例最高(80%)。其次为UC-MSC+分泌组(70%)、分泌组(60%)和UC-MSC组(50%)。
排卵率:分泌组的排卵率最高(70%)。其次是UC-MSC组(60%)。二甲双胍组和联合组均为50%。
妊娠率(最关键的生殖结局):UC-MSC组表现最佳,取得了最高的妊娠率(40%),且所有妊娠均发生在治疗6个月后。其次是UC-MSC+分泌组(30%),但多数病例仍在观察中。二甲双胍组为20%。分泌组最低,仅为10%。
卵巢形态:所有治疗组的平均卵巢体积均较基线有所下降。二甲双胍组和UC-MSC组的下降更为稳定。分泌组和联合治疗组的变化较轻微或呈波动性。
05、综合代谢指标与临床结局,哪一组治疗方案表现最为突出?存在怎样的“分离现象”?
最突出的治疗方案:UC-MSC单药组。
- 代谢层面:虽然UC-MSC组在空腹血糖、胰岛素和HOMA-IR上未显示出显著变化,但它成功提升了保护性脂肪因子脂联素(+0.893),这是改善代谢内分泌环境的积极信号。
- 临床层面:UC-MSC组取得了最高的妊娠率(40%) 和较高的排卵率(60%)。
结论:UC-MSC治疗可能通过改善内分泌环境(如升高脂联素)而非直接调节糖代谢来促进生殖功能的恢复。
值得注意的“分离现象”:分泌组。
- 代谢层面:分泌组在多项指标上(C肽、空腹胰岛素、空腹血糖、HOMA-IR)均显示出恶化趋势,表明其可能加重了胰岛素抵抗。
- 临床层面:尽管代谢指标恶化,分泌组却取得了最高的排卵率(70%)。
解读:这种代谢与生殖结局的分离现象提示,排卵的恢复可能不仅仅依赖于胰岛素敏感性的改善,分泌组中的某些生物活性因子可能直接作用于卵巢功能,但同时也对全身糖代谢产生了干扰。
06、研究中是否观察到与干细胞或分泌组治疗相关的安全性事件?
安全性良好。在为期6个月的随访期内,未观察到与脐带间充质干细胞(UC-MSC)或分泌组给药相关的严重不良事件。这一结果为UC-MSC及分泌组作为PCOS潜在治疗策略的短期安全性提供了初步证据,支持在这一领域开展更大规模的深入研究。
结论
这项随机对照研究表明,UC-MSC疗法和分泌组疗法对伴有胰岛素抵抗的PCOS女性产生了不同的效应。
- UC-MSC单药治疗与最理想的代谢特征相关,表现为脂联素水平的延迟但显著升高,且未引起血糖或胰岛素相关指标的不良变化,并取得了最高的妊娠率。
- 分泌组疗法则与空腹血糖、胰岛素和HOMA-IR的升高相关,提示其可能诱导了代偿性高胰岛素血症而非改善胰岛素敏感性,但其极高的排卵率提示可能存在直接促卵泡发育的作用。
- 联合治疗导致早期但短暂的代谢改变,6个月时未观察到持续获益。
总体而言,UC-MSC单药治疗在本研究队列中显示出更稳定的代谢趋势和最佳的临床妊娠结局。然而,这些发现仍需通过更大样本量的安慰剂对照研究,并结合深入的药代动力学和药效学评估进行进一步验证。
参考资料:
[1]:Prayitno, G.D.; Sartika, C.R.; Djuwantono, T.; Wijaya, A.; Muharam, R.; Hidayat, Y.M.; Haifa, R.; Zahrah, A.; Lestari, K. The Effect of Umbilical Cord-Derived Mesenchymal Stem Cells and Secretome on Metabolomic Profiles (C-Peptide, Adiponectin, Fasting Insulin, and Fasting Glucose): A Randomized Controlled Trial. J. Clin. Med. 2026, 15, 1707. https://doi.org/10.3390/jcm15051707
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信