1型糖尿病(T1DM)是自身免疫攻击胰岛β细胞所致,胰岛素缺乏,血糖居高不下。现行治疗方案包括胰岛素注射、免疫抑制剂联合耐受性疫苗接种、免疫调节剂与β细胞增强药物、细胞因子或基因治疗,异体胰岛移植亦占一席。近年来,间充质干细胞(MSCs)移植被视为有望实现永久性治愈的新策略。
MSCs在再生医学领域应用广泛,具备易于获取、增殖能力强、分化潜能高、致瘤风险低、免疫原性弱等优势。然而,针对T1DM的MSCs临床试验仍为数不多。

11项临床试验证实:间充质干细胞治疗1型糖尿病-护胰岛、调免疫、降糖需
2026年2月28日,《糖尿病与代谢紊乱杂志》在线发表一项系统综述[1],全面梳理2015年至2024年间MSCs治疗T1DM的临床试验。经严格筛选,11篇符合预设标准的原创研究被纳入最终分析。该综述表明,MSCs治疗是T1DM可接受的治疗选择,安全性良好;MSCs有助于维持β细胞功能、调节免疫反应,进而降低胰岛素需求。
研究方法及过程
本研究严格遵循PRISMA(系统评价和荟萃分析的首选报告项目)与MOOSE(流行病学观察性研究的荟萃分析)指南。研究团队制定详细检索策略,采用MeSH标准化关键词,在PubMed和Google Scholar数据库中系统检索2015—2024年发表的文献,关键词组合涵盖“1型糖尿病”“间充质干细胞”“临床试验”等维度。同时,手工检索入选文献的参考文献列表,以最大限度查全相关研究。
文献筛选与数据提取由两名审稿人(SA、MAK)独立完成。两人分别对初检获得的129篇文献进行标题与摘要审阅,依照预先设定的纳入与排除标准进行筛选:纳入标准为关于MSCs治疗T1DM的英文原创临床试验、可获取全文;排除综述、病例报告、会议摘要等。遇分歧时,由第三名研究者(DD)参与讨论并达成共识。
最终,排除118篇无关文献后,对剩余文献进行全文审查,确定最终11项研究纳入系统评价(图1)。
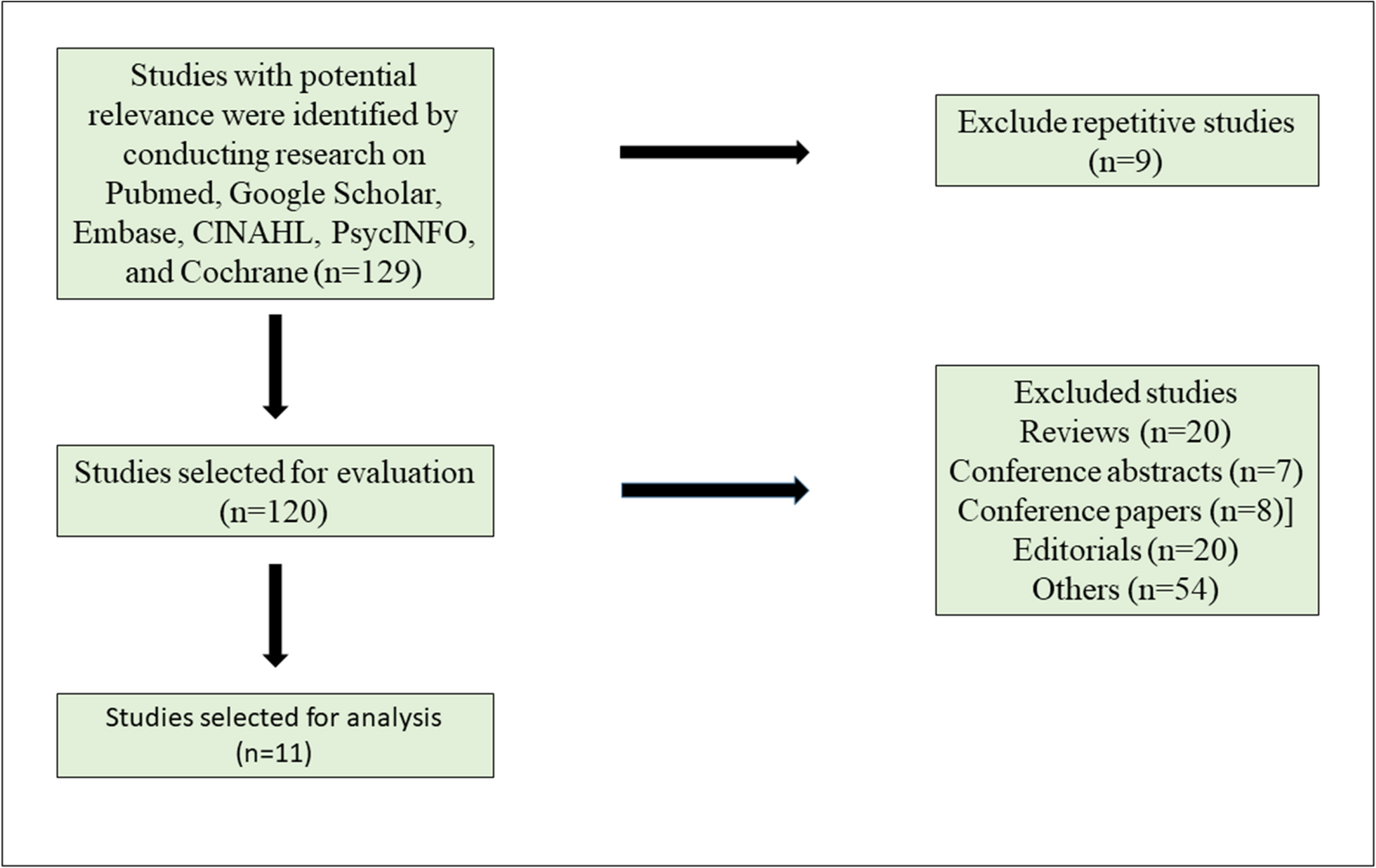
研究结果
1、研究的区域分布与参与者特征
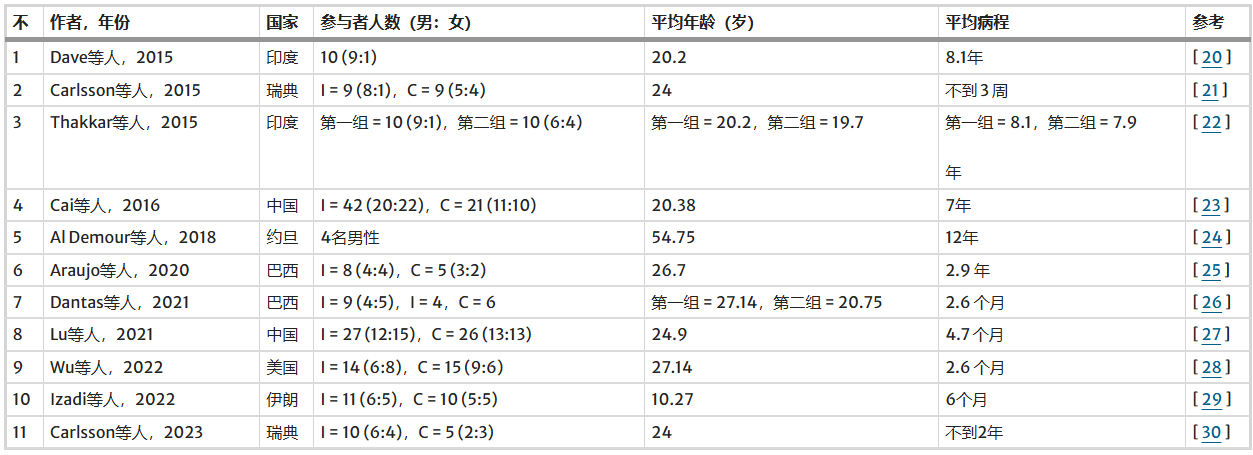
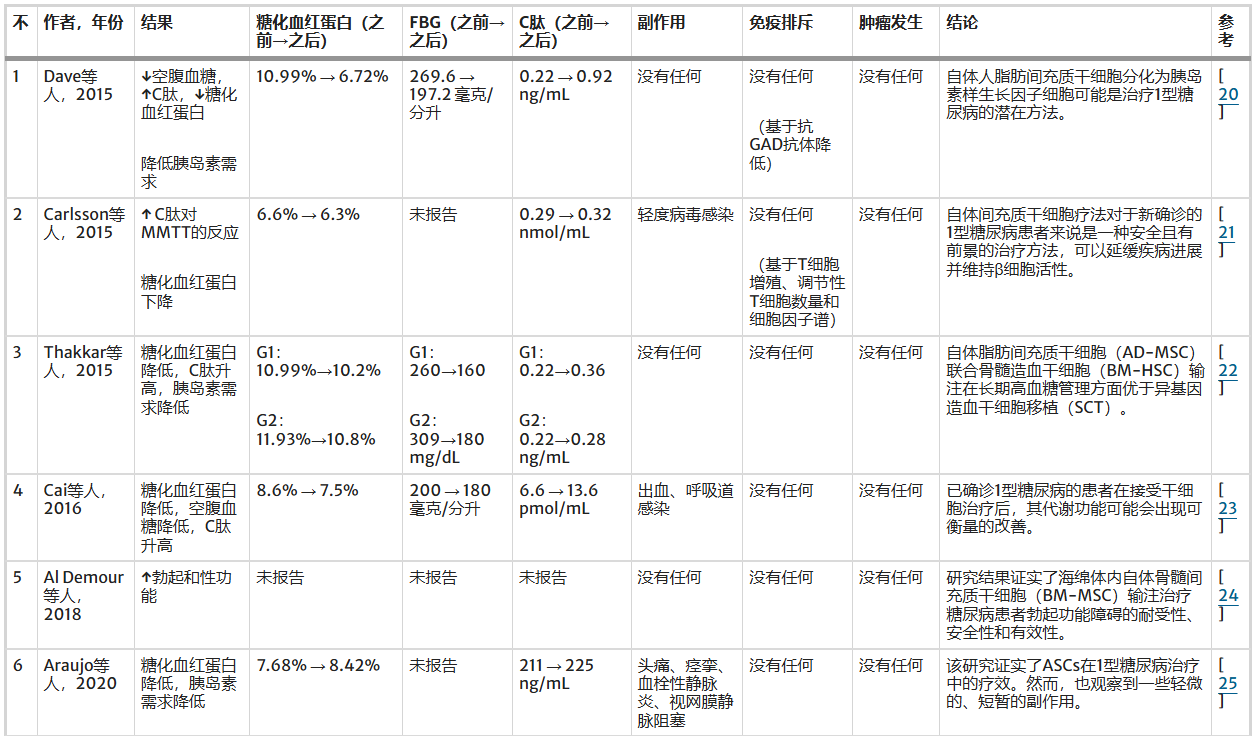
纳入的研究覆盖了多个地理区域,主要集中于亚洲和中东地区(如伊朗、中国、印度、约旦),此外南美洲(巴西)、北美洲(美国)和欧洲(瑞典)也有相关报道。参与者年龄范围从4岁至43岁不等,平均年龄介于10至55岁之间,多数为青年至中年人群,且干预组与对照组的平均年龄基本相当。
性别分布上,大多数队列中男性人数较多。疾病病程差异显著:约45%的试验纳入慢性病患者(平均病程2.9至12年),另45%的研究纳入病程不足一年的短期患者,少数研究(约10%)涉及病程不足两年的患者(表1)。
2、间充质干细胞移植方案的特征
干细胞来源多样,45%的试验使用骨髓来源MSC,18%使用脂肪来源MSC,18%使用脐带血MSC,另有少数研究采用脐带血或两种细胞共移植。移植途径以静脉输注最为常见(54%),其次为门静脉、胸腺、皮下注射或胰动脉注射,少数采用阴茎海绵体注射(表2)。
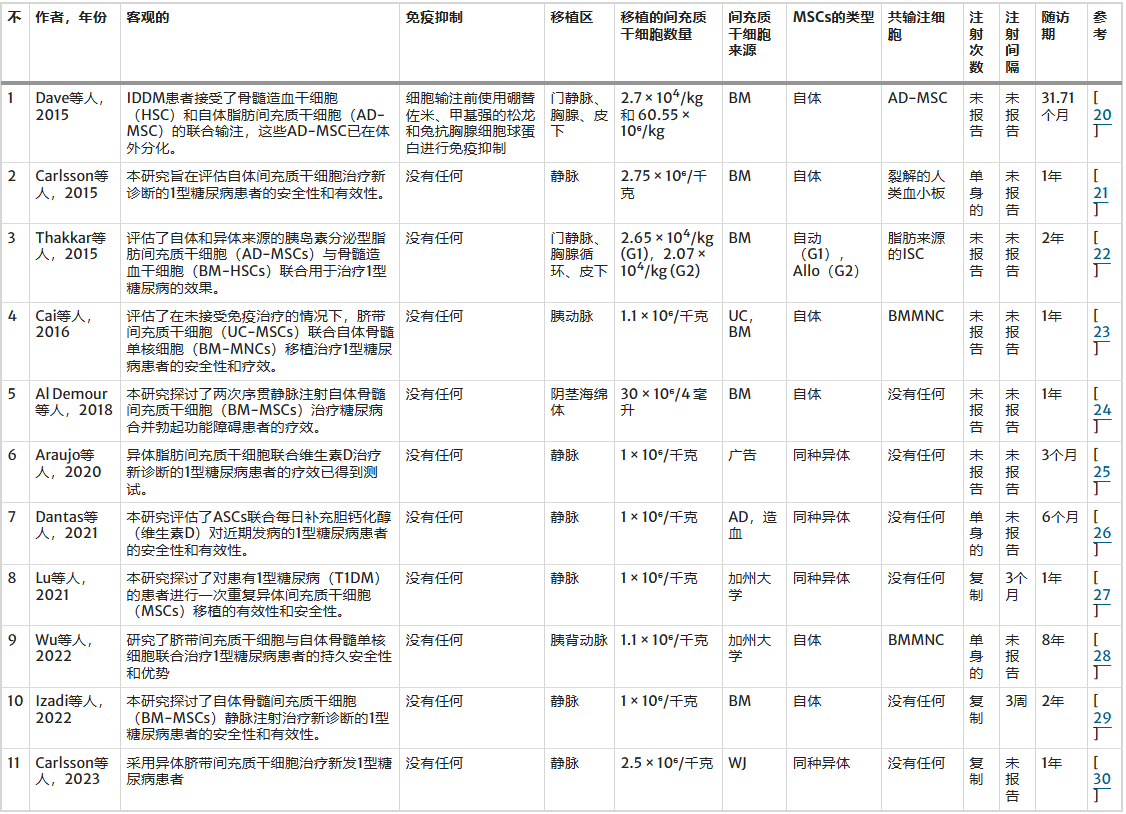
细胞剂量方面,约54%的试验使用1-1.1×10⁶/kg,部分研究(18%)使用2.5-2.75×10⁶/kg,其他剂量较少见(表2)。
移植次数方面,27%的研究采用单次输注,27%采用重复注射,但多数研究(45%)未报告注射次数,注射间隔也大多未明确描述。免疫抑制方案仅在个别试验中应用,大多数研究未使用免疫抑制。共输注其他细胞的情况较少(约36%)(表2)。
3、临床疗效评估:血糖控制与β细胞功能
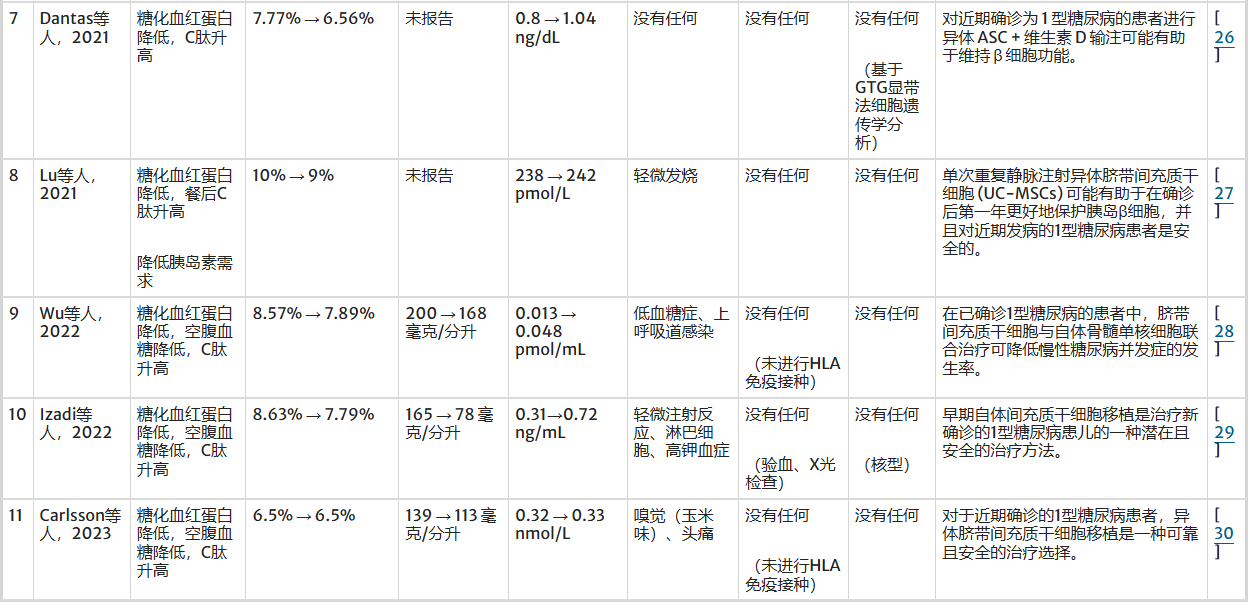
在血糖控制方面,91%的研究观察到MSC治疗后HbA1c水平降低,表明长期血糖控制得到改善;54%的试验报告空腹血糖下降,降幅约20mg/dL至130mg/dL以上。C肽水平作为反映β细胞功能的指标,约73%的研究显示治疗后C肽水平略有升高,提示β细胞活性改善或维持。这些结果一致支持MSC治疗对1型糖尿病患者的血糖代谢具有积极影响。
4、安全性与不良事件
MSC移植总体耐受性良好,约54%的研究未报告任何不良反应。出现的不良反应多为轻中度,包括短暂发热、头痛、轻微感染、注射部位反应及暂时性实验室异常(如淋巴细胞计数升高、高钾血症)。
罕见严重不良事件,仅个别研究报道低血糖或嗅觉改变。免疫排斥反应评估方法各异(如抗GAD抗体、T细胞增殖等),但所有研究均显示MSC治疗与极低的免疫排斥相关。尤为重要的是,所有研究在随访期内均未发现肿瘤形成或恶性转化的证据,证实了MSC治疗的安全性。
讨论
基于1型糖尿病的病理特征,间充质干细胞(MSCs)治疗的科学依据和核心优势是什么?
T1DM的根本病理是β细胞数量减少。传统胰岛素治疗虽能维持生命,却存在低血糖风险、血糖控制欠精确及沉重经济负担,亟需更根本的策略。MSCs之所以成为研究焦点,源于其多重治疗机制。
首先,MSCs具备分化潜能,为直接替代受损的β细胞提供了理论可能。但更重要的是其旁分泌作用:它们能分泌生长因子、细胞因子和外泌体,这些生物活性物质能够促进受损组织的修复、诱导血管生成、抑制细胞凋亡,并发挥关键的免疫调节功能。MSCs能够迁移至炎症部位,促进调节性T细胞的生成,从而抑制攻击胰岛的自身免疫反应,从根源上保护或保留残存的β细胞功能。
此外,讨论特别指出,与某些类型的干细胞不同,现有证据表明MSCs在临床应用中没有肿瘤形成的风险,并且已在众多临床试验中展现出良好的安全性,这构成了其作为治疗新策略的核心优势。
在移植策略上,自体移植与异体移植各有什么利弊?为何在没有免疫抑制的情况下异体移植也能成功?
回答:讨论详细对比了两种移植模式。异基因移植(AlSCT) 理论上能提供一个全新的、不攻击β细胞的免疫系统,但其临床应用面临巨大挑战:需要严格的HLA配型、长期的免疫抑制治疗,且移植排斥和感染风险高。
相比之下,自体干细胞移植(ASCT) 使用患者自身的细胞,从根本上规避了初始的移植排斥反应,因此通常不需要免疫抑制。然而,其缺点是移植的细胞仍可能再次成为自身免疫攻击的目标,可能需要定期重复移植以维持疗效。
本综述的数据显示,在纳入的研究中,自体移植占比更高(54.54%),这与其避免免疫排斥和HLA配型困难的优点相符。然而,一个非常关键的发现是:除了极少数研究(9.09%)外,高达90.91%的试验均未使用免疫抑制方案,这其中既包括自体移植,也包括异体移植。这表明,无论采用何种移植方式,MSCs本身强大的免疫调节特性可能足以在不需要强力免疫抑制药物的情况下,为自身创造一个相对宽容的微环境,从而成功实现治疗。
因此得出结论,尽管存在理论上的风险,但现有证据表明,无需免疫抑制的异体MSC移植在控制1型糖尿病方面同样具有极佳的疗效,这为简化治疗方案和扩大细胞来源提供了重要依据。
三、细胞来源、共输注策略与移植参数如何影响疗效?优化方向何在?
MSCs来源、辅助策略与技术参数共同决定治疗成败。
细胞来源与特性:不同来源MSCs生物学特性各异。骨髓来源(BM-MSCs)最常用(45.45%),优势在于强大归巢与免疫调节能力,但采集有创且细胞质量随供体年龄下降。脂肪来源(AD-MSCs)采集无创、增殖率高,但免疫调节作用略逊。脐带/脐带血来源(UC-MSCs/WJ-MSCs)属年轻细胞,免疫原性低、增殖快,但归巢能力相对较弱。尽管特性有别,各类MSCs在治疗中均取得满意效果,提示可根据患者具体情况灵活选择。
共输注策略:部分研究尝试联合移植。与骨髓单核细胞共输注可改善归巢能力、增强免疫调节;与血小板裂解物共输注,其富含的生长因子可提高MSCs存活率;甚至将两种不同类型MSCs共移植,以期更全面改善β细胞保存、减少自身免疫攻击。
移植技术参数:
注射途径:静脉输注(54.54%)最为简便,但面临细胞易滞留于肺部、归巢效率低的问题。胰动脉/门静脉注射能更精准递送细胞至胰腺,增强局部免疫调节,但有创且存在血栓风险。胸腺注射旨在诱导中枢免疫耐受,但受限于胸腺萎缩和操作创伤。皮下注射相对安全,可作为细胞储存的“免疫豁免”区域。部分研究(如Thakkar、Dave等)尝试多部位联合注射,综合不同途径优势,提高细胞存活率与功能。
细胞剂量:多数研究(63.63%)使用了低于3×10⁶/kg的剂量,这与文献中推荐的理想剂量(1-2×10⁶/kg)相符,因为过高剂量可能增加栓塞和免疫反应的风险。
注射频次:这是当前研究的薄弱环节。由于单次注射的MSCs大多在短期内(24-72小时)被清除,其有益作用(主要是旁分泌效应)持续时间有限(约1-2周)。因此,讨论明确提出,实现永久性T1DM治疗很可能需要按照明确的时间间隔进行多次注射。然而,现有研究中超过半数未报告注射次数和间隔,这凸显了未来在方案标准化上的巨大缺口。
问题四:现有临床证据如何评估MSCs治疗1型糖尿病的有效性与安全性?具体体现在哪些指标上?
有效性证据:所有被综述的研究均显示出积极的临床改善信号。具体体现在:降低空腹血糖(FBG) 和降低糖化血红蛋白(HbA1c) 水平,表明长期血糖控制得到改善;减少外源性胰岛素的注射需求,这是患者最直接的获益;以及提高或维持C肽水平,C肽是反映胰岛β细胞功能的金标准,其水平升高或稳定表明MSCs治疗有助于改善或保护了残存的β细胞功能。
安全性证据:MSCs移植总体耐受性良好。
不良反应:约54%的研究未报告任何不良反应。出现的不良反应多为轻度至中度,如一过性发热、头痛、轻微感染、注射部位反应和短暂的实验室检查异常。严重不良事件极为罕见。
免疫排斥:尽管评估方法各异(如检测抗GAD抗体、T细胞增殖反应、调节性T细胞计数等),但所有研究均显示MSCs治疗与极低的免疫排斥反应相关,再次印证了其强大的免疫调节能力。
肿瘤发生:这是干细胞治疗中最受关注的远期风险。本综述给出了一个关键的安全信号:在所有评估的研究中,其各自的随访期内均未发现任何肿瘤形成或恶性转化的证据,这为MSCs的临床应用提供了重要的安全保障。
问题五:现有证据如何评估MSCs治疗T1DM的安全性与有效性?未来研究需要克服哪些挑战?
讨论指出,所有被综述的研究均显示出积极的有效性信号,包括降低空腹血糖(FBG)和糖化血红蛋白(HbA1c)、减少胰岛素需求以及提高C肽水平,表明MSCs有助于改善或维持β细胞功能。
在安全性方面,MSCs移植通常耐受性良好,不良反应多为轻度至中度(如短暂发热、注射部位反应),严重不良事件罕见。尤为重要的是,所有研究在随访期内均未观察到肿瘤发生,并且通过免疫学检测证实了极低的免疫排斥反应。
尽管前景光明,讨论也指出了未来研究需要克服的关键挑战:
- 标准化缺失:MSCs的制备、剂量、注射次数和间隔缺乏统一标准,导致研究间存在差异,阻碍了结果的比较和推广。
- 长期疗效未知:对移植后MSCs在人体内的长期存活状态、分布及功能知之甚少。
- 供体异质性与微环境:供体来源的差异和患者体内不利的微环境影响MSCs的存活率和疗效的可靠性。
- 伦理与大规模生产:基于细胞的疗法涉及伦理问题,且大规模生产符合严格质量标准的MSCs仍具复杂性。因此,未来需要更多大样本、设计严谨的临床试验,并在临床前和临床研究中加强对免疫原性和致瘤性的深入评估。
结论
间充质干细胞疗法为1型糖尿病治疗开辟了新路径。现有证据表明,MSCs有助于维持β细胞功能、调节免疫反应、降低胰岛素需求,且安全性良好。然而,当前研究受限于样本量小、试验设计多样、随访时间短。
未来亟需开展更大样本、更标准化设计、更长随访的临床试验,以全面评估其疗效与安全性,推动MSCs疗法从实验室走向临床,惠及广大患者。
参考资料:
[1]:Dayer, D., Ahadi, S. & Khaksar, M.A. A systematic review of clinical trials in mesenchymal stem cell therapy for type 1 diabetes mellitus. J Diabetes Metab Disord 25, 93 (2026). https://doi.org/10.1007/s40200-026-01920-9
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信