老年衰弱是一种显著缩短老年人健康寿命的临床综合征,目前临床干预手段十分有限。2026年2月25日,一项关于人骨髓来源间充质干细胞(laromestrocel)治疗老年衰弱的IIb期剂量递增试验结果发表于《Cell Stem Cell》[1]。

该研究共纳入148例老年衰弱患者,结果证实:与安慰剂相比,laromestrocel输注可使6分钟步行试验(6MWT,主要终点)距离出现具有临床意义的改善,且呈明确的剂量与时间依赖性——第6个月增加41.3米,第9个月增加63.4米。6MWT的改善与患者报告的身体功能评分(PROMIS)显著相关。
此外,laromestrocel剂量与可溶性TIE2(血管生成素受体,反映血管功能的关键分子)水平下降呈正相关,提示sTIE2可作为预测治疗应答的潜在生物标志物。上述发现为干细胞疗法改善老年衰弱患者行动能力及整体功能状态提供了直接证据。

老年衰弱的定义与可干预性
老年衰弱是一种独立于正常衰老的多系统退行性状态,核心特征是个体因生理储备下降而对压力源的脆弱性显著增加。它并非单纯的衰老,而是一种具有潜在可逆性的病理状态,主要外在表现为身体机能的下降,尤其体现在力量和耐力的减退,例如在6分钟步行试验中表现不佳,进而导致行动能力受限、生活质量降低。
从内在机制看,衰弱涉及慢性炎症(炎症衰老)、血管内皮功能障碍、骨骼肌功能异常以及多种干细胞(如肌肉、神经干细胞)数量和更新能力的下降。这种状态导致老年人面临极高的不良健康结局风险,包括残疾、痴呆、住院、死亡等,并消耗大量医疗资源。值得注意的是,它不同于不可逆的衰老,具有潜在的可逆性,这意味着通过针对性的干预(如改善炎症、干细胞修复等),衰弱的状况可能得到改善。
“基于这种可逆性的理论基础,针对上述病理机制的干预研究正在开展。以下报告了一项具体的干细胞疗法探索。”
Laromestrocel干细胞疗法的IIb期研究及其生物学证据
这项IIb期剂量探索研究评估了名为laromestrocel(Lomecel-B)的异体间充质干细胞制剂在70至85岁无痴呆的老年衰弱患者中的疗效。Laromestrocel通过多种作用机制,针对衰弱的核心病理环节,包括炎症衰老、血管功能障碍及骨骼肌能量代谢减退。作为一种同种异体干细胞疗法,它具有获取便捷和安全性高的优势;其前期研究已在阿尔茨海默病中显示出减少脑萎缩和改善认知的潜力,且提示具有抗炎作用。
本研究基于前期探索中发现的6分钟步行试验变化,旨在系统评估laromestrocel在改善老年衰弱患者身体功能方面的剂量反应关系,并同步探索患者报告结局及相关的血管功能生物标志物。研究发现,一种与血管功能和炎症相关的候选生物标志物——可溶性酪氨酸激酶(sTIE2)的水平变化,与laromestrocel的输注剂量呈现明确的反应关系,这为干细胞疗法通过改善血管功能来干预老年衰弱提供了初步的生物学证据。
研究人群与分组
该研究从2017年8月至2020年2月期间进行,共筛查了365例患者,最终155例符合纳入标准的老年衰弱患者被随机分组(图1)。筛选失败的主要原因是TNF-α水平低于2.5pg/mL(约占26.9%),其他原因包括乙型肝炎病毒阳性、6分钟步行试验距离超出范围及HbA1c过高。最终148例受试者接受了单次研究药物输注并纳入安全性分析,其中137例完成了试验,完成率为95.8%。
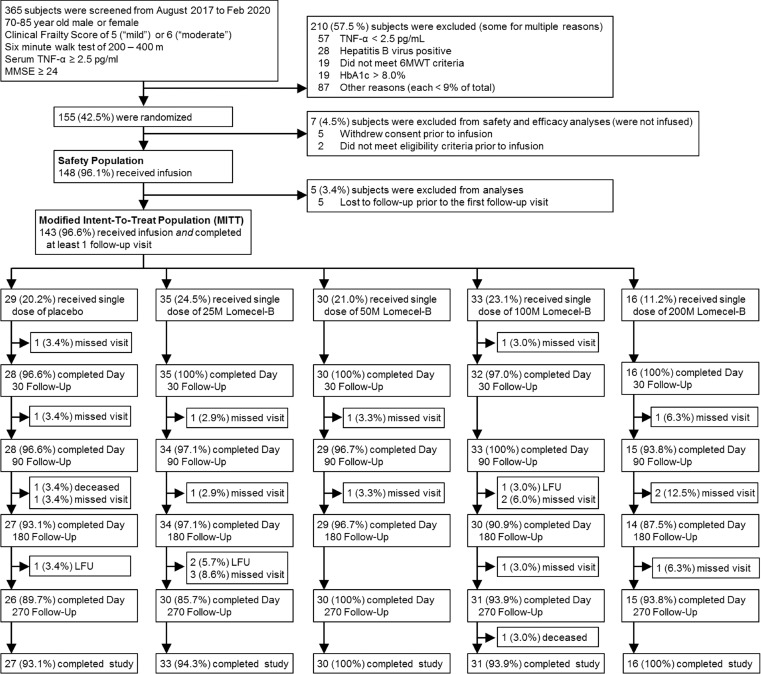
疗效分析采用改良意向性治疗人群,共143例患者被分为五组:安慰剂组(29例)、2500万干细胞组(35例)、5000万干细胞组(30例)、1亿干细胞组(33例)和2亿干细胞组(16例)。各组基线特征均衡,参与者平均年龄74.3至76.8岁,女性占20.6%至53.3%,整体虚弱程度为轻度至中度,临床虚弱量表平均得分为5.1分。
疗效证据之一:6分钟步行距离的剂量依赖性改善
这项研究的主要终点评估了laromestrocel各剂量组与安慰剂组在输注后6个月时6分钟步行试验(6MWT)距离的变化。虽然各活性剂量组在数值上均有改善,但单独与安慰剂组相比未达到统计学显著性。然而,研究预先设定的剂量反应分析显示,laromestrocel的剂量增加与6个月时6MWT距离的改善之间存在显著的线性关系,表明疗效存在明确的剂量依赖性趋势。在第6个月时,最高剂量(200M)组与安慰剂组的6MWT差异达到41.3米,接近统计学显著性(p=0.0635)(图2)。
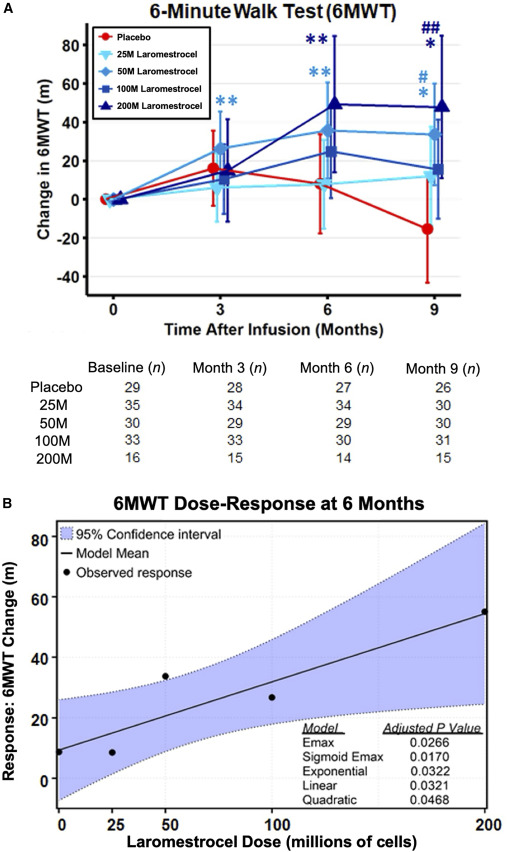
(A) mITT人群中6分钟步行试验(6MWT)距离随时间的变化。所有四个拉罗美司特罗组均显示步行距离呈增加趋势或显著增加,其中200M剂量组的基线变化最大。相比之下,安慰剂组在治疗后9个月时步行距离呈下降趋势。
(B)采用多重比较程序建模(MCP-Mod)方法计算6个月时的剂量反应效应。所有五个模型均具有统计学意义,但线性模型的AIC值最小,表明它是最简约的预测模型。
研究进一步分析了所有时间点的完整剂量反应关系,发现治疗效果呈现出时间依赖性的持续增强。至输注后第9个月,高剂量组与安慰剂组的差异达到统计学意义:200M剂量组较安慰剂组多走63.4米,50M剂量组多走49.2米。
此外,从各组自身基线的改善来看,50M、100M和200M剂量组在6个月时均显示出显著的6MWT距离增加,50M和200M剂量组在9个月时仍保持显著改善,而安慰剂组在任何时间点均无显著变化。性别和BMI分层分析显示,这些人口统计学因素均不影响laromestrocel的疗效。
患者报告结局与临床虚弱状态的综合改善
这项研究通过患者报告结局测量信息系统(PROMIS)量表评估了患者自我感知的身体功能变化。虽然各治疗组的PROMIS评分与安慰剂组相比未达到统计学显著性差异,但研究发现PROMIS评分与客观测量的6分钟步行试验(6MWT)距离变化之间存在显著的正相关性。
将所有治疗组与安慰剂组合并分析后,输注后第6个月,PROMIS SF-20身体功能量表与6MWT变化的Pearson相关系数为0.3124(p=0.0002),而6MWT原始值与PROMIS评分的相关性更强,达到0.44(p<0.0001)。此外,6MWT与PROMIS活动能力量表及上肢功能量表也均呈现显著正相关。这表明,患者自我报告的身体功能改善与其客观步行能力的提升是一致的(图3)。
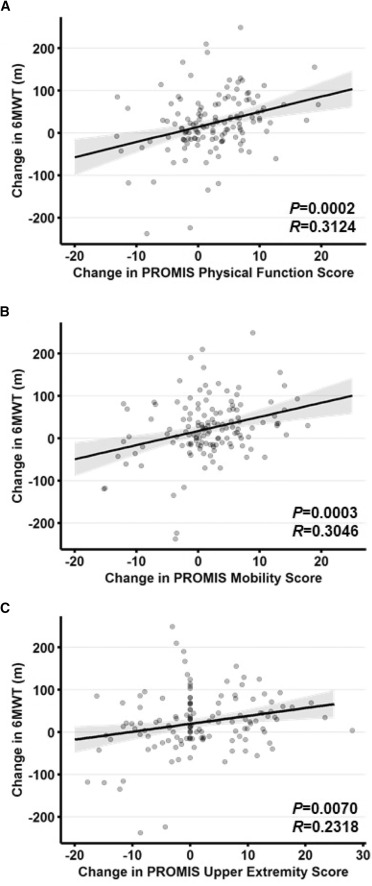
(A在mITT人群中,治疗后6个月PROMIS身体功能SF20的变化(被选为次要终点)与6MWT的变化显著相关。
(B和C)PROMIS活动能力和PROMIS上肢的变化均与治疗后6个月6MWT的变化显著相关。
研究还采用加拿大健康与老龄化研究临床虚弱量表(CSHA-CFS)评估了laromestrocel对患者整体虚弱状态的影响。根据CFS评分将受试者分为三类后分析发现,laromestrocel治疗组中改善至健康状况良好状态(CFS 2-3级)的患者比例显著高于安慰剂组。
输注后第9个月,安慰剂组仅有14.8%的受试者改善至CFS2-3级,而laromestrocel治疗组这一比例达到30.8%,同时安慰剂组进展至中度虚弱(CFS 6级)的比例也相应更高。这一结果表明,laromestrocel治疗可能为老年衰弱患者带来具有临床意义的整体状态改善。
什么是sTIE2?为什么要选用sTIE2作为活性生物标志物?
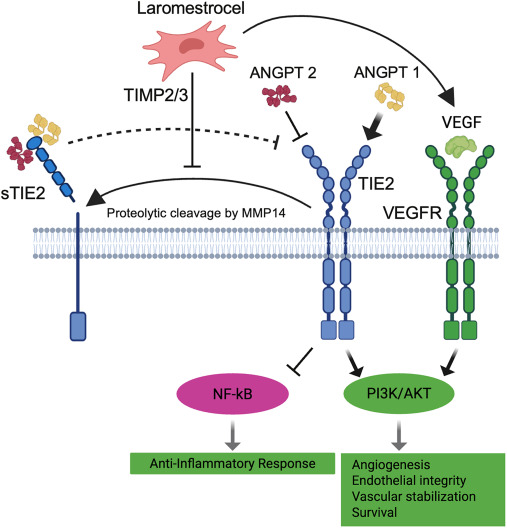
sTIE2(可溶性TIE2)是TIE2受体的可溶形式。TIE2(又称TEK)是一种主要存在于微血管内皮细胞和内皮祖细胞上的酪氨酸激酶受体,通过与血管生成素ANGPT1和ANGPT2结合而被激活。ANGPT1和ANGPT2通常以拮抗方式发挥作用,共同平衡血管健康、血管生成及炎症反应。
因此,TIE2位于血管生成/血管健康与炎症通路交汇处的关键节点。当TIE2被基质金属蛋白酶(MMPs)切割后,就会以sTIE2的形式释放到血液循环中,其水平升高反映了这一关键细胞表面信号通路受体的降解。本研究选用sTIE2作为活性生物标志物,是因为它在探索的多种血管/炎症生物标志物中,唯一同时满足两个核心标准:一是能够预测laromestrocel治疗的功能性结果,二是其变化与laromestrocel剂量呈现明确的反应关系。
sTIE2作为活性生物标志物能说明什么问题?
sTIE2的变化能够说明laromestrocel可能通过保护血管内皮细胞表面的TIE2受体,进而改善血管功能和调节炎症。研究发现,laromestrocel能够大量分泌金属蛋白酶组织抑制剂TIMP2(即MMPs的抑制剂),从而可能抑制MMPs对TIE2的切割,减少TIE2受体的降解。
研究数据证实,在laromestrocel治疗组中,sTIE2水平较安慰剂组显著降低(如100M剂量组在6个月和9个月时均显著低于安慰剂组),且这种降低呈现明确的剂量反应关系(Emax模型显示在50M剂量出现平台期)(图4)。
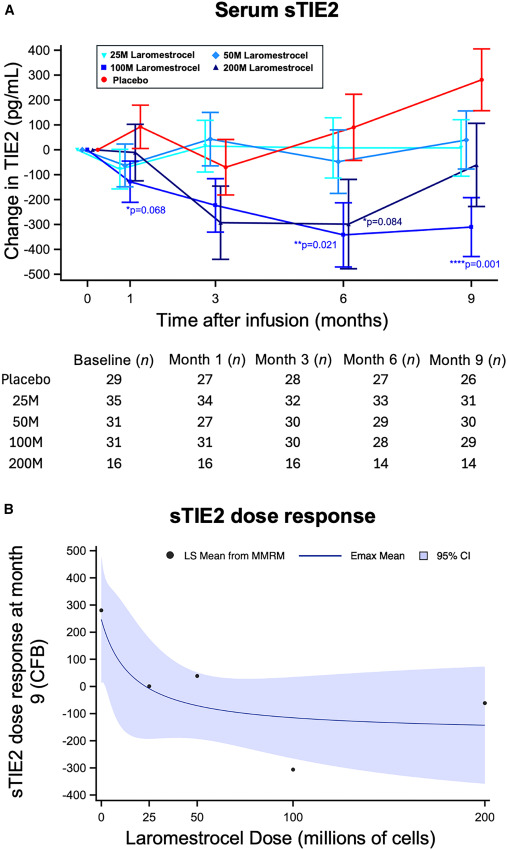
这表明,laromestrocel可能通过TIMP2介导的机制保护TIE2受体完整性,从而维持血管稳态和抗炎平衡。sTIE2的降低为干细胞疗法通过改善血管功能、调节炎症来干预老年衰弱提供了直接的生物学证据,并与临床上观察到的6分钟步行试验改善相呼应。
安全性与产品批次一致性评估
本研究未发现安全性隐患。各治疗组严重不良事件发生率相似,两例死亡(一例肺栓塞、一例合并症)均判定与研究无关。输注过程中仅有两例短暂中断,所有输注相关事件均被判定无关。跌倒、骨折、住院率在组间无显著差异。
为排除产品效价变异对结果的影响,研究者采用重复测量混合效应模型,分析批次对6MWT、CFS及PROMIS评分的影响。结果显示,批次的主效应及其与治疗的交互作用均不显著,表明各批次laromestrocel效价一致,疗效差异非批次差异所致,为后续研究与应用提供了质量依据。
综合发现:疗效的临床意义与机制解析
本研究核心发现可归纳为四点:
其一,单次输注laromestrocel可呈剂量依赖性提高轻度至中度衰弱老年人的步行能力,最高剂量组较安慰剂组多走63.4米,超过既往研究确立的最小临床重要差异(20~30米)。
其二,这一改善持续至输注后9个月,提示干细胞可能触发持续的生物学效应或下游修复过程。
其三,血清sTIE2水平呈剂量依赖性降低,为抗血管内皮损伤机制提供了分子证据(图5)。
其四,客观步行能力与主观身体功能及整体虚弱状态改善相印证,治疗组中健康状态转化率明显高于对照组。
为何握力未见改善,而6MWT改善显著?
一种合理的机制解释是:6分钟步行主要依赖I型慢肌纤维,该纤维血管丰富、线粒体密集,对促血管生成信号敏感;而握力等测试主要涉及II型快肌纤维,依赖无氧代谢,血管分布较少。Laromestrocel的促血管活性可能优先作用于I型纤维,从而提升耐力表现。这一假设与sTIE2降低所提示的血管保护作用相契合,也为后续研究提供了方向。
参考资料:
[1]:Ruiz JG, Oliva AA Jr, Ramdas KN, et al. Randomized phase 2b dose-escalation trial of stem cell therapy with laromestrocel for aging frailty. Cell Stem Cell. 2026 Feb:S1934-5909(26)00040-8. DOI: 10.1016/j.stem.2026.01.017. PMID: 41747733.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信