摘要:尽管干细胞疗法在历年来的发展日新月异,但安全性、伦理性和监管始终是保障患者安全的关键。了解干细胞、细胞疗法或间充质干细胞的伦理获取、开发和监管方式,将有助于患者做出明智的选择。
干细胞疗法已从抽象概念走向现实应用,为关节退行性疾病、自身免疫性疾病等患者提供了长期治愈的可能,而不仅仅是缓解症状。然而,随着全球干细胞临床转化的加速,安全性争议、伦理困境以及监管政策的“松紧带”效应,正成为2026年患者必须正视的新课题。
因此,到了2026年,患者不再仅仅问“它有效吗?”,他们还会问“它安全、合乎伦理且科学可靠吗? ”。本文章将结合2026年最新的国内外政策与真实案例,指导患者了解他们需要知道的有关干细胞和细胞疗法的安全性、伦理和监管方面的信息。
一、了解干细胞治疗中安全的重要性:从“实验室标准”到“真实世界证据”
在进行任何细胞疗法(包括干细胞疗法)时,安全性是成功进行再生治疗的基础,并且取决于几个受控的临床因素:
- 对间充质干细胞(MSCs)进行适当的筛选和鉴定,以确保其活力、纯度和再生潜能。
- 受控的实验室处理流程,以防止污染并维持无菌条件。
- 精准给药和靶向给药方法可减少不良反应并提高治疗效果。
- 根据病史仔细筛选患者,以避免不适宜或高风险的应用。
2026年政策与案例洞察:
安全性验证正在从“理论要求”走向“真实世界数据强制收集”。2026年初,海南博鳌乐城正式将“脐带间充质干细胞治疗膝骨关节炎”纳入真实世界研究项目,这意味着干细胞疗法的有效性不再仅依赖小规模临床试验,而是必须在实际临床应用中接受持续性监测。
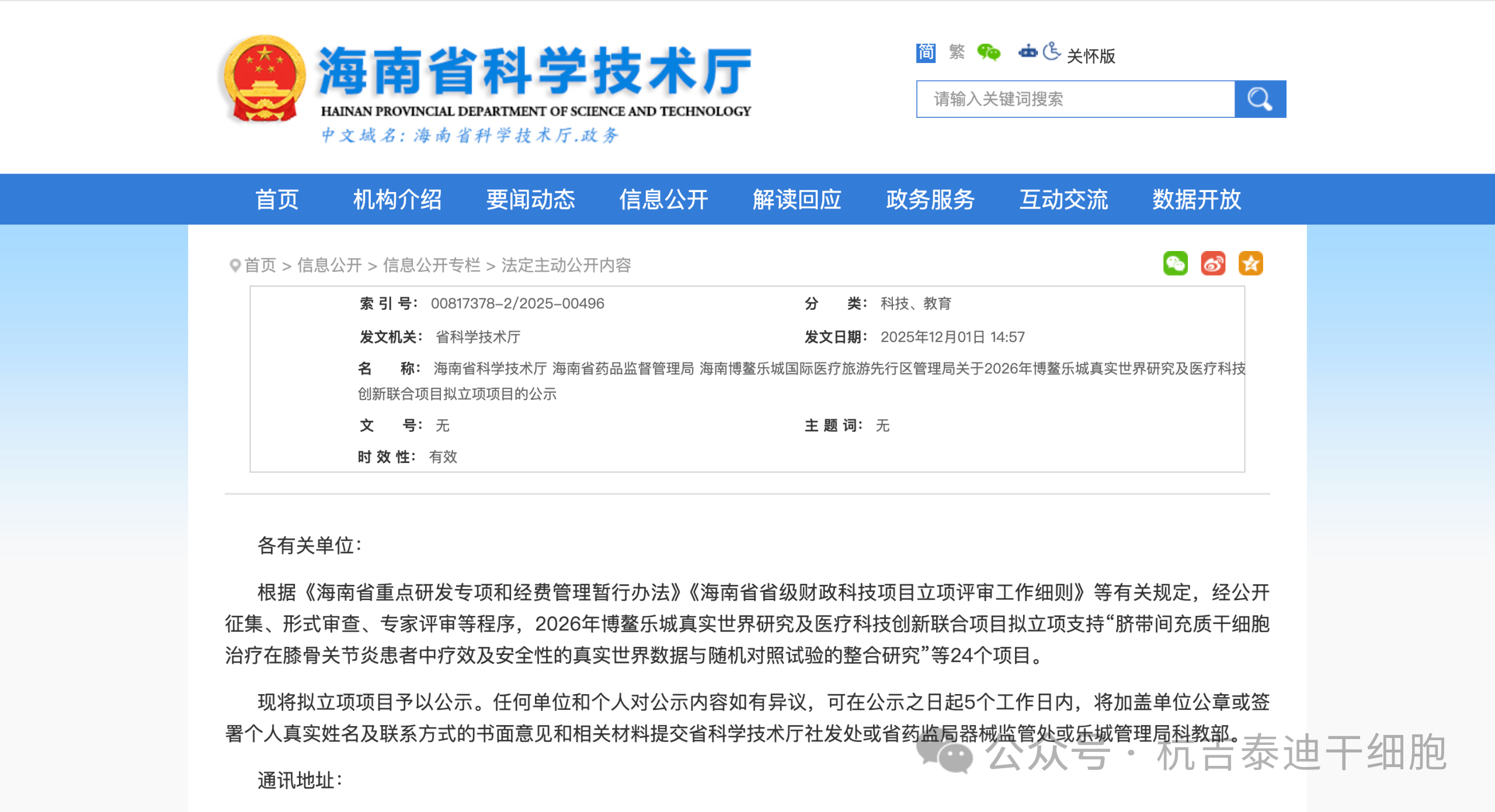
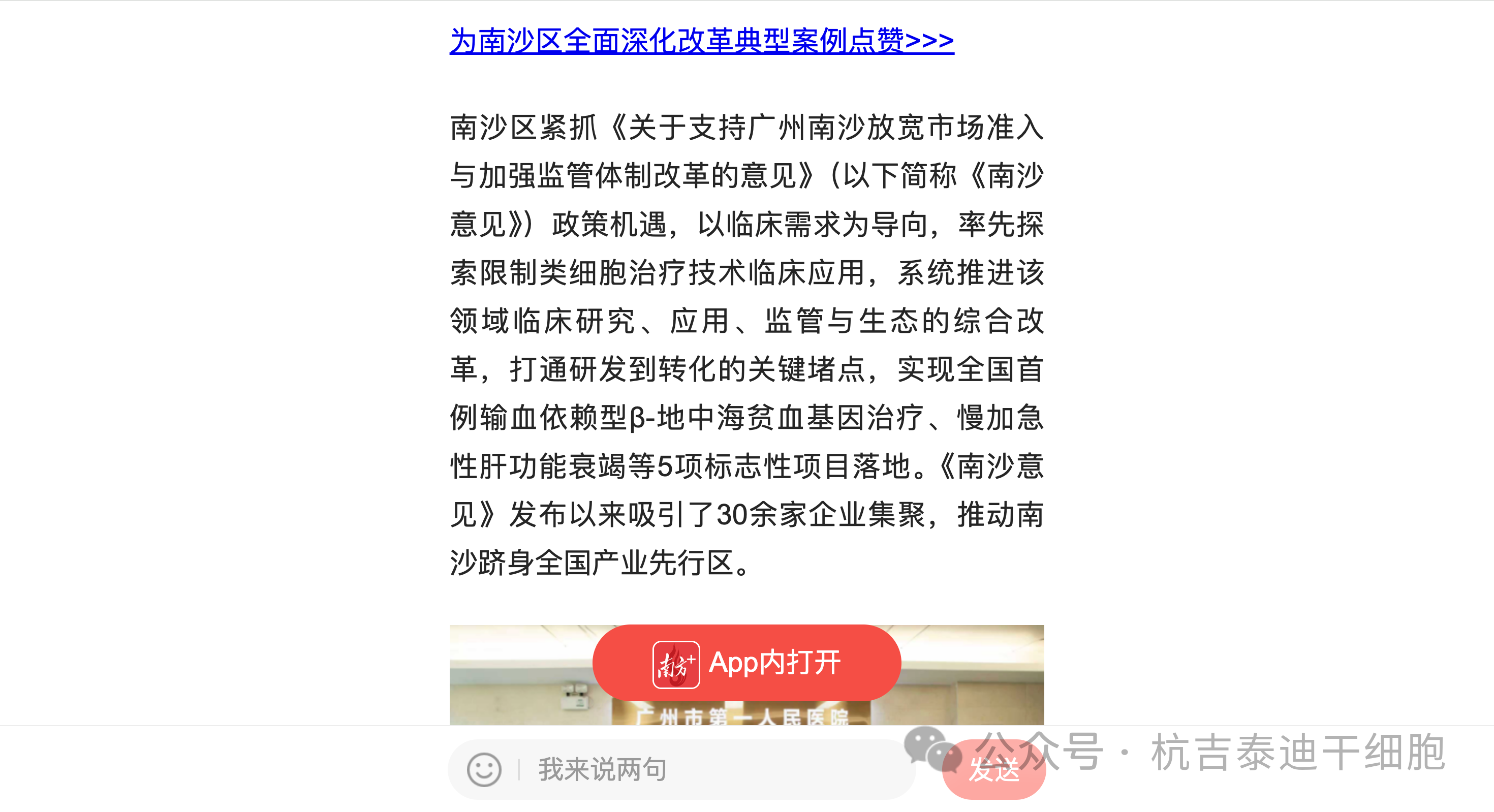
同期,广州南沙完成了全国首例输血依赖型β-地中海贫血基因治疗及异体干细胞治疗肝衰竭,72例地贫治疗患者中已有31例彻底脱离输血依赖。这些突破的背后,是严格的患者筛查、无菌制备及长期随访体系在支撑——这正是安全落地的关键。
反面警示:
安全并非天然伴随新技术而来。日本“快速审批”框架下的脊髓损伤疗法Stemirac,2024年因同类产品HeartSheet在确证性试验中显示治疗组死亡风险是对照组的1.9倍而被撤销批准,Stemirac自身也面临2025年底能否通过确证试验的生死关。这一案例向2026年的患者发出明确信号:仅凭“政府批准”或“已上市”不足以判断安全,必须核实是否有强制性的长期随访数据。
现代再生医学强调最大限度地减少免疫反应、感染风险和不可预测的后果。到2026年,安全规程正通过真实世界证据体系实现标准化与个体化的平衡。
二、为什么我们需要细胞疗法的伦理基础?从“获取透明”到“政策博弈”
伦理规范确保再生医学以患者利益为导向,不会辜负患者的希望。干细胞疗法的伦理遵循以下准则:
- 透明且自愿的捐赠者同意。
- 以合乎伦理的方式,在不使用武力的情况下获取干细胞。
- 沟通中的诚实在于权衡利弊。
- 远离毫无根据和未经证实的说法。
间充质干细胞因其再生特性而被广泛应用,且在来源(如脐带、胎盘)与应用方式合理的情况下,伦理问题相对较少。然而,2026年的伦理语境已发生重要变化。
2026年伦理争议焦点:
2026年1月,美国国立卫生研究院(NIH)突然颁布新政,终止对“人胎儿组织研究”的联邦资金支持。国际干细胞研究学会(ISSCR)立即发表声明反对,指出胎儿组织来源的细胞系在过去一个世纪中对疫苗开发、神经退行性疾病研究至关重要,且此类研究长期受严格的伦理框架(知情同意、非营利性捐赠)约束。

这一事件向患者揭示了一个深层事实:干细胞的“伦理安全”不仅取决于来源本身,还受到公共卫生
政策波动的影响。当某种干细胞来源突然被政治或法规切断,依赖该来源的在研疗法可能面临中断风险。
来自临床一线的伦理实践:
2026年1月,海南博鳌乐城完成了首例类风湿关节炎脐带间充质干细胞治疗。该技术此前已完成三期临床试验,且单次治疗费用仅为美国同类疗法的1/5,通过“按疗效付费”等创新支付模式减轻患者负担。合乎伦理的实践不仅关乎“细胞怎么来”,更关乎患者是否因经济门槛被排除在创新疗法之外。

符合伦理的实践能够保护患者免受误导性治疗,并建立人们对细胞疗法的信任。
三、干细胞治疗的监管:全球化协调与“区域性试验田”
监管的作用在于区分循证医学和高风险实验。监管框架的主要关注领域包括:
- 干细胞处理的质量控制
- 治疗方案的记录
- 临床随访和结果监测
- 符合生物医学安全标准
2026年监管格局新特征:
全球范围内的监管协调程度有所提高,但呈现出 “成熟市场收紧、亚洲先行区试点突破” 的分化态势。
中国的“先行先试”经验:
- 海南博鳌乐城:依托“特许医疗”政策,2026年已密集落地类风湿关节炎干细胞治疗、膝骨关节炎真实世界研究等项目。其核心价值在于:将审批周期从数年压缩至数月,同时强制要求真实世界数据收集,为全国监管政策提供“沙盒实验”样本。
- 广州南沙:率先探索限制类细胞治疗技术临床应用,构建区域临床应用项目审查机制,已落地5项标志性项目。
- 北京昌平:2026年1月在爱尔兰总理见证下,引进爱尔兰奥森干细胞公司,加速糖尿病并发症治疗管线的本土化临床试验。昌平区在研管线达190余条,占全国IND批件的5%。
国际监管的“日本教训”:
日本的条件性限时批准制度允许基于小样本、非对照数据上市,导致Stemirac等产品陷入“批准了却证不明确有效”的尴尬境地。2026年,这一模式的警示意义被全球引为监管过度宽松的反面教材。
四、为什么监管对患者至关重要?(附2026年决策指南)
监管在保护接受干细胞治疗和其他细胞疗法的患者方面发挥着至关重要的作用。以下是监管如何直接惠及患者:
1. 持续的治疗质量
监管确保干细胞的获取、处理、储存和输送流程标准化。2026年案例:美国FDA近期批准了Cabaletta Bio公司的CAR-T自体疗法在全自动封闭平台上生产,这正是通过生产流程的标准化来降低批次差异。
2. 降低感染或排异风险
严格的监管规程要求实验室环境必须无菌,并进行污染检测和患者筛查。2026年案例:广州南沙的干细胞移植治疗中心配备了30间层流病房、150张床位,物理环境本身就是监管合规性的体现。
3. 基于研究的适应症限制
监管框架将间充质干细胞的用途限制在有科学证据支持的适应症范围内。2026年案例:马来西亚一项针对哮喘、COPD患者的雾化吸入外泌体治疗研究显示,三名患者在GMP级生产条件下接受治疗,肺功能指标(FEV1/FVC)显著改善,且未出现任何严重不良事件——这正是研究与临床界限清晰的范例。

4. 长期患者安全监测
受监管的干细胞疗法需要结构化的随访和疗效监测。2026年趋势:无论是海南的真实世界研究,还是日本的Stemirac确证试验,监管机构都在强制要求可追溯的结局数据。患者有权要求治疗机构出示同类适应症的随访数据。
五、结语
到2026年,干细胞疗法的未来已不再是抽象的理论探讨。海南的真实世界数据、南沙的地贫治愈案例、日本的监管受挫、美国的伦理政策逆转——所有这些正在发生的事件共同塑造了干细胞疗法的真实面貌。
对于患者而言,2026年的核心问题是:你所接受的疗法,是否处于“负责任的政策试验田”之中,还是在监管真空地带游走?
通过合理运用干细胞、间充质干细胞和细胞疗法,患者将能够获得创新且可靠的再生治疗。
常见问题(2026年2月更新)
Q1:2026年干细胞疗法是否安全?
答:取决于“在哪里做”以及“是否有真实世界数据支撑”。博鳌乐城、广州南沙等监管试点区因强制要求数据收集和质量控制,安全更有保障;而纯粹以商业推广为目的、拒绝提供既往同类患者随访数据的机构,风险极高。
Q2:间充质干细胞主要用于什么用途?
答:当前最成熟的循证应用集中在膝骨关节炎、类风湿关节炎、肝纤维化、糖尿病并发症、神经系统损伤等领域。其优势在于免疫原性低、伦理争议小。
Q3:所有干细胞疗法都受到监管吗?
答:并非所有疗法都受到同等监管。患者应核实治疗是否遵循国家或国际认可的临床和伦理准则,以及是否在国家药品监管部门(如国家药监局、海南省卫健委、乐城管理局)有备案记录。
Q4:患者可以通过哪些途径找到符合伦理的干细胞来源?
答:有道德的供应商会明确告知细胞来源组织(脐带/胎盘/脂肪等)、制备机构是否通过GMP认证、是否经过无菌及支原体检测,并会主动提供客观的风险说明,而非只展示成功案例。
Q5:法规是否会影响干细胞疗法的获取?
答:监管既可能通过“特许政策”加速合法疗法的可及性(如海南、南沙模式),也可能因伦理政策突变导致某些疗法供应链中断(如NIH胎儿组织禁令)。患者应关注政策动态,避免选择依赖单一争议来源的疗法。
参考资料:
[1]:Hyun I., 2010 – The bioethics of stem cell research and therapy
Explains ethical principles, informed consent, and patient protection in stem cell research and clinical use.https://pmc.ncbi.nlm.nih.gov/articles/PMC2913594/
[2]:Trounson A., McDonald C., 2015 – Stem cell therapies in clinical trials: Progress and challenges.Supports regulatory oversight, clinical safety requirements, and ethical challenges in translating stem cell therapy to practice.https://www.nature.com/articles/nrm.2015.10
[3]:Galipeau J., Sensébé L., 2018 – Mesenchymal stromal cells: Clinical challenges and therapeutic opportunities
Details safety considerations, immune modulation, and regulated clinical use of mesenchymal stem cells.https://www.sciencedirect.com/science/article/pii/S1525001625000930
[4]:Taylor C.J. et al., 2018 – Regulatory issues in stem cell research and therapy
Discusses international regulatory frameworks, quality control, and patient safety monitoring in stem cell therapies.https://pmc.ncbi.nlm.nih.gov/articles/PMC6029272/
[5]:Marks P., Witten C., Califf R., 2017 – Clarifying stem-cell therapy regulation
Explains how regulatory agencies distinguish evidence-based stem cell therapies from unsafe or unproven interventions.https://www.nejm.org/doi/full/10.1056/NEJMp1701469
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信