Meta描述:2026年4月27日,河北医科大学第一医院“脐带间充质干细胞注射液治疗Child B级肝硬化失代偿期随机对照临床研究”获国家干细胞临床研究备案(编号MR-13-26-029229)。本文详解肝硬化分期、传统治疗局限、MSC作用机制及患者参与临床试验的常见问题。
引言:又一国家级干细胞临床研究项目落户河北医大一院
2026年4月27日,由河北医科大学第一医院作为发起、实施单位的 “脐带间充质干细胞注射液治疗Child B级肝硬化失代偿期随机对照临床研究”项目(项目负责人:张玉果),经过院级、省级、国家层层审核,成功获批国家干细胞临床研究备案项目,备案编号为 MR-13-26-029229,并已在国家医学研究登记备案信息系统登记。
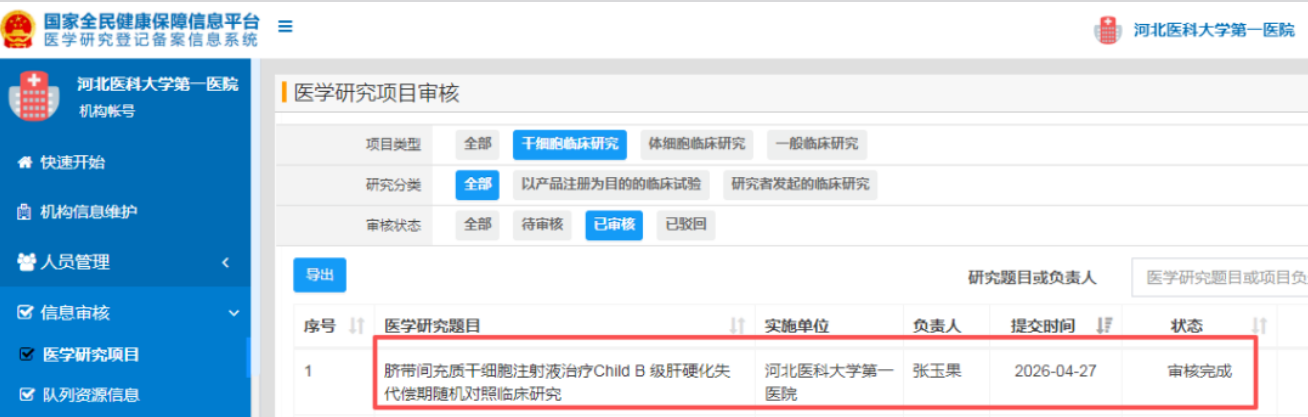
这标志着该院在干细胞治疗失代偿期肝硬化领域的研究正式进入规范化临床研究阶段,为众多肝硬化患者带来了新的治疗希望。
新获批|河北医科大学第一医院干细胞治疗Child B级肝硬化失代偿期临床研究获成功备案
一、什么是肝硬化?代偿期与失代偿期的区别
肝硬化(Liver Cirrhosis, LC)是一种常见的慢性、进行性肝病,病理特征为:
- 肝细胞变性坏死
- 纤维组织弥漫性增生
- 再生结节形成
- 肝脏逐渐变形、变硬
晚期常出现上消化道出血、继发感染、腹水、癌变等严重并发症。
1.1 代偿期肝硬化
- 临床表现:无任何特异性症状或体征,肝功能检查无明显异常
- 组织学:已有明显病理变化
- 肝功能:正常或轻度异常,可有门脉高压
- 无并发症:未发生腹水、出血、肝性脑病等
1.2 失代偿期肝硬化
当肝硬化继续加重,出现以下至少一项并发症时,即进入失代偿期:
- 脾功能亢进
- 消化道出血(食管胃底静脉曲张破裂)
- 肝性脑病
- 腹水
- 黄疸进行性加重
流行病学数据:据统计,我国约有700万肝硬化患者,每年约有4%~12% 的肝硬化患者进展为失代偿期肝硬化。
二、传统治疗的困境:为何需要新疗法?
从肝炎发展到肝硬化,曾长期被认为是不可逆的过程。传统治疗手段包括:
| 治疗方式 | 作用 | 局限性 |
|---|---|---|
| 病因治疗(抗病毒、戒酒等) | 延缓进展 | 无法逆转已形成的纤维化/硬化 |
| 对症支持(利尿剂、降门脉压) | 控制并发症 | 治标不治本 |
| 肝移植 | 根治性手段 | 供体短缺、手术风险、免疫排斥、费用高昂(数十万至百万) |
因此,亟需发展安全、有效、可及的新型治疗产品,以造福失代偿期肝硬化患者。
三、间充质干细胞治疗肝硬化的机制
近年来研究发现,间充质干细胞(MSCs)可能是一种潜在有效的失代偿期肝硬化新疗法。其主要作用机制包括:
| 机制 | 具体作用 |
|---|---|
| 免疫调节 | 分泌多种免疫调节因子,抑制过度炎症反应 |
| 抑制肝星状细胞活化 | 减少肝纤维化水平,延缓甚至逆转纤维化 |
| 旁分泌效应 | 释放生长因子、抗炎因子,减轻肝细胞损伤 |
| 营养支持 | 为肝脏提供营养,改善组织微环境 |
| 促进肝再生 | 可能激活内源性肝干细胞或促进肝细胞增殖 |
与肝移植不同,MSCs治疗无需配型、无免疫排斥、创伤小,且来源于脐带,取材方便、伦理争议少。
四、项目详情:一项严谨的随机对照临床研究
4.1 基本信息
| 项目 | 内容 |
|---|---|
| 项目名称 | 脐带间充质干细胞注射液治疗Child B级肝硬化失代偿期随机对照临床研究 |
| 实施单位 | 河北医科大学第一医院 |
| 项目负责人 | 张玉果 |
| 备案编号 | MR-13-26-029229 |
| 获批日期 | 2026年4月27日 |
| 研究类型 | 随机对照临床研究(RCT) |
| 备案系统 | 国家医学研究登记备案信息系统 |
4.2 研究目标人群
- Child-Pugh分级:B级(中度失代偿期肝硬化)
- 诊断标准:符合肝硬化失代偿期临床诊断标准
- (具体入排标准以研究方案为准,可咨询项目组)
4.3 研究设计亮点
- 随机对照:最大程度减少偏倚,提供高质量循证医学证据
- 脐带来源间充质干细胞:异体使用,无需抽取患者自身骨髓/脂肪
- 严格质控:符合国家《干细胞临床研究管理办法》
4.4 研究进度
项目将严格对标 《生物医学新技术临床研究和临床转化应用管理条例》(国务院第818号令) 及医学伦理要求,目前已获批备案,后续将进入受试者筛选与入组阶段。
五、研究意义与展望
5.1 临床价值
- 为Child B级失代偿期肝硬化患者提供新的治疗选择
- 有望延缓疾病进展、减少并发症、提高生活质量
- 部分患者可能避免或推迟肝移植
5.2 学术与学科意义
- 彰显河北医科大学第一医院在干细胞临床研究、肝病治疗领域的科研实力
- 推动再生医学与临床诊疗的交叉融合
- 为后续开展III期临床试验及产品上市奠定基础
5.3 未来展望
若本研究证实安全有效,未来可能:
- 扩大至Child C级(重度失代偿期) 患者
- 探索重复给药方案(如每3-6个月一次)
- 联合抗病毒、抗纤维化药物实现协同治疗
六、常见问题解答(FAQ)
问1:这个研究获批备案,意味着干细胞治疗肝硬化已经成熟了吗?
答: 不是的。获批国家干细胞临床研究备案,意味着该研究可以在河北医科大学第一医院按照规范开展临床试验,但尚未成为常规临床治疗。所有参与者均需签署知情同意书,并且研究团队不向患者收取治疗相关费用。市面上任何声称“干细胞治疗肝硬化已成熟”并收费的机构,均属违规或虚假宣传。
问2:我/家人是肝硬化患者,能参加这个临床试验吗?如何报名?
答: 本研究入选标准之一为Child-Pugh B级(失代偿期) 肝硬化患者。具体是否适合,需要由研究医生进行面诊和全面评估。建议您:
- 直接联系河北医科大学第一医院肝病科或项目负责人张玉果医生团队
- 或关注医院官网、临床试验注册平台发布的招募信息
⚠️ 所有正规临床试验均不收取患者任何治疗费用。
问3:治疗过程是怎样的?需要住院吗?
答: 通常为静脉输注脐带间充质干细胞,类似普通输液,每次约30-60分钟。根据研究方案,可能需要单次或多次输注,并在治疗后规定时间点(如第1、3、6、12个月)返院复查肝功能、影像学及生活质量评估。具体住院要求请咨询研究团队。
问4:干细胞治疗肝硬化安全吗?有什么副作用?
答: 根据既往国内外同类研究,脐带间充质干细胞具有良好的安全性记录。常见不良反应包括一过性低热、头痛、乏力,多可自行缓解。严重不良事件(感染、过敏、栓塞等)极为罕见。但任何医疗操作均有风险,研究团队会在您参加前详细告知并签署知情同意书。
问5:治疗费用是多少?医保能报销吗?
答: 作为国家备案的临床试验,研究药物(脐带间充质干细胞注射液)及相关方案规定的检查费用均免费。与研究无关的常规治疗(如原有基础病的用药)可能需自理。医保不覆盖,但因免费,患者无需自费治疗。
问6:这个研究和“肝移植”相比有什么优势?
答:
| 维度 | 干细胞治疗 | 肝移植 |
|---|---|---|
| 创伤 | 微创(静脉输注) | 大手术 |
| 供体来源 | 无需配型,脐带来源充足 | 供体短缺,等待期长 |
| 免疫排斥 | 极低(MSCs低免疫原性) | 需终身服用免疫抑制剂 |
| 费用 | 临床试验期免费 | 数十万至上百万元 |
| 根治性 | 可延缓/改善,但不能完全替代肝功能 | 可根治 |
干细胞治疗更适合暂时不适合或无法接受移植的中度失代偿期患者,作为桥接或辅助治疗。
问7:Child B级是什么意思?我该如何判断自己的分级?
答: Child-Pugh分级是评估肝硬化严重程度的常用系统,根据以下5项指标打分(总分为5-15分):
| 指标 | 1分 | 2分 | 3分 |
|---|---|---|---|
| 总胆红素(μmol/L) | <34 | 34-51 | >51 |
| 白蛋白(g/L) | >35 | 28-35 | <28 |
| 凝血酶原时间延长(秒) | <4 | 4-6 | >6 |
| 腹水 | 无 | 轻度 | 中重度 |
| 肝性脑病 | 无 | 1-2级 | 3-4级 |
- A级(5-6分) :代偿期,预后最好
- B级(7-9分) :中度失代偿期,本研究的入组人群
- C级(10-15分) :重度失代偿期,预后最差
您可以通过肝功能、凝血功能、腹部超声及临床评估由医生判定。
问8:这项研究预计什么时候能出结果?什么时候能上市?
答: 临床试验通常需要2-4年完成入组、随访和数据分析。若结果阳性,还需进一步开展III期试验,之后提交国家药监局(NMPA)审批。因此,保守估计5-8年内可能上市。在此期间,患者仍可关注其他临床试验或继续接受标准治疗。
七、给患者及家属的理性建议
- 保持理性期望:干细胞治疗有望改善肝功能、延缓进展,但不能保证治愈,也非100%有效。
- 警惕收费陷阱:任何在临床研究阶段就向患者收费的“干细胞治疗”,均属违法。
- 优先参与正规试验:如果您符合入组条件,可积极咨询河北医科大学第一医院,参与免费临床试验。
- 不要放弃标准治疗:在进行干细胞治疗前,仍需规范使用抗病毒、利尿、降门脉压等基础药物。
参考资料
- 河北医科大学第一医院官方发布(2026年4月27日)
- 国家干细胞临床研究备案信息系统(备案号MR-13-26-029229)
- 《生物医学新技术临床研究和临床转化应用管理条例》(国务院第818号令)
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议。本文内容不能替代医生或药剂师的专业建议。所有治疗决策请咨询正规医疗机构专科医生。关于本临床试验的具体入组标准、排除标准及研究流程,以河北医科大学第一医院发布的正式招募说明及知情同意书为准。




 扫码添加官方微信
扫码添加官方微信