全球首款!两款干细胞疗法获批日本,用于心衰和帕金森病
2026年2月,诱导多能干细胞(iPS细胞)技术迎来了历史性时刻。日本厚生劳动省专家小组正式批准两款iPS细胞来源的再生医学产品有条件上市,分别用于治疗重症心力衰竭和帕金森病。这是全球首次有iPS细胞治疗产品获得监管放行,标志着这项源于日本、曾获诺贝尔奖的技术,历经20年探索,正式从“实验室故事”迈入“临床实用阶段”。

借此马年开工之际,这两款产品的获批不仅为医学界注入强心针,也象征着再生医学领域“一马当先”的突破。
两款划时代产品:修复心脏与大脑
本次获批的两款产品均利用了iPS细胞的分化潜能,通过将健康供体的iPS细胞诱导分化为特定功能细胞,来修复受损的人体组织。
- ReHeart(重症心衰治疗):由大阪大学衍生企业Cuorips开发。该产品将iPS细胞诱导分化为心肌细胞,制成约0.1毫米厚的超薄心肌细胞片。通过手术贴附于受损心脏表面后,细胞片可通过分泌细胞因子促进血管新生与心肌组织修复,专门用于重症缺血性心肌病的治疗。
- Amshepri(帕金森病治疗):由住友制药基于京都大学的研究成果开发。该产品将iPS细胞诱导为多巴胺神经前体细胞,通过立体定向手术精确移植至脑内壳核。移植后的细胞能够分化为功能性多巴胺能神经元,从而补充帕金森病患者大脑中缺失的多巴胺,改善运动功能。
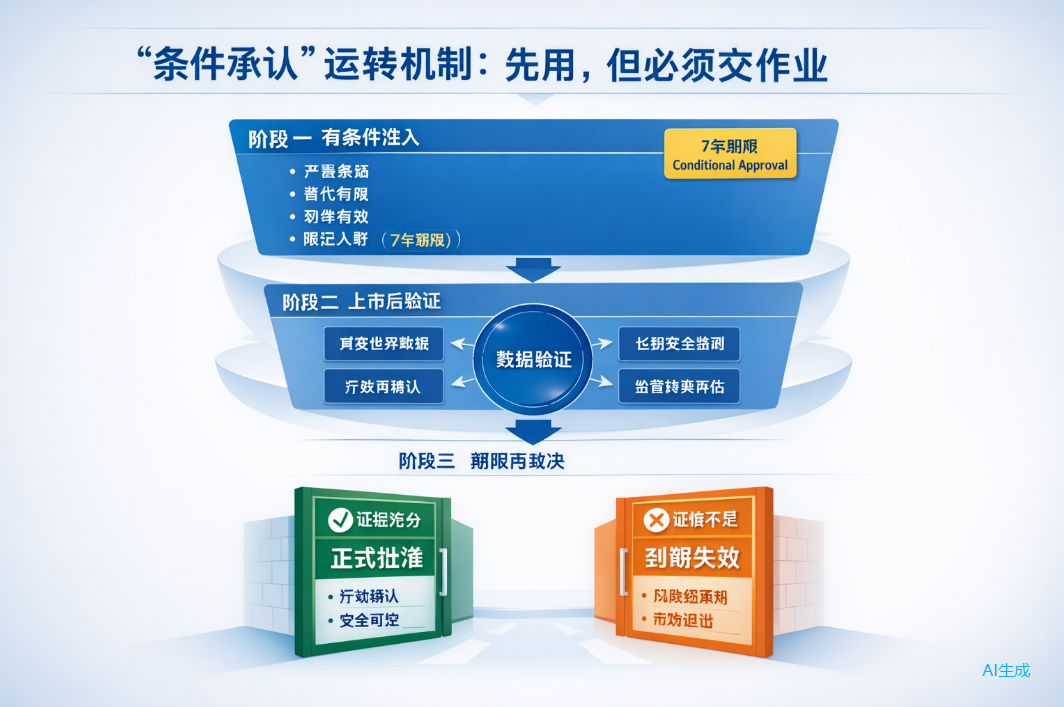
“7年条件承认”:加速背后的严谨逻辑
这两款产品并非传统意义上的“完全批准”,而是通过日本特有的“条件及期限付承认”(有条件限时审批)制度获批。

这一制度的本质是“先让符合条件的患者用上”,同时要求企业在最长7年的“条件承认期”内,完成更大样本的临床验证。监管机构明确表示,这一机制的前提是早期数据已“可预测有效且安全性已确认”。企业必须在期限内提交能支撑转为完全批准的证据,如果有效性无法确认,批准将到期失效。
因此,这一里程碑并非监管“放水”,而是在确保安全底线的前提下,为高风险、高潜力的再生医疗产品开辟了一条“先上市、后补证”的现实通道。历史上,也曾有产品因后续证据不足而在该机制下被撤回,这提醒着行业:加速不是终点,补证才是胜负手。
临床数据:初步验证安全性与有效性
两款产品的获批基于有限的但令人鼓舞的早期临床数据:
ReHeart:在纳入8例重症心衰患者的临床研究中,术后3个月患者心脏功能显著改善,所有患者症状得到缓解,且在观察期内未发现肿瘤形成。
Amshepri:在纳入7例帕金森病患者的临床研究中,6例疗效可评估者中有4例运动功能获得明确改善,部分患者甚至恢复了日常活动能力。PET影像学证实移植细胞可在脑内存活并分泌多巴胺,且无肿瘤形成。该研究结果已发表于国际顶尖期刊《自然》(Nature)。

展望:从科学可行到制度可行
iPS细胞由京都大学山中伸弥教授于2006年首次在实验室中制备成功,2012年即荣获诺贝尔奖。然而,从“能做”到“能批”,这十多年来,科学家们一直在攻克规模化制造、批间一致性以及长期安全性随访等难题。
日本此次通过“条件承认”制度为iPS疗法打开了监管之门,被国际媒体称为“全球iPS疗法走向社会化应用的关键拐点”。接下来,业界关注的重点将聚焦于三件事:
- 正式批复的细节:最终适用的具体适应症、患者人群界限以及严格的医疗机构要求。
- 上市后评估方案:如何设定合理的终点指标和评估频率,以在7年内完成证据链的闭环。
- 全球监管的连锁反应:日本先行一步后,这款产品将成为各国监管机构讨论iPS细胞疗法审批路径的现实参照物,推动该领域从“科学可行”全面进入“制度可行”的新阶段。
参考资料:
1.iPS Cell Products Win World-First Approval in Japan: Heart Failure and Parkinson’s Treatments Mark 20-Year Milestone
2.Big step toward world’s first practical use of iPS cells
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信