全球范围内急性和慢性肝病负担沉重,亟需安全有效的再生疗法来补充或延缓肝移植。间充质干细胞(MSCs)已被公认为用途广泛的生物制剂,主要通过旁分泌信号传导调节炎症、逆转纤维化并促进肝脏修复。
全球肝病的沉重负担与主要类型:肝脏疾病是全球重要的公共卫生挑战,约占全球死亡总数的4%,每年导致约150万人死亡。慢性肝病是发病和死亡的主要原因,2021年全球肝硬化病例估计达5840万例。肝病相关死亡的主要诱因包括慢性乙型及丙型肝炎病毒感染所致的肝硬化、酒精相关性肝病、代谢功能障碍相关脂肪性肝病(MASLD)以及肝细胞癌,而急性肝损伤(ALI)所占比例相对较小。

肝脏再生潜力与传统治疗局限:肝脏虽具有显著的再生能力,但慢性损伤会破坏这一过程,导致持续炎症、纤维化和血管异常,最终形成阻碍再生的病理性微环境。对于终末期肝病,原位肝移植是当前唯一的根治性手段,但其应用受到供体严重短缺、高昂费用、需终身免疫抑制治疗及相关并发症(如感染、代谢性疾病和移植物排斥)的严重限制,影响了患者的长期生存与生活质量。
干细胞再生疗法的前景与挑战:基于上述局限,调节肝脏微环境的再生疗法成为备受关注的策略,其中间充质干细胞(MSCs)及其衍生物因具有多机制促再生潜力而展现出广阔前景。虽然MSCs疗法为急性肝损伤、肝硬化等疾病提供了生物学依据,但其来源、培养与给药策略的差异要求建立标准化方案和临床效价检测方法,以确保治疗可靠性。
间充质基质/干细胞疗法在肝脏再生中的应用:现状与未来方向
在此背景下,近期,国际医学科学杂志刊发了一篇“间充质基质/干细胞疗法在肝脏再生中的应用:现状与未来方向”的研究综述[1]。

该研究对MSCs的生物学特性、肝脏再生以及基于细胞的疗法与基于EVs的疗法,包括给药途径、剂量、质量和安全性进行了逐一综述。此外,该研究表明未来的研究方向将侧重于生物标志物、多中心临床试验以及用于可扩展的个性化肝脏再生的工程化MSC/EV平台。
间充质干细胞的生物学和来源依赖性特性
基本生物学特性与定义:根据国际细胞治疗协会的定义,间充质干细胞的基本生物学特性包括:在塑料表面贴壁生长;表达特定表面标志物(CD73、CD90、CD105阳性,而造血标志物阴性);具备体外成骨、成脂和成软骨的三系分化潜能。术语上,“间充质基质细胞”更贴近这一定义,而“间充质干细胞”通常需体内自我更新和多能性的证据,但研究中两者常混用。
主要组织来源及其特性:MSCs最初从骨髓中分离,现已广泛发现于脂肪、脐带、胎盘等成人与围产期组织中。其特性受来源、供体年龄和培养条件影响,导致显著的异质性,这也是治疗标准化面临的主要挑战。
- 骨髓来源MSCs(BM-MSCs):具有较强的成骨和免疫调节能力,但获取过程有创,且细胞数量有限。
- 脂肪来源MSCs(AD-MSCs):易于从吸脂物中大量获取,分泌组富含生长因子和EVs,能有效促进血管生成、细胞增殖与迁移,适合规模化生产。
- 围产期来源MSCs(如脐带、胎盘):具有低免疫原性、高增殖潜能以及显著的抗纤维化和抗炎特性,例如通过分泌基质金属蛋白酶(MMPs)抑制纤维化并调节免疫反应,在再生医学中展现出独特优势。
iPSC衍生MSCs及挑战:除天然组织来源外,MSCs也可由诱导多能干细胞(iPSC)定向分化获得。iPSC衍生的MSCs表面标志物与天然MSCs相似,且能长期扩增,但可能存在基因组异常和潜在的致瘤风险,需要严格的质量控制。
总体而言,MSCs的来源依赖性体现在其增殖能力、分泌组组成、免疫调节活性和分化倾向上,这些差异决定了其在肝脏疾病等具体应用中的适用性。表1总结了与肝脏应用相关的间充质干细胞的来源依赖性特性。
| 特征 | 骨髓间充质干细胞 | AD-MSCs | 围产期间充质干细胞 | iMSCs |
|---|---|---|---|---|
| 组织 来源 | 骨髓 | 脂肪组织 | 华通氏胶、脐带血、胎盘 | iPSC衍生 |
| 扩散能力 | 低( 占有核细胞的 0.001%–0.01%) | 高的 | 非常高 | 无限 |
| 提取方法 | 侵入性抽吸 技术 | 微创吸脂 术 | 无创采集围产期组织 | 复杂的制造 过程 |
| 免疫学特性 | 强 免疫调节 作用 | 免疫调节剂 | 免疫原性低,具有显著的抗炎和抗纤维化作用 | 与天然间充质干细胞类似 |
| 功能特性 | 具有强大的 成骨潜能、免疫调节作用,并已开展广泛的临床 研究 | 高效增殖、 强效促再生 分泌组、高细胞产量,适合规模化生产 | 保留原始表型;干细胞特性标记物(如 OCT4 和 SOX2)表达升高; 可直接用于异体移植。 | 表面标志物和 功能特征与天然间充质干细胞相似; 基因组不稳定、 具有致瘤风险、 生产工艺复杂 |
间充质干细胞助力肝脏再生中的作用机制是什么?
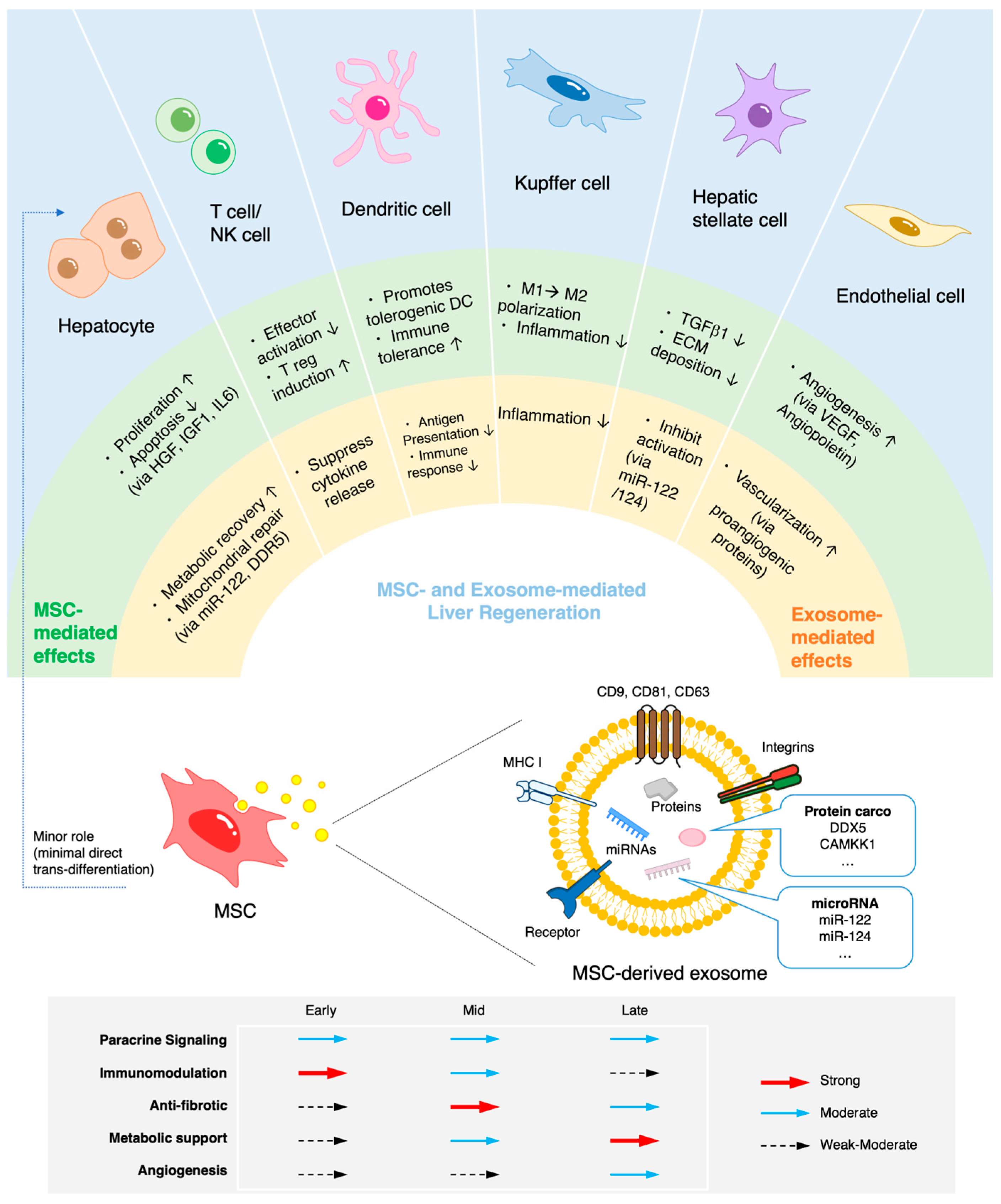
间充质干细胞(MSCs)通过多方面的旁分泌、免疫调节、抗纤维化、代谢和血管生成机制支持肝脏修复。MSCs协调肝脏微环境中的多种再生通路,并通过这些机制促进组织修复(图1,表2)。
- 营养支持与直接促增殖:分泌肝细胞生长因子(HGF)、胰岛素样生长因子-1(IGF-1)等,直接促进肝细胞增殖与存活。
- 免疫调节:释放细胞因子,抑制促炎性T细胞和M1型巨噬细胞,同时激活调节性T细胞(Tregs)和抗炎的M2型巨噬细胞,从而减轻局部炎症。
- 抗纤维化:通过下调转化生长因子-β1(TGF-β1)等因子,抑制肝星状细胞活化,减少细胞外基质过度沉积。
- 促进血管生成:分泌血管内皮生长因子(VEGF)等,改善损伤区域的血液循环。
- 细胞外囊泡(EVs)介导的调控:MSCs释放的EVs可递送功能性RNA、蛋白质,甚至进行线粒体转移,直接恢复受损肝细胞的代谢功能。
| 机制 | 关键因素 | 主要功能 | 参考 |
|---|---|---|---|
| 旁分泌/营养 | HGF、VEGF、IGF-1、IL-6 | 促进肝细胞增殖,抑制细胞凋亡,增强组织灌注 | [ 56 , 57 , 58 ] |
| 免疫学 | CD8 + T细胞、NK细胞和B细胞数量减少;M2巨噬细胞极化;前列腺素诱导调节性树突状细胞 | 抑制免疫反应,促进抗炎环境,增强组织修复 | [ 47 , 48 , 49 , 59 ] |
| 抗纤维化 | miR-378c(外泌体),TGF-β1抑制 | 抑制肝星状细胞活化和纤维化 | [ 50 , 51 ] |
| 代谢 | 通过隧道纳米管进行线粒体转移 | 恢复肝脏氧化能力和脂质代谢 | [ 54 ] |
| 血管生成 | 血管紧张素-1、血管紧张素-2、血管内皮生长因子 | 增强肝脏再生过程中的血管生成和氧气输送 | [ 53 ] |
| 细胞外囊泡介导/旁分泌 | MicroRNA(miR-19b、miR-122、miR-124、miR-182-5p、miR-148a)、蛋白质(DDX5、CAMKK1) | 调节受体细胞行为,无需细胞移植即可恢复肝功能 | [ 51 , 52 , 55 , 60 , 61 , 62 , 63 ] |
这些机制相互重叠、协同作用,形成一个动态网络。其主导地位随肝损伤与修复阶段而变化:损伤早期以快速免疫调节为主,为修复创造稳定环境;组织重塑阶段抗纤维化作用凸显;长期来看,代谢支持和促血管生成效应则持续促进功能与结构的恢复。
基于细胞与无细胞的治疗肝脏疾病的策略是什么?
基于细胞与无细胞的治疗肝脏疾病策略,核心区别在于是否使用活的间充质干细胞(MSC)本身。基于细胞的策略指直接输注活体MSCs。这些细胞被视为“智能药物工厂”,能够在体内存活、归巢至损伤部位,并根据局部微环境动态调整其旁分泌(如生长因子、细胞外囊泡)和免疫调节功能,实现个体化的、自适应的治疗响应。然而,该策略面临活细胞固有的挑战,包括静脉输注后的肺部滞留、随培养扩增而下降的归巢能力和潜在的遗传不稳定性风险。
无细胞的策略则主要利用MSCs分泌的细胞外囊泡(EVs)。EVs是富含蛋白质、RNA等生物活性物质的纳米级囊泡,可视为MSC治疗效应的“标准化包裹”。它们能再现MSCs的抗炎、抗纤维化和促再生作用,同时规避了活细胞移植的肿瘤风险和免疫排斥问题,且更易于储存、灭菌和剂量标准化。但EVs的功能是固定的,无法像活细胞那样动态适应体内变化,其大规模生产与质控也面临技术挑战。
因此,当前形成了一种互补范式:在需要复杂、动态免疫调节(如严重炎症或自身免疫相关肝病)时,优先使用活的MSCs;而当治疗目标明确为标准的抗炎和抗纤维化时,则可选用更安全、易控的EVs制剂。治疗时还需综合考虑细胞/囊泡来源、递送途径和疾病阶段等因素以优化疗效。
间充质干细胞治疗肝病的给药途径和剂量对治疗效果的影响
给药途径是影响间充质干细胞治疗肝脏疾病效果和安全性的关键因素。常见的途径包括外周静脉输注、门静脉/肝动脉注射以及局部肝内注射。
静脉注射是最简单、创伤最小的方法,因此方便且通常是首选。但大量细胞会滞留于肺部,导致肝脏靶向性降低。
相比之下,经门静脉或肝动脉的直接肝脏给药能显著提高细胞在肝内的局部浓度和滞留率,但属于侵入性操作,对伴有门脉高压和凝血功能障碍的肝硬化患者存在较高出血和血栓风险。局部影像引导下的注射能精准作用于特定病灶,但不适用于弥漫性肝损伤,MSC和EV在治疗肝病中的递送途径总结于图2中。
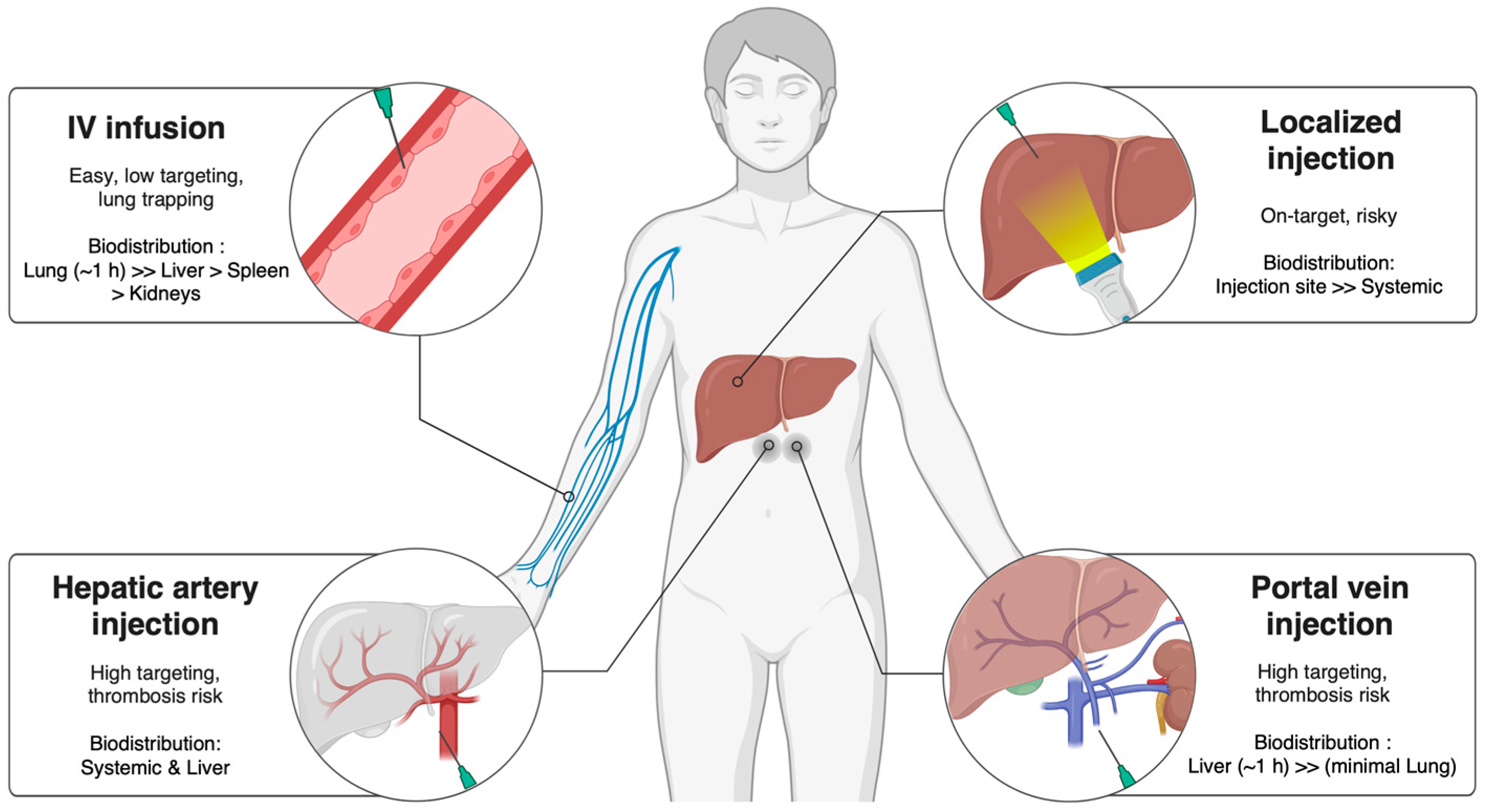
治疗剂量和方案需根据疾病类型和阶段进行个体化调整。在急性肝损伤的临床前模型中,常用有效剂量为1–5×10⁶个细胞/公斤体重,其中中等剂量效果最佳,更高剂量未必增效。对于慢性肝损伤或肝纤维化,典型剂量范围为0.5–3×10⁶个细胞/公斤体重,且研究显示重复给药通常比单次给药效果更优,表明存在累积治疗效应。
若使用MSC来源的细胞外囊泡,常用剂量范围为10⁹–10¹²个颗粒/公斤或50–600微克蛋白质,中等剂量往往能产生最佳治疗反应,表3详细总结了适应症特异性剂量范围和剂量-反应趋势。这些发现强调了仔细滴定和药效学监测的必要性,以优化治疗效果。
| 肝损伤模型 | 治疗 | 剂量范围 | 行政路线 | 剂量反应 | 参考 |
|---|---|---|---|---|---|
| ALI(小鼠/大鼠) | 间充质干细胞 | 1–5 × 10⁶个细胞/千克 | 第四 | 1–2 × 10⁶ :效果差; 2–4 × 10⁶ :效果最佳/中等;>4 × 10⁶ :效果停滞或略有下降 | [ 97 , 101 ] |
| CLI/纤维化(小鼠/大鼠) | 间充质干细胞 | 0.5–3 × 10⁶ 个细胞/千克(或 1–20 × 10⁷个总细胞) | IV,IP | 0.5–1 × 10⁶ :效果不佳; 1–3 × 10⁶ :效果中等; >3 × 10⁶ :无进一步改善 | [ 101 , 105 ] |
| 失代偿期 肝硬化(人类,早期临床) | 间充质干细胞 | 5 × 10⁷ – 2 × 10⁸个细胞/输注 | 第四 | 5–10 × 10⁷ :效果不佳; 1–2 × 10⁸ :中等/最佳; 更高剂量:未观察到额外益处 | [ 104 ] |
| 肝损伤(小鼠/大鼠) | MSC-EVs | 10⁹ – 10¹²个颗粒/千克或 50–600 微克蛋白质 | 第四 | 10⁹ – 3 × 10¹⁰ 个颗粒(或 50–150 µg):低效应; 3 × 10¹⁰ –1 × 10¹¹个颗粒(150–300 µg):中等效应; >1 × 10¹¹ 个颗粒(300–600 µg):平台期 | [ 102 , 106 ] |
| 缺血性肝病/ 中风模型 | MSC-EVs | 30–250 µg 蛋白质 | 第四 | 30–100 微克:效果较差;100–250 微克:效果中等/最佳;重复给药可能进一步增强效果 | [ 103 , 106 ] |
综上所述,给药途径和剂量的选择需要综合权衡。途径选择需考虑靶向性、操作风险及疾病分布特点(局灶性或弥漫性),而剂量确定则需依据损伤的急慢性性质,并通过仔细的剂量滴定和药效学监测来优化。理想的治疗策略应是在确保安全的前提下,通过最合适的途径和剂量,使治疗成分最大化地作用于肝脏靶点。
间充质干细胞治疗肝脏疾病基于生物材料增强治疗效果的方式
生物材料作为先进的递送载体,能显著改善间充质干细胞(MSCs)及其细胞外囊泡(EVs)在肝脏疾病治疗中的局限。通过水凝胶或可注射支架包裹MSCs/EVs进行局部给药,可以将治疗成分有效锚定在肝脏靶点,避免静脉输注后的肺部首过滞留和全身性清除,从而大幅提高局部浓度和滞留时间。
这些材料模拟细胞外基质,为MSCs提供了一个支持存活、增强旁分泌功能的三维微环境,并能缓释EVs等活性物质,延长治疗窗口。这从根本上优化了传统给药途径的靶向性和效率,图3总结了生物材料辅助策略在增强间充质干细胞和细胞外囊泡治疗肝病中的疗效方面的应用。

生物材料的应用更进一步,通过功能化设计实现了治疗效果的精准增强。
- 一方面,利用温敏水凝胶等实现微创注射和原位成型,便于临床操作。
- 另一方面,通过对载体进行表面修饰(如连接靶向肝细胞的半乳糖配体)或对MSCs/EVs本身进行工程化改造(如聚乙二醇化),可主动引导它们向肝脏或特定细胞(如肝细胞)归巢,减少脱靶效应。
这些策略综合提升了抗炎、抗纤维化和再生信号的传递效率,临床前研究已证实其能协同增强MSC的治疗效果,为实现更安全、强效和持久的肝脏修复提供了关键技术支撑。
间充质干细胞治疗肝脏疾病的临床概况:安全性和有效性
使用间充质干细胞治疗肝脏疾病的早期临床试验
多项早期临床试验研究了自体或异体间充质干细胞(MSC)疗法在肝硬化、急性加重型慢性肝衰竭(ACLF)及其他肝功能失代偿患者中的安全性和初步疗效。在这些研究中,MSC输注显示出良好的安全性,未报告重大输注相关不良事件或致瘤并发症。
初步疗效指标包括肝功能参数的改善,例如血清白蛋白和胆红素、凝血酶原时间以及终末期肝病模型(MELD)评分和Child-Pugh评分。
表4总结了MSC治疗肝病的早期临床研究,包括疾病适应症、MSC来源、给药途径、样本量、随访时间、主要结局指标和不良事件。
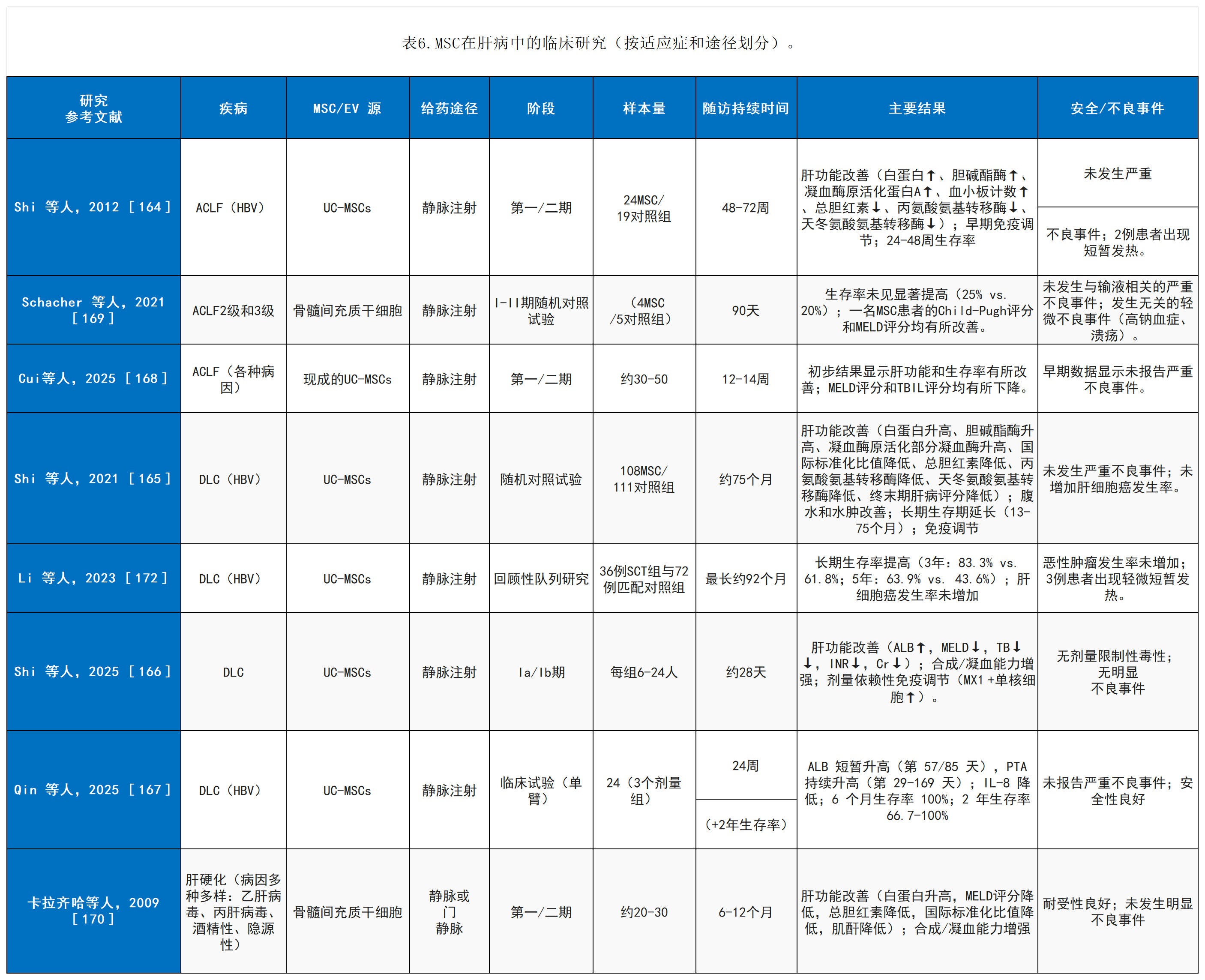
在这些早期短期试验中,临床获益通常仅在特定患者亚组中观察到,例如病情较轻(MELD或Child-Pugh评分较低)、肝合成功能良好(基线白蛋白或凝血酶原活性较高)、乙型肝炎病毒相关病因或基线全身炎症水平较低的患者。由于这些研究通常缺乏长期随访,因此疗效在6-12个月后的持久性仍不确定。这些短期研究中疗效持续时间明显有限或不一致,可能反映了肝损伤进展、持续的炎症环境和/或输注的间充质干细胞在不利的肝脏环境中植入或存活率有限。
重要的是,多项长期随访研究报告了持续获益,包括数年内生存率和肝功能的改善。较高剂量的间充质干细胞(MSC)(2×10⁸个细胞)和重复给药(每周一次,持续3周)可改善肝功能,这体现在Child-Pugh评分和MELD评分的降低,以及MX1⁺单核细胞比例的降低。这些观察结果表明,剂量、重复给药和患者特征可能影响疗效。需要更大规模的对照试验来证实这些临床发现。
在各种间充质干细胞(MSC)来源中,脐带间充质干细胞(UC-MSC)显示出最稳定的疗效。短期至长期随访结果显示,血清白蛋白升高5-15g/L,凝血酶原活性提高10-20%,总胆红素降低20-35%。MELD评分降低2-5分,Child-Pugh评分提高1-3分,长期生存获益可达75-92个月。
最常见的不良反应是轻度短暂发热,并观察到剂量依赖性的免疫调节作用,包括MX1+单核细胞和IL-8的减少。BM-MSCs也改善了肝功能,白蛋白升高约5–10g/L,MELD评分降低约1–3分,总胆红素降低约15–25%。然而,生存获益并不稳定,尤其是在随访时间较短的小型随机对照试验中。静脉和门静脉给药均耐受性良好,未报告严重不良事件。
总体而言,UC-MSCs似乎比BM-MSCs提供更持久的功能和生存获益,而AD-MSCs的临床数据非常有限,iMSCs仅进行了临床前研究。
间充质干细胞治疗肝脏疾病安全性怎么样?以及缓解风险的方法有哪些?
间充质干细胞(MSCs)治疗肝脏疾病虽显示出良好的总体安全性,但仍存在若干需谨慎管理的特定风险。
- 输注相关反应:如短暂发热、寒战。
- 血栓栓塞风险:尤其对肝硬化患者,可能与高细胞剂量或MSCs表达组织因子有关。
- 遗传不稳定与致瘤潜能:与长期体外扩增相关。
- 免疫致敏风险:异体MSCs重复给药可能诱发免疫反应。
风险缓解策略包括:控制细胞剂量与输注速度、采用抗凝方案、对细胞产品进行严格的基因组稳定性评估、排除活动性恶性肿瘤患者。此外,采用无细胞的EVs策略可提供更高的理论安全边际。优化递送方式(如局部注射)和加强患者筛选与治疗后监测,也是平衡获益与风险的关键。
表5总结了基于MSCs的疗法在肝硬化和急性加重型慢性肝衰竭中报告的不良事件,包括常见和严重不良事件的发生率和严重程度。
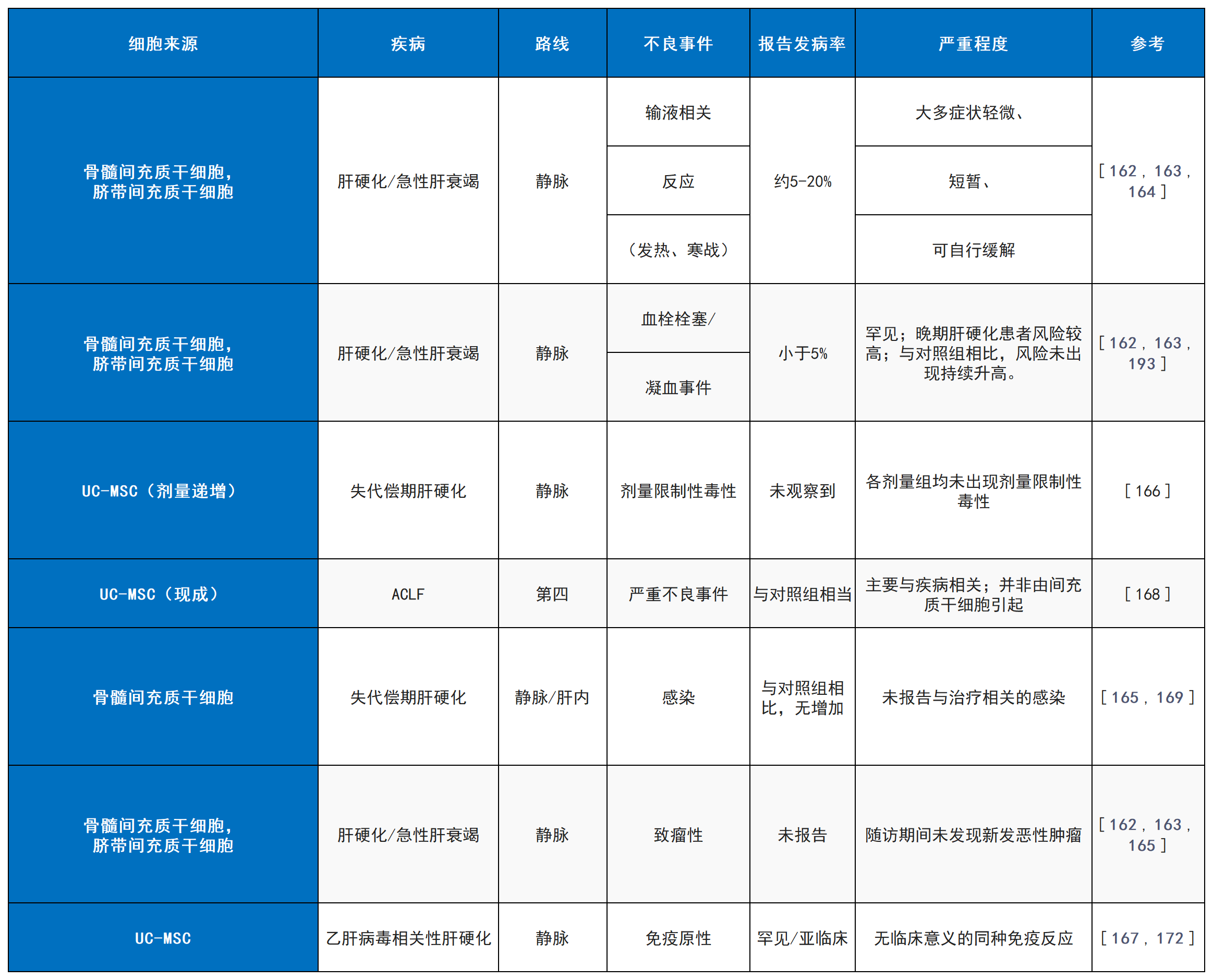
结论与未来方向
间充质干细胞及其细胞外囊泡在再生肝病学领域展现出巨大潜力,有望恢复肝功能并减少对肝移植的需求。尽管临床前与早期临床研究结果鼓舞人心,但在治疗方案标准化、效力验证和监管路径方面仍面临挑战。生物材料、EVs工程和精准医学的进步,为开发可扩展、安全有效的疗法提供了新途径。
未来研究应聚焦于:优化符合药品生产质量管理规范(GMP)的生产工艺;建立并验证可靠的效力检测方法;开展设计严谨的多中心临床试验;以及整合个体化医疗策略。建议的发展时间表包括:短期(1-2年)内完善GMP生产与临床前验证;中期(3-5年)推进关键性多中心临床试验;长期(5-10年)实现更广泛的临床转化与应用。
参考资料:
[1]:Choi, S.; Jeong, J. Mesenchymal Stromal/Stem Cell-Based Therapies for Liver Regeneration: Current Status and Future Directions. Int. J. Mol. Sci. 2026, 27, 619. https://doi.org/10.3390/ijms27020619
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信