脑瘫(Cerebral Palsy, CP)是由围产期脑损伤引起的运动功能障碍综合征,传统康复治疗虽能部分改善症状,但存在疗效局限性和功能倒退风险。近年来,干细胞疗法作为一种再生医学手段,通过修复神经损伤、调节微环境等机制,为脑瘫患者提供了新的治疗方向。然而,不同严重程度的脑瘫患者是否都适合干细胞治疗吗?
本文结合多项临床研究进展,系统分析不同严重程度脑瘫患者的干细胞治疗适用性及优化策略,为临床决策提供循证依据。

干细胞治疗脑瘫:不同严重程度患者的适用性如何?
一、干细胞治疗脑瘫的机制与类型
作用机制
- 替代作用:干细胞可分化为神经元或胶质细胞,重建受损神经网络(如神经干细胞定向修复结构性损伤)。
- 营养支持:通过旁分泌细胞因子(如BDNF、VEGF)促进神经存活、血管生成及髓鞘形成。
- 抗炎与免疫调节:间充质干细胞(MSCs)可抑制炎症反应,减轻继发性脑损伤。
常用干细胞类型
- 间充质干细胞(MSCs) :来源广泛(脐带、骨髓),安全性高,适用于改善粗大运动功能。
- 神经干细胞(NSCs) :直接分化为功能性神经元,重建受损的神经环路,与MSCs相比,NSCs更侧重于结构修复。
- 脐带血干细胞(UCBs) :含多种祖细胞,临床试验显示对运动功能改善显著。
相关阅读:脑瘫治疗选间充质还是神经干细胞?机制、疗效和安全性的全面对比
二、不同严重程度患者的适用性分析
2.1 轻度脑瘫患者:(GMFCS I级)
2011年,解放军第四六三医院神经外科应用脐带间充质干细胞治疗脑瘫患者229例,选择其中无智力障碍、一直进行康复治疗,近一年无明显进展的51例轻度脑瘫患者,进行日常生活活动能力(ADL)评估。比较治疗前与治疗1个疗程(21~28d进行4次脐带间充质干细胞治疗)后ADL得分,评估疗效。

临床结果表明,患者日常生活活动能力得到显著改善,具体来说床上运动、认知交流动作、步行动作的得分及总得分均显著提高,提示干细胞治疗在改善基础运动功能和认知相关动作方面效果显著。(见表1)
但个人卫生、进食、更衣、排便动作的得分差异无统计学意义,表明这些精细动作的改善可能受限于当前治疗手段或评估周期。

综上所述,本研究结果表明,脐带间充质干细胞治疗显著改善了无智力障碍轻度脑瘫患儿的基础运动功能(如床上运动、认知交流及步行动作),但对个人卫生、进食等精细动作的改善效果有限。
2.2 中度脑瘫(GMFCS II-III级)
2017年,中国人民武警总医院在国际期刊《转化医学杂志》上发表了一篇关于《骨髓间充质干细胞与骨髓单个核细胞移植治疗痉挛型脑瘫疗效对比分析》的临床研究成果。本研究纳入了105例脑性瘫痪 (CP) 患者,粗大运动功能分类系统(GMFCS)评分大部分在Ⅱ~Ⅲ级。

粗大运动:骨髓间充质干细胞(BMMSC)治疗痉挛型脑瘫患儿的粗大运动功能改善显著优于其他疗法:3个月即见效(关键动作能力提升),12个月所有指标均改善;而骨髓单个核细胞(BMMNC)疗效较慢且有限,传统康复仅在1年后部分有效,表明BMMSC是更优的早期干预手段。(见图2)
精细运动功能:BMMSC组在精细运动功能(FMFM)的改善上显著优于其他组:3个月时多数维度(A-D)及总分提升,6-12个月所有维度均持续改善;BMMNC组仅在后期(6-12个月)实现全面改善,而对照组仅在12个月时部分改善。组间比较显示,BMMSC组早期(3个月)即在关键维度(如手部控制)领先,长期(6-12个月)全面占优,BMMNC组与对照组疗效无显著差异。(见图3)
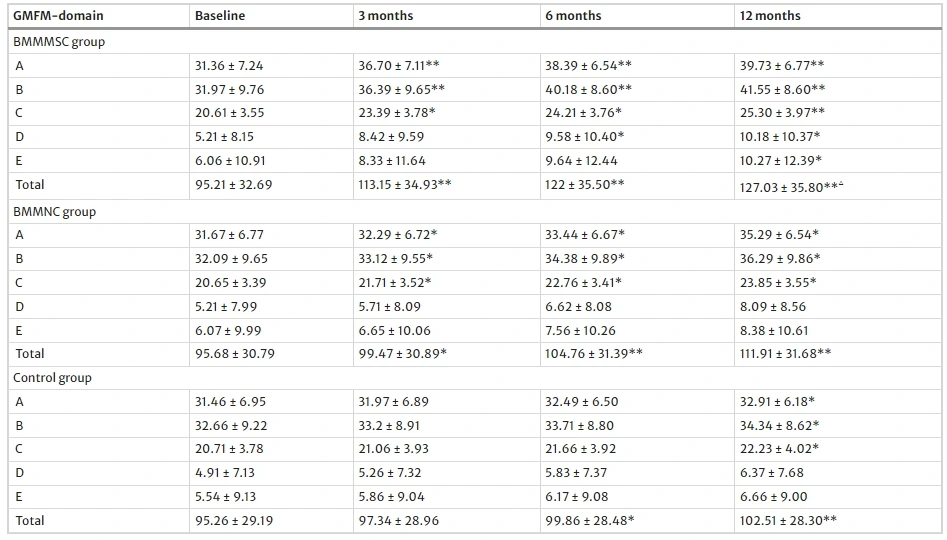
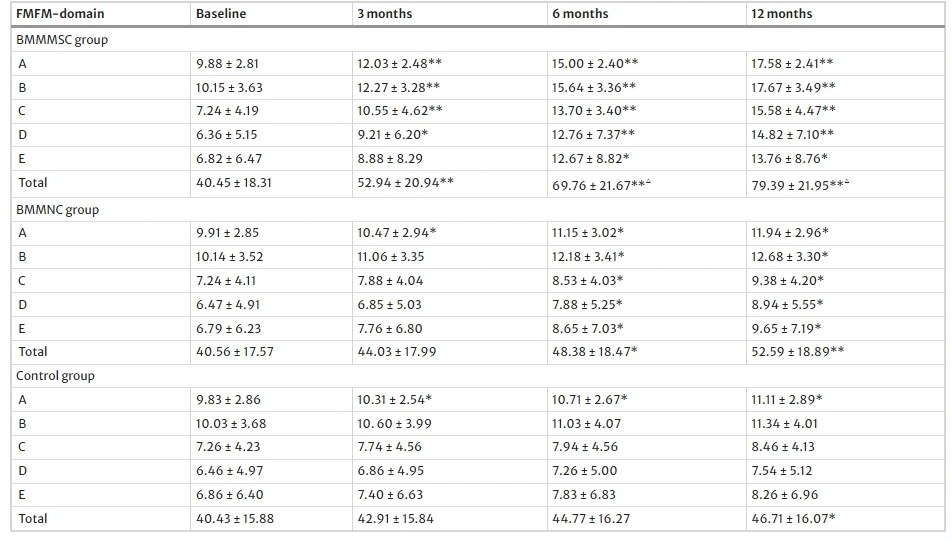
综上所述,研究显示,间充质干细胞治疗痉挛型中度脑瘫患儿的运动功能(粗大及精细)改善显著优于其他疗法:早期(3个月)即在关键维度(如姿势、移动能力)见效,12个月时所有指标均稳定提升;而骨髓单个核细胞(BMMNC)疗效滞后且有限,传统康复仅在1年后部分有效。因此,BMMSC是更优的早期干预手段,可显著改善患儿运动功能,而传统康复需结合细胞治疗以提升短期疗效。
2.3 重度脑瘫(GMFCS IV-V级)
2024年,波兰医科大学在行业期刊《干细胞评论和报告》上发表了一篇关于《脐带间充质干细胞对脑瘫儿童运动功能的影响:真实世界、同情使用研究的结果》的临床研究成果。该研究纳入了152例脑瘫(CP)患儿,患者主要为脑瘫运动功能分级系统(GMFCS)V级(最严重级别),部分为IV级,整体病情处于重度至极重度范围。

研究结果表明:
1.粗大运动功能测量(GMFM):所有患儿(n=152)的GMFM中位评分在基线至第5次随访(第四次干细胞注射后)显著提升1.9分,且改善与年龄呈负相关。并且所有GMFM子领域(如姿势控制、移动能力等)均观察到统计学显著改善。
2.功能性活动测试:
- 6分钟步行测试(6MWT):26名符合测试条件的轻中度患儿(GMFCS I-II级)中,步行距离中位数增加75米,改善与GMFM变化相关。
- 计时起立行走测试(TUG):26名患儿中位完成时间缩短2秒,改善与年龄相关,但与癫痫或性别无关。
3.临床总体印象(CGI)评估:
- 治疗后,39.7%患儿获得轻微改善到III级,35.8%无变化,18.5%改善至II级,5.3%显著改善至I级,仅0.7%患儿病情恶化。
- 改善程度与基线GMFCS分级显著相关,且GMFM评分变化与CGI结果呈负相关。
4.肌肉力量(洛维特测试):63名患儿中,臀大肌力量改善最显著(5.2%患儿提升1级),股四头肌和肱二头肌力量改善有限(仅少数患儿提升1-2级),但肌肉群间力量改善呈中等相关性。
综上所述,hUC-MSCs治疗显著改善了脑瘫患儿的运动功能(尤其在GMFM评分和功能性活动能力),且对重度患者(GMFCS V级)具有潜在疗效。然而,个体反应差异显著,年龄和基线功能水平是关键影响因素。尽管肌肉力量改善有限,但综合结果提示干细胞疗法为重度脑瘫患儿提供了一种安全有效的干预选择。
三、不同严重程度患者的适用性总结
综上所述,针对不同严重程度脑瘫患者的干细胞治疗研究显示:轻度脑瘫患者(GMFCS I级)接受干细胞治疗后,基础运动功能(如床上活动、认知交流及步态)显著改善;中度患者(GMFCS II-III级)干细胞治疗后,其粗大和精细运动功能(如姿势控制、手部操作)在3个月内即显著提升,且疗效持续至12个月,优于别的治疗方法和传统康复;重度患者(GMFCS IV-V级)通过干细胞治疗后,GMFM评分和功能性活动(如步行距离、肌肉力量)虽有一定改善,但个体差异显著,疗效与年龄和基线功能密切相关,且对肌肉力量的修复有限。
总体而言,干细胞治疗对轻度和中度患者运动功能改善明确;重度患者虽获部分获益,但疗效受限,需结合年龄、病情及个体化策略优化方案以提升效果。
四、影响适用性的核心因素
1. 神经可塑性差异
- 年龄窗口:2-6岁儿童神经再生潜力最强,即使重度损伤也可尝试早期干预89。
- 损伤时间:急性期(发病6个月内)干预效果优于慢性期,但慢性重度患者仍可通过调节微环境获得部分改善
2. 干细胞技术选择
- 神经干细胞(NSC):更适合婴幼儿及低龄儿童,因其可直接分化为神经元,重建神经网络。例如,国内研究显示NSC移植后1个月内即可显著改善重症患儿的运动功能。
- 间充质干细胞(MSC):对>6岁患者更具实用性,虽分化能力较弱,但可通过分泌神经营养因子改善微环境,且安全性较高。
相关阅读:脑瘫治疗选间充质还是神经干细胞?机制、疗效和安全性的全面对比
3.其他关键因素
损伤类型与部位:不同类型脑瘫对不同干细胞疗法的响应不同,如;共济失调型更适合神经干细胞移植,神经干细胞能够直接参与神经环路重建。
治疗时机与持续性:
- 早期干预(<3岁)结合多次治疗(如波兰研究中四次干细胞注射)可最大化疗效,尤其是对重度患者的功能维持。
- 长期随访显示,单次治疗后6个月疗效可能衰减。
康复训练协同作用:干细胞治疗需与物理治疗、语言训练等同步进行。例如,英国研究中MSCs联合针灸使肌肉功能改善持续更久,而单纯细胞治疗对精细动作(如手部控制)的提升有限。
结语
干细胞治疗为脑瘫患者提供了突破传统疗法局限的希望,但其适用性需基于病情严重程度、年龄、损伤类型及技术选择进行精准评估。轻度至中度患者通过个体化方案可显著改善运动功能,而重度患者虽疗效受限,仍可通过优化干预策略获得部分功能恢复。未来,随着干细胞技术的创新及多学科联合疗法的推进,将逐步缩小不同严重程度患者的疗效差距,为更多脑瘫患者带来更优的治疗选择。
相关阅读:从婴幼儿到成人:干细胞疗法适用于哪些年龄段的脑瘫患者?
参考资料:
王金刚,尹忠民,闻华,等.脐带间充质干细胞治疗脑瘫51例疗效观察[J].中国全科医学,2011,14(21):2446-2447.
Liu, X., Fu, X., Dai, G. et al. Comparative analysis of curative effect of bone marrow mesenchymal stem cell and bone marrow mononuclear cell transplantation for spastic cerebral palsy. J Transl Med 15, 48 (2017). https://doi.org/10.1186/s12967-017-1149-0
Chrościńska-Kawczyk, M., Zdolińska-Malinowska, I. & Boruczkowski, D. The Impact of Umbilical Cord Mesenchymal Stem Cells on Motor Function in Children with Cerebral Palsy: Results of a Real-world, Compassionate use Study. Stem Cell Rev and Rep 20, 1636–1649 (2024). https://doi.org/10.1007/s12015-024-10742-2
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信