
近日,美国梅奥诊所在国际权威期刊杂志《肾脏国际报告》上发表了一项关于“动脉内自体间充质干细胞治疗糖尿病肾病”临床研究的文章[1]。
动脉内输注间充质干细胞治疗糖尿病肾病,肾功能衰退显著减缓
该研究首次在进展性糖尿病肾病(DKD)患者中开展自体脂肪来源间充质干细胞(MSC)经肾动脉输注的临床试验,旨在评估其安全性、耐受性以及对肾功能的潜在益处。研究发现,该疗法对患者耐受性良好,并可能有效减缓肾功能恶化的速度。
糖尿病肾病的病理特征与现有治疗方法
糖尿病肾病 (DKD) 的核心病理机制涉及慢性无菌性炎症引发的血管损伤,伴随氧化应激增强、晚期糖基化终末产物 (AGE) 积累、脂肪变性、胰岛素抵抗、肾脏缺氧、细胞衰老增加以及肾素-血管紧张素-醛固酮系统 (RAS) 异常激活。
目前,钠/葡萄糖协同转运蛋白抑制剂 (SGLT2i)、胰高血糖素样肽-1受体激动剂 (GLP-1RA)、非甾体盐皮质激素受体拮抗剂 (MRA) 和内皮素A受体拮抗剂等药物已被证明能降低DKD患者的心血管风险并延缓肾功能下降。
未解难题与治疗方向
然而,炎症作为驱动DKD进展的一个关键病理因素,尚未被现有疗法完全解决。因此,迫切需要开发和优化能够同时干预多重病理通路的多靶点治疗方法,以更有效地遏制DKD的复杂发病机制和进行性恶化。
间充质干细胞治疗糖尿病肾病的潜力与展望
间充质干细胞/基质细胞 (MSC) 源自多种组织(如骨髓、脂肪、脐带),能通过分泌生物活性物质(生长因子、细胞因子、细胞外囊泡)及细胞间接触促进组织修复。在DKD动物模型中,MSC治疗显示出减轻肾小球硬化、微量白蛋白尿、炎症、氧化应激和纤维化的效果。
随着2024年12月美国FDA批准首个MSC产品 (Ryoncil) 用于儿童类固醇难治性急性移植物抗宿主病,以及全球其他地区的类似批准,MSC的治疗潜力得到重要验证,这强调了推进其在DKD领域研究的必要性。
基于前期在动脉粥样硬化性肾血管疾病中的研究经验,提出通过肾动脉输注自体脂肪来源MSC治疗 DKD 在可行性和安全性上是值得探索的新策略。
方法:详细方法见补充方法和补充参考文献。
这项单中心、开放标签、剂量递增的试验在美国明尼苏达州罗切斯特的梅奥诊所进行,旨在评估自体脂肪来源间充质干细胞(MSC)动脉内给药在进展性糖尿病肾病(DKD)患者中的安全性(第一阶段)、耐受性和剂量反应。纳入标准详见补充表S1。
进展性糖尿病肾病定义为需药物治疗的糖尿病,并满足以下任一条件:
- a) 估算肾小球滤过率(eGFR)为25-55ml/min/1.73m²,且在18个月内下降≥5ml/min,或在3年内下降≥10 ml/min;
- b) Tangri肾衰竭风险评分处于中高风险水平。
受试者首先进行脂肪组织采集,随后对MSC进行分离、体外扩增并冷冻保存(见图1)。MSC给药方案包括两次动脉内输注(2.5×10⁵ 个细胞/公斤),分别在基线和三个月时注入同一侧肾脏。安全性和临床结局评估持续15个月。
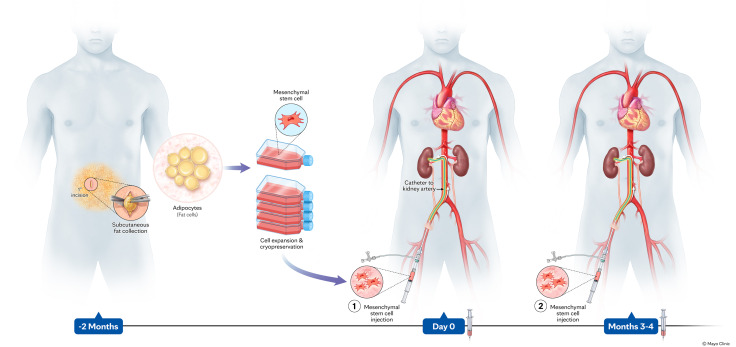
临床试验流程包括通过在腹部脐周区域开一个1-2英寸的切口,皮下提取脂肪组织。脂肪组织消化后分离、提取并扩增 MSC,随后进行严格检测,最后冷冻保存直至使用。MSC经肾动脉(同一肾脏)注射,间隔约3-4个月。
动脉内输注间充质干细胞治疗糖尿病肾病的结果
筛选和入组:2019-2020年,经过详细评估后,仅邀请两名受试者进行正式筛选并入组(补充图S1)。一名受试者因拒绝接受动脉MSC输注而退出。第二名受试者因COVID-19疫情爆发期间的医疗服务中断,在第0天和第4个月接受了MSC输注(延迟了一个月)。鉴于公共卫生部门对非必要旅行的限制,进一步入组工作暂停,试验随访也缩短。后续肾病护理在当地进行。
基线特征:受试者(70岁以上白人男性)患有归因于糖尿病肾病(DKD)的慢性肾脏病 (CKD),并有15年糖尿病病史,通过胰岛素、二甲双胍和GLP-1RA治疗,病情控制良好(糖化血红蛋白A1c,6.9%)。高血压治疗采用二氢吡啶类钙通道阻滞剂、血管紧张素转换酶抑制剂和噻嗪类利尿剂。蛋白尿<100毫克/24小时。基线和围手术期临床实验室值及安全性评估详见补充表S2。
安全性和耐受性
未发生输注相关、MSC相关的严重不良事件 (AE) 或手术并发症。在输注 MSC(包括少量碘化造影剂用于有限的血管显影)后,血清肌酐水平短暂升高(补充图S2)。值得注意的是,第一天血清肌酐水平的变化可能受到近期静脉注射造影剂的影响,该造影剂是在MSC输注前24-48小时进行的一项计划外的临床CT心脏成像检查中发现的。治疗后,红细胞沉降率和C反应蛋白未观察到显著变化。然而,白细胞、血小板和乳酸脱氢酶水平呈下降趋势。
肾功能变化
在MSC治疗前阶段,估算的年化eGFR绝对变化为-7.02(标准误差;SE3.15)mL/min/1.73m²/年;而在MSC治疗后阶段,该估算值为-1.84(SE 0.53)mL/min/1.73m²/年。图2展示了eGFR值叠加在MSC治疗前后(大约5年)两个阶段的年化eGFR绝对变化估算,肌酐变化轨迹见补充图S3。
![图2:长期肾功能随访:MSC治疗前后。间充质干细胞 (MSC) 输注前后肾功能变化(根据2021年CKD-EPI估算的肾小球滤过率[eGFR])。 图2:长期肾功能随访:MSC治疗前后。间充质干细胞 (MSC) 输注前后肾功能变化(根据2021年CKD-EPI估算的肾小球滤过率[eGFR])。](https://www.hjtdsm.com/wp-content/uploads/2025/08/2025080809425719.jpg)
讨论动脉内输注间充质干细胞治疗糖尿病肾病的有效性
本研究展示了若干新颖且具有临床意义的发现。这是首项在糖尿病肾病(DKD)患者中采用自体MSC经肾动脉给药的临床研究。即使来源于老年DKD患者,也能够成功制备具备治疗潜力的MSC。动脉内给药的耐受性良好。值得注意的是,MSC治疗显著减缓了肾功能的下降速度(eGFR年下降率从-7.0改善至-1.8mL/min/1.73m²/年)。
近期,美国FDA已认可eGFR下降速率作为评估肾病治疗药物加速审批的替代终点指标,并据此批准了在REGEN-006(PROACT1)III期临床试验中应用的专有自体细胞疗法Rilparencel。总体而言,这些结果支持进一步探索MSC疗法作为延缓DKD进展的潜在治疗策略。
自体间充质干细胞治疗糖尿病肾病的安全性:2016年,Packham等人进行了一项多中心、随机、双盲、剂量递增、安慰剂对照试验,在DKD患者(n=30)中评估了静脉注射的异体间充质前体细胞的安全性,结果未发现输注相关或治疗相关的严重不良事件(SAE)。

2023年,Perico等人报道了一项欧洲多中心试验的结果,使用骨髓来源、抗CD362筛选的异体MSC(ORBCEL-M)治疗进展性DKD成人患者。接受ORBCEL-M治疗的受试者(n=12,按3:1比例随机分组)在安全性方面表现良好,且较安慰剂组(n=4)肾功能下降速度更慢。与上述研究结果一致,我们的研究也展示出良好的安全性。然而,术后肌酐水平的升高提示,在今后的研究中应考虑替代的血管造影策略(如使用二氧化碳成像),以避免即便是微量碘造影剂的暴露。

自体间充质干细胞治疗糖尿病肾病的给药途径:局部或动脉内输注MSC可能通过避免肺部首过效应、减少肺部细胞滞留,从而提高细胞植入效率。尽管如此,静脉输注后的肺巨噬细胞介导的清除作用仍可能通过持续释放促修复信号而产生治疗效应。虽然静脉输注在创伤性和经济性上具有优势,但动脉内肾脏输注具有更高的治疗潜力。
Abumoawad等人曾在肾血管疾病患者中进行两次动脉内MSC输注,结果显示肾功能和肾氧合均有改善。
最近,Carstens等人在18例原因不明CKD(美洲肾病)患者中开展研究,评估自体脂肪来源血管基质细胞动脉内给药的安全性,结果表明在eGFR≥30 mL/min/1.73m²的患者中,肾功能有改善趋势。在本研究中,受试者eGFR也高于30 mL/min/1.73m²,因此可能从MSC治疗中获得长期肾脏获益。
MSC联合降糖治疗以实现最佳肾修复效果:在进展性DKD中,应综合考虑同时使用的药物治疗,包括ACEi/ARB、二甲双胍、SGLT2抑制剂、GLP-1受体激动剂以及非类固醇MRA等。在本研究中,受试者最初表现为肾功能稳定,但后续出现数次急性肾损伤,导致eGFR继续下降,尽管下降速度已减缓。
在长期随访中,大约在第1.5至2.5年期间启动了SGLT2抑制剂治疗。需要指出的是,该患者在MSC治疗前即已长期使用GLP-1RA和二甲双胍,仍出现了进展性DKD。这提示MSC疗法若与现代降糖药物联合使用,或能进一步提升疗效并降低DKD治疗相关的经济负担。
结论
在一名老年进展性DKD患者中,经动脉内输注的自体MSC疗法耐受性良好。在与现代DKD治疗手段联合使用的背景下,MSC治疗显著减缓了DKD的进展速度。本研究是首项在DKD患者中实施MSC动脉内给药的临床探索,为后续再生医学及细胞治疗策略在防止肾衰竭中的应用奠定了基础。
参考资料:[1]:https://www.sciencedirect.com/science/article/pii/S2468024925004863#bib10
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信