在再生医学迅猛发展的今天,我们正见证着医疗理念从“控制症状”走向“修复神经”的革命性转变。
在这一变革浪潮中,干细胞疗法正在为许多长期依赖药物控制、却难以逆转病程的神经退行性疾病带来新的希望,其中,帕金森病的治疗领域尤为引人关注。
然而,对于许多患者和家属而言,“干细胞治疗帕金森病” 仍然是一个既令人期待又略显陌生的概念——为什么这些看似普通的细胞,能够替代已经死亡的神经元?它们进入大脑后究竟如何发挥作用?与传统药物或脑深部电刺激相比,这种新疗法到底带来了怎样的改变?
本文将带您系统了解干细胞疗法治疗帕金森病的科学原理,解析它如何修复神经系统并改善帕金森病症状的,并结合临床研究进展与未来方向,全面呈现这一前沿治疗的真实图景。

一、帕金森病的核心困境:多巴胺神经元的凋零
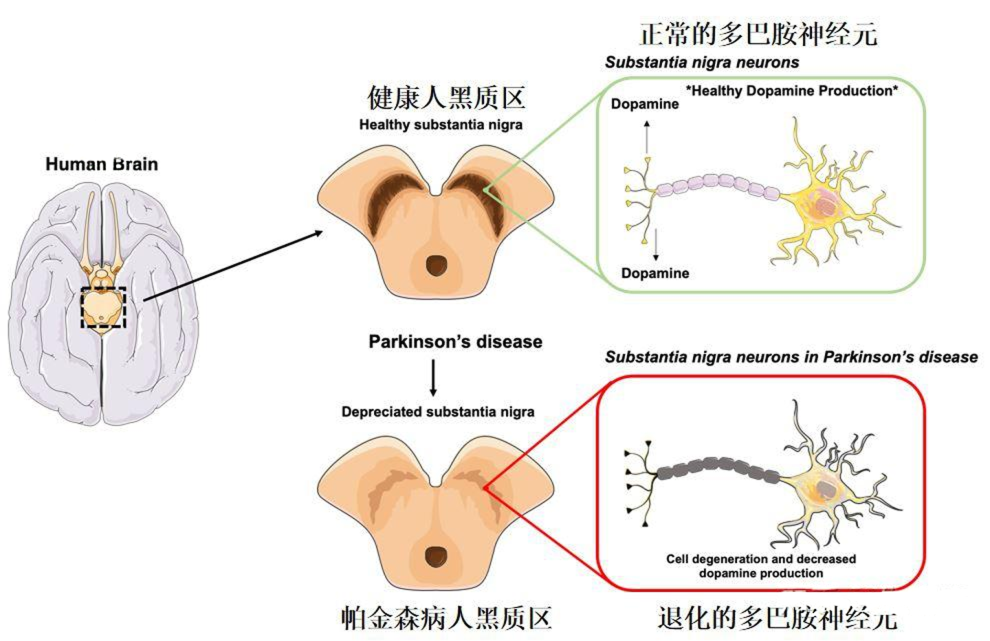
理解干细胞疗法,必须从帕金森病的根源开始。该病的核心病理变化发生在中脑一个名为“黑质”的区域——这里分泌多巴胺的神经元发生进行性、不可逆的死亡。
多巴胺是大脑中关键的神经递质,负责协调精细运动。当这些细胞丧失超过60-80%时,运动功能障碍便会显现。
传统药物治疗的局限性当前主流的左旋多巴等药物,如同为枯竭的泉水临时引水,只能补充多巴胺,却无法阻止神经元的继续死亡。
随时间推移,药物疗效逐渐减退,还会引发剂末现象、异动症等副作用。全球近1000万帕金森病患者中,约40%在治疗5年后出现严重并发症。
二、什么是干细胞疗法?它与传统治疗的根本区别
干细胞疗法代表了一种全新的治疗范式,其核心理念与传统方法有根本性区别。我们可以用一个简单比喻来理解:
- 传统药物治疗(如左旋多巴):如同给干涸的土地持续浇水——暂时补充缺失的多巴胺,但无法阻止水源(神经元)的持续流失。随着病程发展,需要的水量越来越大,效果却越来越差,还可能引发”剂末现象”和”异动症”等并发症。
- 干细胞疗法:则像是直接播种新的水源。它不再满足于临时补充,而是致力于从根本上修复生态系统——替换那些已经死亡的多巴胺能神经元,重建大脑正常的神经调节网络。
核心机制:利用干细胞这种具有自我更新和定向分化能力的”万能种子”,在实验室精心培养和诱导后,通过精准的神经外科手术移植到患者大脑的特定区域。这些细胞将在脑内成熟为功能性的多巴胺神经元,与现有神经网络建立连接,从源头上恢复多巴胺的自主分泌和运动功能的持久调节。
这种从”替代治疗”到”再生修复”的转变,正是干细胞疗法最具革命性的突破——它不仅控制症状,更直指疾病根源,为帕金森病的长期管理提供了全新的可能性。
三、 干细胞疗法是如何起作用的?
干细胞移植后通过三重协同机制发挥治疗作用,形成全方位的修复网络:
1. 直接细胞替代:移植的干细胞在脑内分化为成熟的多巴胺能神经元,直接填补因疾病丧失的细胞空缺。这些”新生代神经元”能够整合到现有神经回路中,自主分泌多巴胺,恢复运动调节功能。
2. 神经营养支持:干细胞持续分泌脑源性神经营养因子、胶质细胞源性神经营养因子等多种营养因子,为残存的神经元提供保护,延缓其退化进程,创造有利于神经修复的微环境。
3. 免疫调节与抗炎:研究证实,干细胞能够调节脑内过度活跃的免疫反应,减轻慢性神经炎症——这是导致神经元进行性死亡的关键因素之一。通过抑制有害的免疫反应,干细胞为神经修复创造有利条件。
这三重机制相互协同,共同构建了一个自我维持的修复系统,为帕金森病的长期改善提供了可能。
四、治疗帕金森病的常用干细胞类型:各有特点与优势
目前用于帕金森病研究的干细胞主要分为四类,各有其取材来源、安全性和应用潜力:
| 干细胞类型 | 来源 | 核心优势 | 应用现状 |
| 神经干细胞 | 胎儿脑组织、诱导分化 | 可直接分化为多巴胺能神经元,与帕金森病所需修复的损伤部位高度匹配,神经特异性高 | 近年研究热点,多项研究显示可改善运动症状与脑功能指标 |
| 间充质干细胞 | 骨髓、脐带、脂肪组织 | 取材便捷、免疫原性极低(不易引发排斥)、可批量获取 | 临床研究最广泛,安全性已初步验证 |
| 诱导多能干细胞 | 患者自体体细胞(如皮肤细胞)重编程 | 可 “个性化定制”(避免免疫排斥)、可定向分化为高纯度多巴胺能神经元 | 近年研究热点,部分进入早期临床试验 |
| 胚胎干细胞 | 早期胚胎 | 分化能力最强,可生成各类神经细胞 | 伦理争议大,多数国家限制临床应用 |
其中,神经干细胞以及诱导多能干细胞因其高度针对性和更接近疾病本质的修复机制,正成为研究与临床探索的重点方向。
五、临床研究进展:从实验室走向患者的 “关键突破”
近年来,干细胞疗法治疗帕金森病的临床研究已从 “基础实验” 逐步迈向 “人体试验”,多项临床试验结果显示出积极潜力:
国内首例自体iPSC神经细胞移植,实现从“患者”到“见证者”的突破
在第29个世界帕金森病日来临前夕,中国首例帕金森病患者接受GCP级自体干细胞移植治疗的帕金森病患者,2025年4月8日现身上海瑞金医院科普活动现场,首度面向公众分享其阶段性康复体验。[1]
这也意味着,中国首例帕金森病患者通过国际标准临床试验,用自身干细胞修复受损脑神经,迈出细胞治疗帕金森病的关键一步。

作为我国首位通过国家药监局批准的GCP级临床试验参与者,沈女士于3月1日接受手术,通过微创方式将自体诱导多能干细胞(iPSC)分化的多巴胺能神经前体细胞移植至脑内特定区域。
术后仅1个月,她已实现全天自主行走,睡眠质量显著改善,肢体僵硬与震颤症状明显缓解。这一案例标志着我国在 细胞治疗帕金森病领域 取得重大突破,为全球神经退行性疾病治疗提供了“中国方案”。
沈女士在分享中提到:
“手术后第二天就能下地走路,睡眠质量从每晚2小时提升到6小时”;
“每天都能感受到细微进步,这种‘向好’的感觉让我重拾信心”;
“希望未来更多患者能像我一样,不必终生效药物控制”。
这一案例标志着我国在细胞治疗帕金森病领域迈出了关键一步,为全球神经退行性疾病的创新治疗提供了全新的“中国方案”。
亚洲首次人胚胎干细胞神经元移植试验,验证安全性与有效性的新里程碑
2025年10月14日,延世大学Severance研究团队公布了亚洲地区首次、全球范围内第二次报道的通过移植源自人胚胎干细胞的A9型多巴胺前体细胞(A9-DPC),成功实现了对中重度帕金森病患者的精准治疗。[2]

这项单中心、开放标签的临床试验历时12个月,纳入12名病程超过5年的帕金森病患者。通过立体定向手术,将细胞精确移植至患者双侧壳核区域,其中低剂量组(315万细胞)和高剂量组(630万细胞)各6例。
研究数据显示,干细胞移植在安全性方面表现良好。整个试验中仅出现少量轻微不良反应,多与免疫抑制药物相关,无严重并发症或细胞异常增殖。影像学结果也证实,移植细胞精准分布,无异常迁移或肿瘤形成。
疗效方面,患者在术后12个月运动功能平均提升14分以上,高剂量组效果更为显著。日常活动能力、生活质量及药效持续时间均有明显改善。分子影像学进一步验证了这一变化:移植区域的多巴胺转运体活性显著增强,说明移植细胞成功整合进神经系统,部分恢复了多巴胺通路功能。
组织分析显示,移植的细胞已在宿主体内分化为成熟的多巴胺神经元,并与原有神经网络形成有效连接。这一结果标志着人源胚胎干细胞衍生细胞治疗帕金森病的安全性与可行性得到初步验证,为未来大规模临床应用奠定了基础。
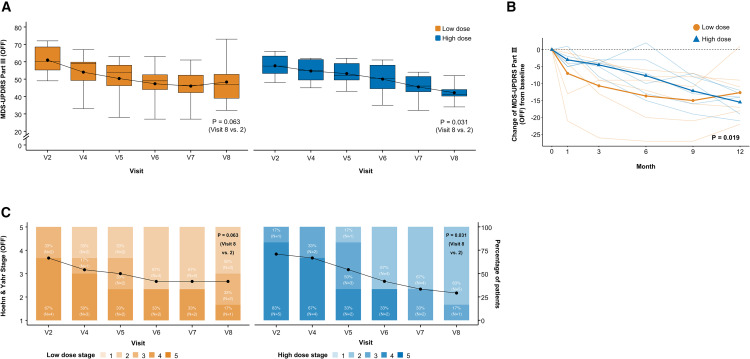
该研究的最大突破,在于首次系统验证了人胚胎干细胞衍生神经元治疗帕金森病的可行性与安全性。与过去依赖胎儿组织移植不同,这一方案在伦理、来源及生产标准上都实现了突破。采用新鲜细胞移植的策略,也最大限度地保留了细胞活性。科学的剂量设计,源自前期动物实验的积累,使得疗效更具可靠性。
详情请浏览:2025干细胞疗法治疗帕金森病最新临床指南(截至10月)
六、现存挑战与未来方向:让 “希望” 落地的关键
尽管干细胞疗法为帕金森病治疗带来了革命性希望,但从实验室成果转化为稳定、可靠的临床方案,仍有一段关键路程需要跨越。当前面临的核心挑战主要集中在以下几点:
首先,移植细胞的存活与整合效率仍需提升。研究表明,移植后仅有部分细胞(约15-30%)能在复杂的大脑环境中长期存活并成功融入原有的神经回路,发挥功能。这好比将珍贵的种子播撒后,需要确保它们能在新“土壤”中扎根生长。
其次,治疗的标准化与安全性需持续验证。如何精确控制细胞分化、确保无肿瘤风险、并最小化免疫排斥,是大规模临床应用前必须解答的问题。
针对这些挑战,未来的突破方向正变得清晰:
- 活体监测技术:运用先进的影像学手段,实时追踪移植细胞在体内的命运,实现疗效的可视化评估。
- 基因工程技术:通过编辑干细胞基因,增强其抗凋亡和适应能力,让移植细胞更“顽强”。
- 新型生物材料:开发仿生支架或凝胶,为移植细胞提供支撑与营养,创造一个更友好的生存微环境。
- 个体化精准医疗:结合患者基因图谱与疾病特征,定制专属的细胞疗法方案。
结语:不止于“缓解”,更向“治愈”靠近
帕金森病的治疗正在经历从“对症”到“对因”的历史性转变。干细胞疗法代表着这一转变的最前沿——它不仅旨在缓解颤抖,更致力于修复颤抖的根源。
全球超过200项相关临床试验正在进行,每项研究都在为最终的安全有效治疗积累宝贵数据。虽然前路仍有科学难题需要攻克,但每一次移植尝试,都为千万帕金森病患者带来重获生活品质的新希望。
科学的价值在于将不可能变为可能。随着再生医学、基因工程和神经科学的深度融合,根治帕金森病这一愿景,正从遥不可及的未来,逐渐变为可规划的现实路径。
对于正在与疾病抗争的患者而言,了解这些进展不仅是获取信息,更是储备希望——在医学不断突破边界的时代,今天的尖端研究,可能就是明天的常规治疗。
参考资料:
[1]https://mp.weixin.qq.com/s/FvDBPHYykFR83WXTdBH-VA
[2]Phase 1/2a clinical trial of hESC-derived dopamine progenitors in Parkinson’s diseaseChang, Jin Woo et al.Cell, Volume 0, Issue 0
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信