在过去的二十年中,大量临床前研究表明,干细胞移植在缺血性中风模型中具有巨大潜力。干细胞并非主要通过直接替代丢失的神经元来发挥作用,而是通过多种间接机制,包括提供营养支持、减少细胞凋亡、增强大脑可塑性、抑制梗死周围区域的炎症以及促进血管生成。
然而,尽管已经完成了多项随机对照试验,干细胞疗法在缺血性中风患者中的安全性和有效性仍不确定,缺乏标准化的治疗方案也进一步增加了临床转化的复杂性。
干细胞疗法破局缺血性卒中治疗?17项研究999例患者Meta分析给出肯定答案
在此背景下,《卒中与血管神经病学》发表一篇“干细胞疗法治疗缺血性卒中患者的疗效和安全性:随机对照试验的系统评价和荟萃分析”的研究综述[1]。

本篇荟萃分析旨在系统性地评估临床干细胞疗法在缺血性中风患者中的治疗效果和安全性,对目前可获得的证据进行全面综述。
结果这项荟萃分析表明,干细胞疗法可显著改善缺血性卒中患者的改良Rankin量表评分和Barthel指数(BI)评分,并降低死亡率,且未增加不良事件的发生率。然而,这些功能性获益较为脆弱,因为在敏感性分析中,统计学意义(尤其是BI评分)消失,且未观察到神经功能障碍(美国国立卫生研究院卒中量表)的显著改善。这凸显了需要更多高质量证据来证实该疗法的总体临床疗效。
这项应该怎么做,研究的方法是什么?
方法:检索截至2025年11月的文献,数据库包括OVID Medline、EMBASE、Scopus、Cochrane对照试验中心注册库、Web of Science和ClinicalTrials.gov。
纳入标准遵循人群、干预、对照、结局(PICO)框架:影像学确诊的成人缺血性卒中(IS)患者,接受任何人类干细胞治疗(非神经或神经靶向治疗)、安慰剂或标准医疗护理,并评估功能或神经系统结局(改良Rankin量表(mRS)、Barthel指数(BI)、美国国立卫生研究院卒中量表(NIHSS))、死亡率或不良事件,随访时间≥6个月。仅纳入随机对照试验。
统计分析采用随机效应模型的荟萃分析,比较干细胞治疗组与对照组在疗效和安全性方面的差异。使用I²统计量评估研究间的异质性,并采用Cochrane偏倚风险评估工具2.0版(RoB 2)评估偏倚风险。
两项结果数据呈现:搜索结果、临床数据结果
搜索结果
共筛选了2049篇独特的文章(通过标题和摘要)。其中,25篇符合全文筛选条件,最终纳入17项试验(图1)。荟萃分析共纳入999例患者,其中495例接受了干细胞疗法干预,504例作为对照组。
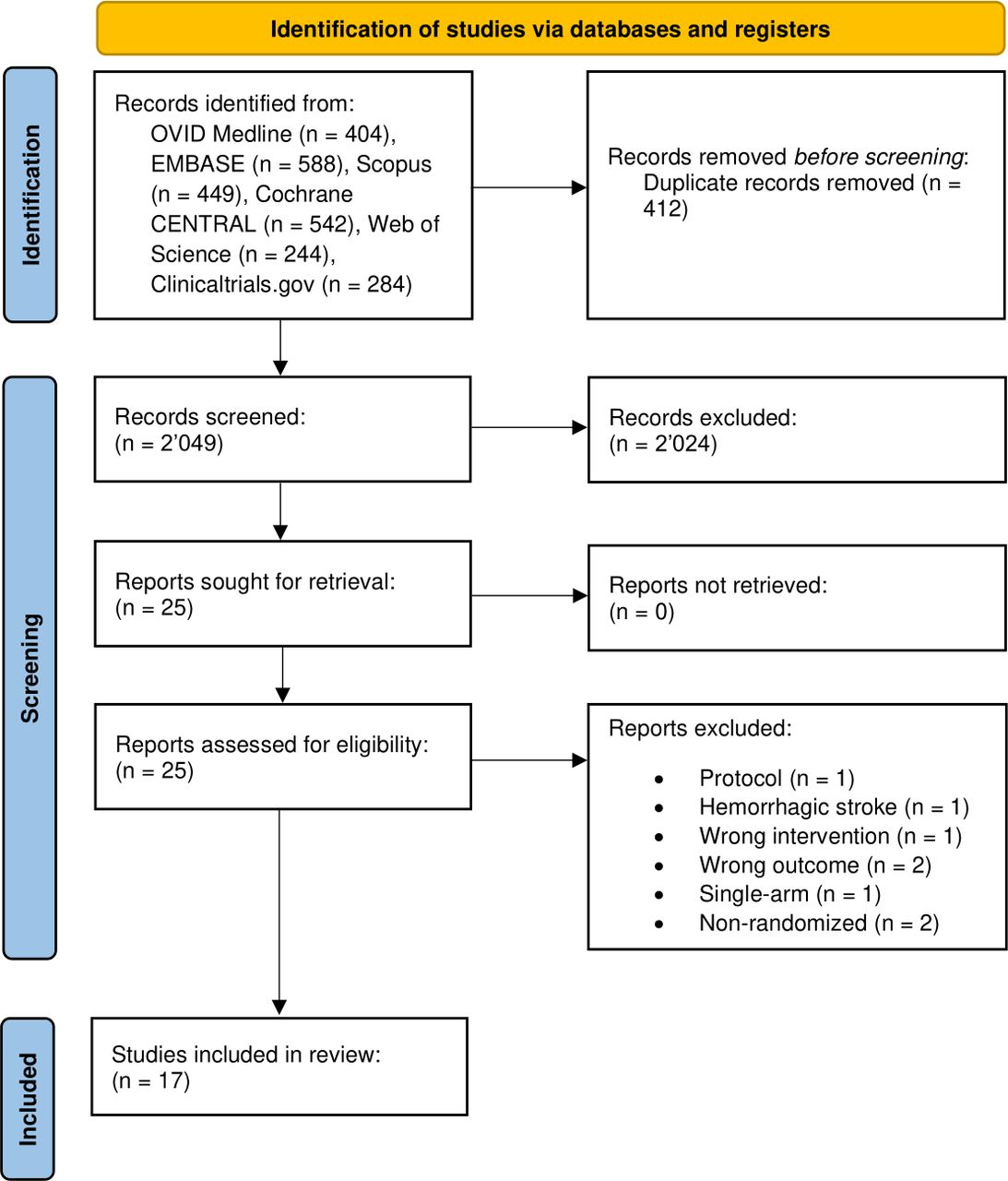
研究特征
本荟萃分析所纳入的研究在时间跨度、疾病阶段与随访时长上呈现显著异质性。研究发表于2005年至2025年这二十年间,表明该领域积累了长期探索。在疾病阶段上,研究重点分布不均,绝大多数集中于急性期(41%)与亚急性期(47%),仅少数(12%)关注慢性期治疗,这反映了当前研究更青睐于卒中早期干预窗口。此外,各研究的随访时间差异极大,从6个月到7年不等(表1),提示对疗效持久性的评估标准尚未统一。表2还列出了纳入研究中患者的基线特征。
在干细胞治疗的具体方案上,细胞来源与类型呈现高度多样性。绝大多数研究(76%)采用自体干细胞,凸显了其对免疫相容性与安全性的重视;而异体干细胞应用(24%)则为即时治疗提供了可能。细胞类型以骨髓来源为主,其中骨髓间充质干细胞(18%)和骨髓单核细胞(24%)最为常用,但整体谱系广泛,还涵盖了造血干/祖细胞、脂肪来源干细胞、甚至胚胎与脐带来源细胞的联合疗法,这体现了研究者正在从不同机制角度探索最佳细胞选择。
治疗的给药途径与剂量方案同样缺乏标准化:静脉输注是最主流的给药方式(59%),因其操作简便、侵入性低;动脉内注射(24%)作为另一种全身性途径也占一定比例。仅有少数研究采用了更具靶向性的局部递送方式,如鞘内注射(12%)或直接脑内注射(6%)。
在剂量方面,各研究间差异巨大,多数(76%)采用固定剂量,而部分(24%)则根据患者体重调整,目前远未形成基于疗效或生物标志物的剂量共识。这些特征共同揭示了该领域仍处于探索阶段,方案标准化是未来研究的关键挑战。
临床数据主要结果
临床结果评估:本研究通过荟萃分析评估了干细胞治疗对脑卒中患者的疗效与安全性。在临床结局方面,分析显示干细胞治疗在改善功能残疾和日常生活能力方面具有明确优势。
改良Rankin量表(mRS):具体而言,基于包含824名患者的15项试验的数据,干细胞治疗组在改良Rankin量表评分的改善上显著优于对照组(均数差=-0.27,95%CI-0.51至-0.03, p=0.027)(图2A)。
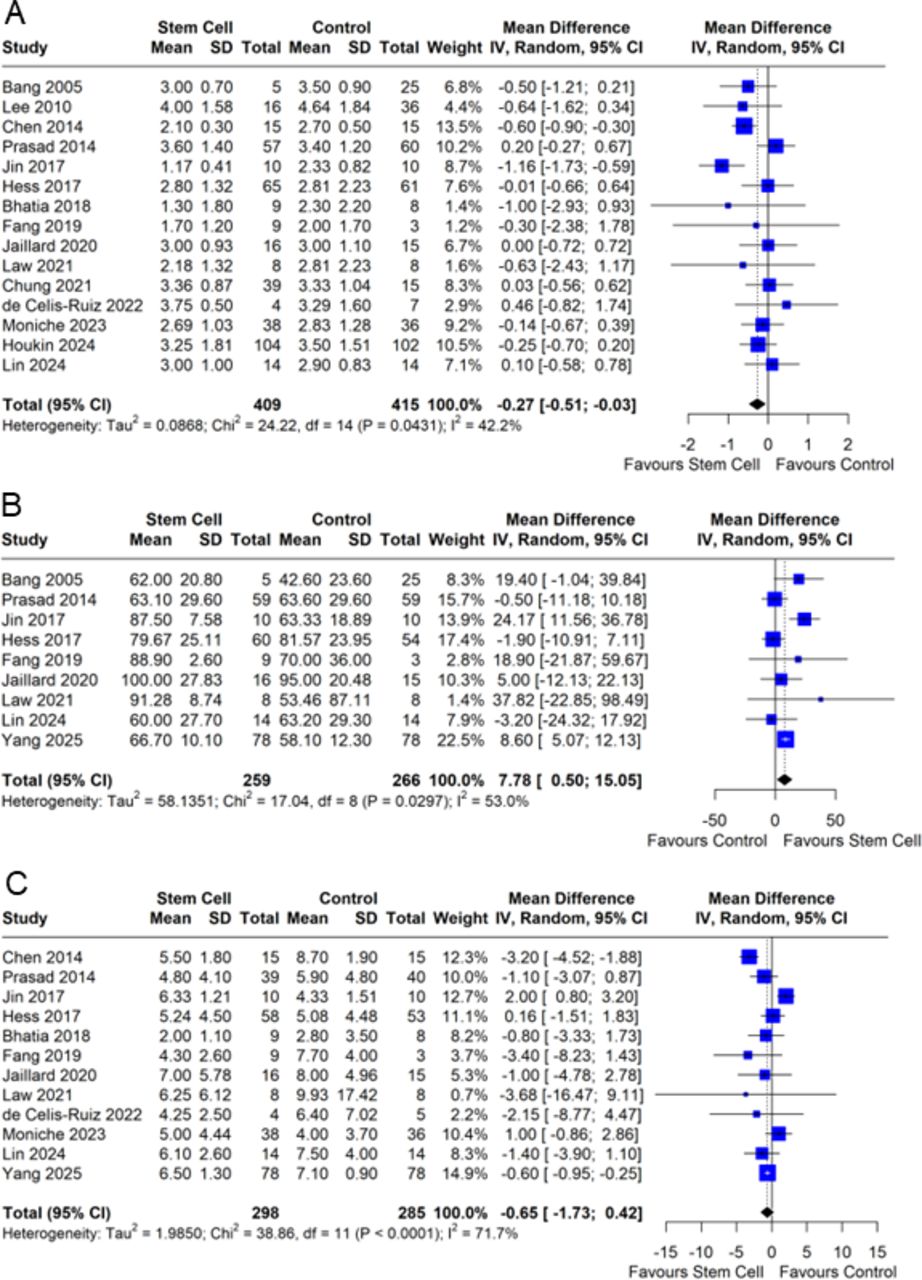
巴特尔指数(BI):同时,对525名患者的9项试验分析表明,治疗组的Barthel指数也显著更高(均数差=7.78,95%CI 0.50至15.06, p=0.036),提示日常生活能力得到更好恢复。然而,研究并未发现干细胞治疗在所有神经功能评估指标上均具优势(图2B)。
美国国立卫生研究院卒中量表(NIHSS):针对美国国立卫生研究院卒中量表,对583名患者的12项试验的汇总分析显示,治疗组与对照组相比未显现出显著差异(均数差=-0.65,95%CI-1.73至0.42, p=0.24)。这表明干细胞治疗在改善该特定神经功能缺损评分方面,未能显示出明确的有利结局(图3C)。
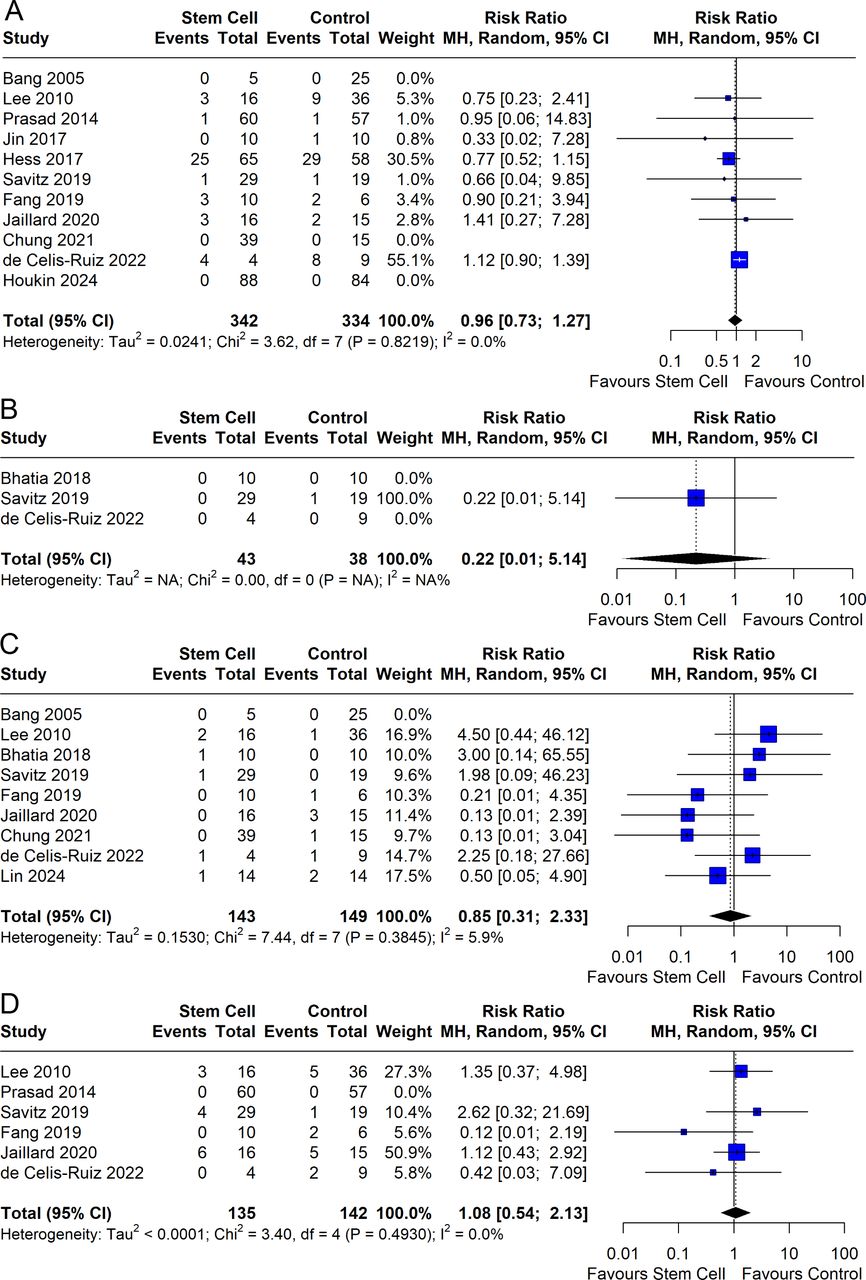
在安全性评估方面,结果显示出积极信号。死亡率数据显示,干细胞治疗组的死亡风险显著低于对照组(图3),相对危险度为0.64(95%CI 0.42至0.98, p=0.040),且各研究间无异质性(I²=0%)。
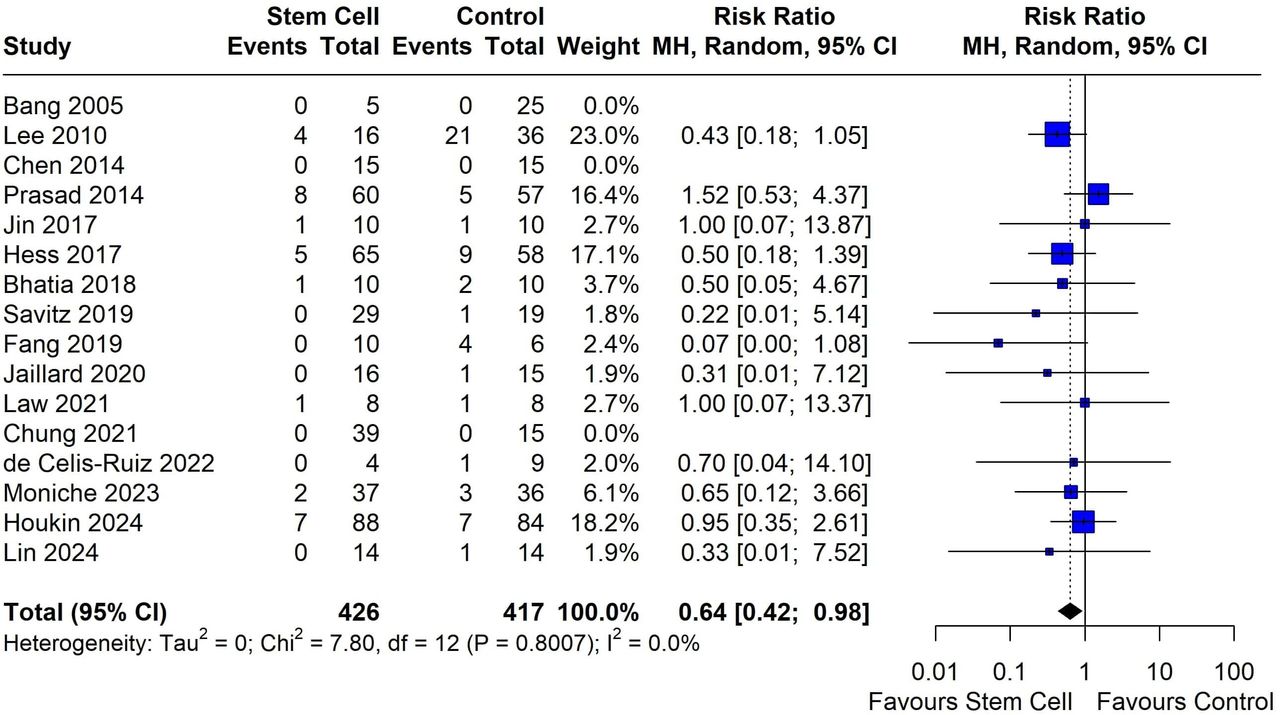
同时,所有研究中均未报告与治疗相关的严重神经功能恶化或肿瘤转化病例,总体不良事件分析也显示治疗组与对照组无显著差异(图4)。
综上所述,现有证据表明干细胞治疗可显著改善脑卒中患者的功能残疾(mRS)和日常生活自理能力(BI),并可能降低死亡率,且安全性良好。但治疗在改善NIHSS评分方面未显示明确益处。需要指出的是,部分原始研究的数据缺失(各指标分别有6%-18%的研究数据无法获取)可能对分析结果的完整性产生一定影响。
干细胞治疗缺血性卒中:循证评估、临床转化挑战与未来展望
1、干细胞治疗缺血性卒中的核心疗效与安全性结论是什么?具体有哪些数据支持?
本荟萃分析综合了多项随机对照试验的数据,得出核心结论:干细胞治疗在改善卒中后功能残障和降低死亡风险方面具有潜力,且未增加严重安全性风险。
疗效方面:与对照组相比,接受干细胞治疗的患者在整体功能恢复(改良Rankin量表评分) 和日常生活活动能力(巴氏指数评分) 方面获得了具有统计学意义的显著改善。同时,治疗组的总体死亡率显著降低。然而,专门用于评估神经功能缺损严重程度的美国国立卫生研究院卒中量表评分在主要分析中未显示显著改善。
安全性方面:分析未发现干细胞治疗与 肿瘤形成、严重神经功能恶化或症状性颅内出血 等严重不良事件相关。其他常见不良事件(如感染、癫痫、复发性卒中)的发生率在治疗组与对照组之间无显著差异。仅有一项个别研究报告了治疗组死亡率较高,但该结果与整体趋势不符。
2、为什么不同评估指标(如mRS、BI与NIHSS)的结果会出现差异?这说明了什么?
这种差异可能揭示了干细胞治疗的作用机制和不同评估工具的侧重点:
mRS和BI是评估患者整体功能状态和日常生活独立性的综合量表,涵盖运动、认知、活动等多个维度。它们的改善提示干细胞治疗可能通过促进大脑整体修复网络,帮助患者实现更有意义的临床功能恢复。
NIHSS则更侧重于量化急性期神经功能缺损的严重程度,如语言、视野、感觉、运动等特定项目。其改善不明显可能意味着,在现有治疗方案下,干细胞对于逆转急性期形成的、明确的核心神经缺损效果有限。
综合解读:这种差异提示,干细胞治疗的主要获益可能不在于“修复”已坏死的神经细胞,而在于通过调节免疫、促进内源性修复、改善微环境(即“旁分泌效应”) 来保护周边脑组织、促进神经可塑性,从而在宏观功能层面实现改善。这也解释了为何治疗在急性期、亚急性期甚至慢性期都可能观察到益处。
3、哪些关键因素被证实会显著影响干细胞治疗的疗效?
亚组分析揭示了多个影响疗效的关键变量,强调了“个性化”治疗方案的重要性:
给药途径:靶向局部递送(如腰椎穿刺鞘内注射、立体定向脑内注射)的疗效似乎优于全身性递送(静脉或动脉注射)。前者能将更多细胞直接送达病灶区域,绕过血脑屏障。
治疗时机:存在一个 “时间窗-疗效谱”。
- 急性期(≤7天) 和慢性期(>3个月) 治疗,与美国国立卫生研究院卒中量表评分的改善更相关。
- 亚急性期(8天-3个月) 治疗,则与巴氏指数评分的改善更相关。
这表明,不同疾病阶段的病理生理微环境可能适合干细胞发挥不同的修复作用。
细胞来源:自体干细胞(取自患者自身)与mRS和BI的显著改善相关。异体干细胞(取自供体)则与NIHSS的显著改善相关。这种差异可能源于两者免疫原性和旁分泌因子谱的不同,且受现有临床试验数量不均的限制。
4、当前证据的质量和可靠性如何?主要存在哪些局限性?
尽管结果积极,但证据基础存在显著局限性,结论的稳健性有待提升:
- 证据质量等级:总体评为 “中等”。
- 主要偏倚风险:大部分研究因采用 单盲或开放标签设计,存在中度偏倚风险。患者和评估者知晓治疗分配,可能影响主观结局指标(如mRS)的评估。
- 高度异质性:各研究在细胞类型、剂量(从百万到十亿级)、给药途径、治疗时机、随访时间上差异极大,导致结果难以简单合并。统计分析表明,整体结论很大程度上受到个别阳性结果显著的小型研究的影响,当剔除这些研究后,部分积极效应消失。
- 样本量与长期数据:多数试验样本量小,统计效力不足。同时,缺乏长期(>5年)的安全性及疗效随访数据。
5、基于现有证据,干细胞治疗面临哪些主要挑战,阻碍其成为常规临床疗法?
干细胞治疗要走向临床常规应用,必须解决以下几个核心挑战:
- 标准化方案缺失:目前尚无公认的最佳细胞类型、最适剂量、黄金给药途径和确定治疗时间窗。治疗方案“五花八门”。
- 技术与物流瓶颈:靶向给药技术(如脑内注射)操作复杂、普及性低。干细胞制备需要严格的GMP标准、昂贵的培养设施和复杂的冷链运输,成本高昂。
- 与现有疗法的协同未知:干细胞与卒中后常规药物(抗血小板、降压药等)或康复训练之间的相互作用尚未明确。康复介入的时机若不当,甚至可能削弱干细胞疗效。
- 疗效验证不充分:现有阳性结果多来自小规模、异质性高的研究,亟需大规模、同质化的III期试验进行确证。
6、未来研究的明确方向和优先事项是什么?
未来的研究应致力于将潜力转化为确凿的临床证据,重点方向包括:
- 开展确证性III期试验:优先进行大规模、多中心、双盲、安慰剂对照的III期随机对照试验,采用 一致化的治疗协议,以提供高级别证据。
- 优化治疗策略:通过研究明确:不同卒中亚型(如大血管闭塞vs小血管病)的最佳给药方式。细胞剂量与疗效的量效关系。干细胞治疗与最佳康复方案的协同时序。
- 深入机制研究:借助影像学和生物标志物,在人体内进一步阐明干细胞发挥作用的 具体分子和细胞机制。
- 解决转化障碍:开发更高效、微创的递送技术(如聚焦超声开放血脑屏障),并建立标准化、可扩展的细胞生产与质控流程,以降低成本和提升可及性。
总结
总之,干细胞治疗为缺血性卒中后遗症的修复带来了充满希望的新范式,但其道路并非坦途。当前证据足以支持其值得进一步深入探索,但尚不足以支撑其成为标准治疗。未来的成功将取决于能否通过严谨、大规模的研究回答上述核心问题,并克服技术转化瓶颈。
参考资料:
注:考虑到文中的表1,表2数据过多,嵌入文章中会影响用户阅读体验,可后台留言小编获取!
[1]:de Wilde D, Saemann A, Guzman R. Efficacy and safety of stem cell therapy in ischemic stroke patients: a systematic review and meta-analysis of randomised controlled trials. Stroke and Vascular Neurology. 2026;:svn-2025-004796. https://doi.org/10.1136/svn-2025-004796
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信