脊髓损伤(SCI)仍然是一种致残性神经系统疾病,有效的治疗选择有限。人诱导多能干细胞衍生的神经干/祖细胞(hiPSC-NS/PCs)通过实现神经替代、促进髓鞘再生和调节受损微环境,提供了一种极具前景的再生策略。临床前模型的研究进展,以及首个基于hiPSC的SCI治疗临床试验的启动,进一步增强了该方法的转化应用潜力。
多能干细胞来源的神经干/祖细胞疗法治疗脊髓损伤:临床进展和转化展望
2026年1月9号,知名期刊杂志《Stem Cells Translational Medicine》发表了一篇“人诱导多能干细胞衍生的神经干/祖细胞疗法治疗脊髓损伤:临床前进展和转化展望”的研究综述[1]。

该研究综述主要综述了神经干细胞移植治疗脊髓损伤的生物学特性、作用机制以及临床前和临床研究的最新进展。此外,我们还探讨了该技术在临床应用方面的未来前景和挑战。
总而言之,这些研究成果凸显了基于hiPSC的再生医学在脊髓损伤治疗领域具有多样化、创新性和转化应用潜力。
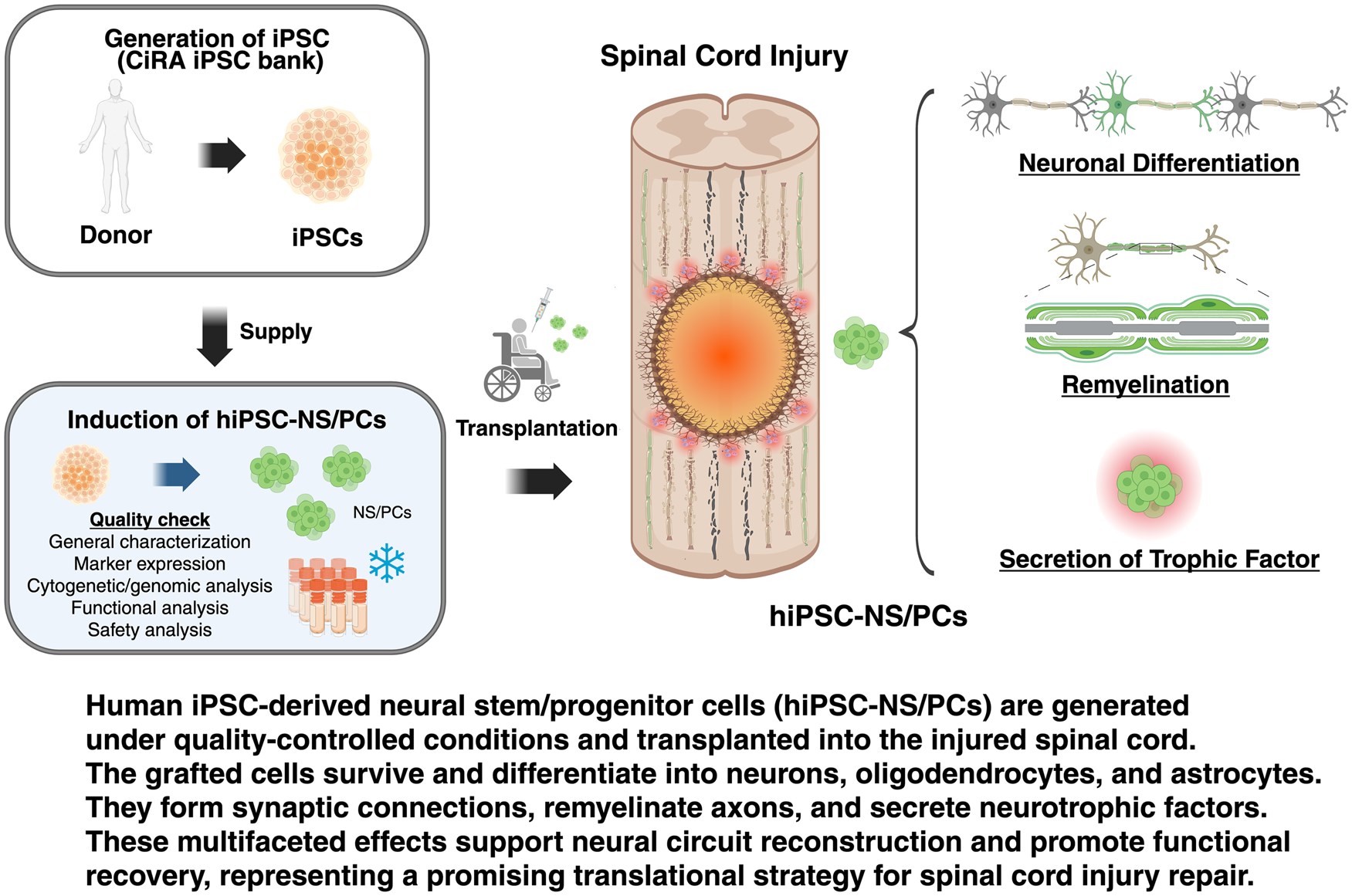
脊髓损伤的流行病学和治疗挑战
脊髓损伤(SCI)的流行病学呈现出全球性负担重、病因多样化的特点。全球有超过1500万患者,其中创伤性损伤(如交通事故、跌倒、运动损伤和暴力)是主要原因。值得注意的是,随着人口老龄化加剧,非创伤性病因(如退行性脊柱疾病、肿瘤和血管病变)的贡献日益显著,老年人因轻微跌倒导致颈椎损伤的病例尤为常见。
这使得SCI不仅是突发性的灾难性事件,也成为与年龄相关的重要健康问题,给患者家庭和社会带来沉重的长期照护及经济负担。
在治疗方面,脊髓损伤面临的根本性挑战在于中枢神经系统的内在修复能力极弱。原发性损伤会引发一系列复杂的继发性病理级联反应(如炎症、缺血、胶质瘢痕形成),进一步阻碍神经再生。
当前的标准临床治疗以手术减压、康复训练和症状管理为主,虽能改善部分功能并预防并发症,但无法实现神经结构的真正重建与功能的完全恢复。
因此,治疗的核心挑战是如何有效促进轴突再生、重建神经连接、并恢复丧失的感觉、运动与自主神经功能。正是在此背景下,基于干细胞的再生医学,尤其是hiPSC技术,为突破这一治疗瓶颈带来了新的希望。
干细胞和诱导多能干细胞疗法在脊髓损伤治疗中的潜力
除了原发性损伤造成的神经组织不可逆破坏外,脊髓损伤还涉及炎症、轴突变性、脱髓鞘和胶质瘢痕形成等继发性过程。这些病理变化显著阻碍了神经回路的重建,使得自发性功能恢复极其有限。目前的标准治疗旨在通过康复治疗限制损伤进展并促进代偿性功能恢复。然而,目前尚无任何疗法能够再生或修复受损的神经组织本身。
在此背景下,基于干细胞的疗法已成为再生医学领域一种极具前景的方法。干细胞具有自我更新和多向分化潜能,有望在损伤部位进行细胞替代、重建神经回路、促进髓鞘再生、提供神经保护并调节炎症反应。
近年来,诱导多能干细胞(iPSC)技术的出现加速了这项研究,它提供了一种符合伦理且免疫学上安全的细胞来源,可以无限扩增。iPSC可由患者自身的体细胞生成,这为个性化医疗提供了重要优势。因此,干细胞疗法——特别是使用iPSC的疗法——作为脊髓损伤(SCI)的潜在基础治疗方法,已引起越来越多的关注,其基础研究和临床前研究正在全球范围内积极推进,以期最终应用于临床。
不同来源神经干/祖细胞的特性与临床应用
在众多干细胞类型中,神经干/祖细胞(NS/PCs)因其能分化为所有中枢神经系统谱系细胞并对局部微环境具有良好的响应性,而在脊髓损伤治疗中备受关注。根据来源不同,主要可分为人胎儿组织来源、人胚胎干细胞(hESC)来源以及人诱导多能干细胞(hiPSC)来源的NS/PCs,它们各具特色,临床转化程度也不尽相同。
01.人类胎儿来源的神经干细胞/祖细胞
人胎儿来源的神经干细胞/祖细胞(NS/PCs)在脊髓损伤治疗中显示出明确的治疗潜力。这些细胞源自发育中的人体中枢神经系统,具有内在的强大神经发生与分化能力,能够较好地适应宿主的损伤环境。
临床前动物实验证实,移植后可促进神经回路重建和运动功能恢复。更关键的是,以NSI-566细胞系为代表的首次人体临床试验(I/II期)初步验证了其安全性与可行性,患者耐受性良好,且长期随访报告了运动和感觉功能的持续改善以及电生理学证据,为这类细胞的治疗有效性提供了初步的临床数据支持。

然而,关于使用人类胎儿组织、供体依赖性和细胞供应不稳定的伦理问题仍然是临床应用中的重大限制,对广泛采用作为一种普遍的治疗策略构成了挑战。
02.人类胚胎干细胞衍生的少突胶质前体细胞
人胚胎干细胞来源的少突胶质祖细胞(hESC-OPCs)在治疗脊髓损伤方面展现出标准化的修复潜力与初步的临床前景。hESC具备无限自我更新和高效分化为特定神经谱系(如OPCs)的能力,这为生产均一、可规模化的细胞产品奠定了基础。临床前研究证实,在亚急性损伤模型中移植hESC-OPCs能有效促进髓鞘再生和运动功能恢复。
基于这些结果,一项使用hESC来源的OPCs(LCTOPC1;曾用名 GRNOPC1和AST-OPC1)治疗急性胸段SCI患者的首次人体试验证实了其安全性和可行性。一项为期10年的随访研究报告称,未出现肿瘤形成、病灶增大或神经功能恶化,支持hESC来源的OPC疗法在人体中的长期安全性。
基于这些发现,一项针对亚急性颈椎脊髓损伤(AIS-A,C4-C7)的I/IIa期临床试验评估了hESC衍生的少突胶质前体细胞(OPC)。
2022年在一项针对亚急性颈髓损伤患者少突星细胞祖细胞的1/2a期剂量递增的研究中,96%的受试者在一侧或双侧至少恢复了一个运动节段,32%的受试者恢复了两个或更多节段的运动功能,且未发生意外不良事件。然而,这种程度的改善可能部分反映了疾病的自然进展或自发性恢复,因此应谨慎解读其与细胞治疗的因果关系。

此外,一项后续临床试验已于2025年启动,目前正在进行中。该研究的结果将进一步阐明这种方法的安全性和治疗潜力。
综合来看,hESC-OPCs疗法是脊髓损伤再生治疗领域一个经过概念验证的重要选项。其未来的发展取决于正在进行的后续临床试验能否提供更确凿的有效性证据,同时也依赖于在技术和监管层面解决其固有的伦理与免疫原性挑战。在多种干细胞疗法竞相发展的格局中,hESC来源的细胞因其标准化生产的优势,将继续作为一个关键的技术路径被深入探索。
03.人诱导多能干细胞衍生的神经干细胞/祖细胞
hiPSC-NS/PCs具有与hESCs相当的多能性,且伦理问题较少。此外,由于它们可由患者自身的体细胞生成,因此在个体化医疗和降低免疫排斥风险方面具有显著优势。然而,基因组不稳定性和非靶向分化问题仍然令人担忧,需要密切监测。
目前,人们正在积极开发降低致瘤风险的策略,例如清除未分化细胞和对移植细胞进行严格的质量控制,基于hiPSC的脊髓损伤 (SCI) 治疗的临床应用也在稳步推进。
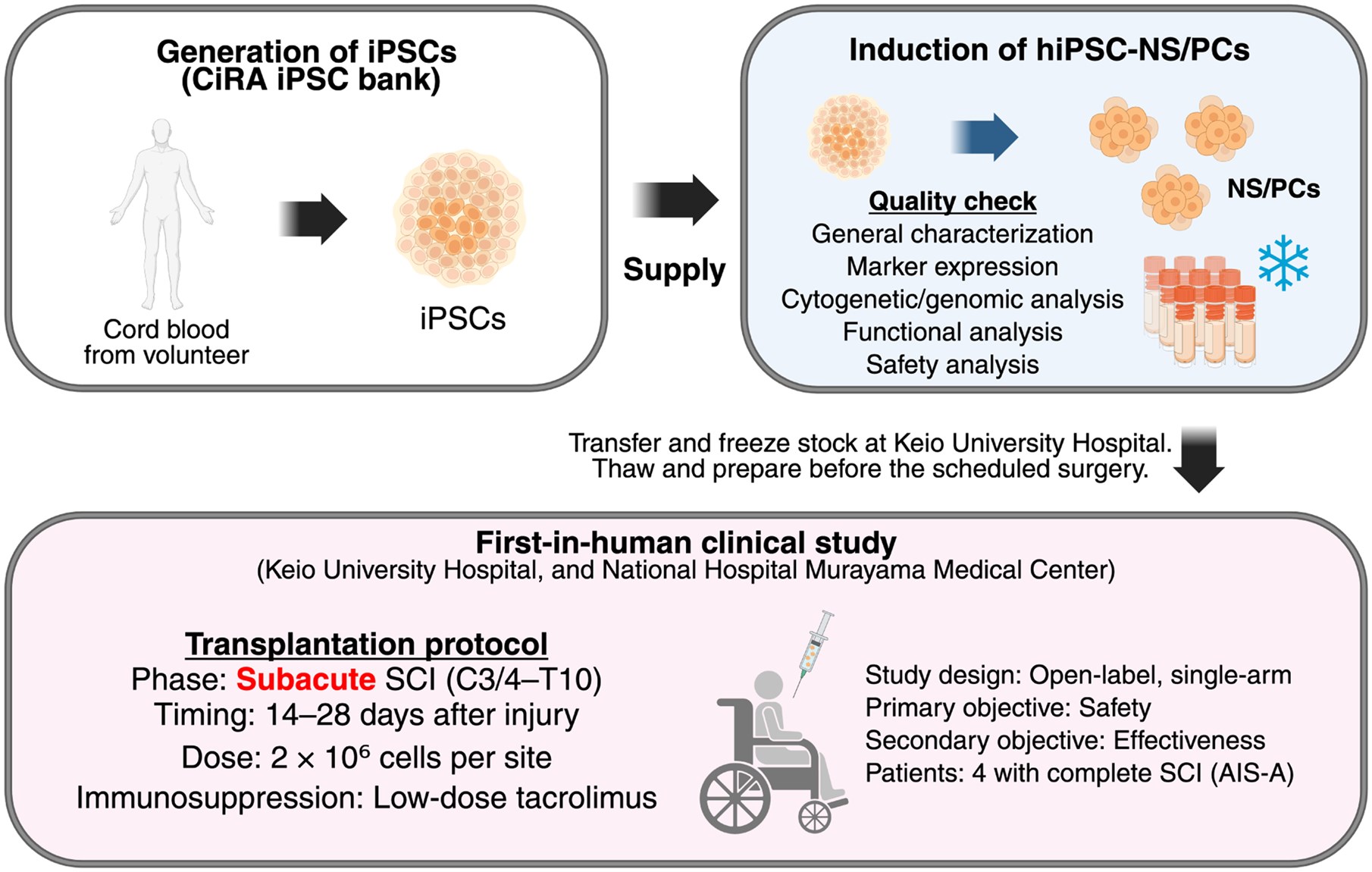
2021年,在日本,首个使用供体来源的hiPSC-NS/PCs治疗亚急性完全性SCI (AIS-A) 的临床研究已经开展;该研究总结于图1。在该试验中,4名C3/4至T10损伤的患者在受伤后28天内接受了细胞移植。首例移植手术于2021年进行,患者观察期于2024年结束。

截至撰写本文时,该研究的详细安全性和功能性结果尚未发表,因此未纳入本次综述。该试验是hiPSC-NS/PCs移植治疗脊髓损伤临床应用的重要里程碑。未来的研究方向包括将该方法推广至慢性脊髓损伤,并通过康复和药物干预等联合策略优化治疗效果。
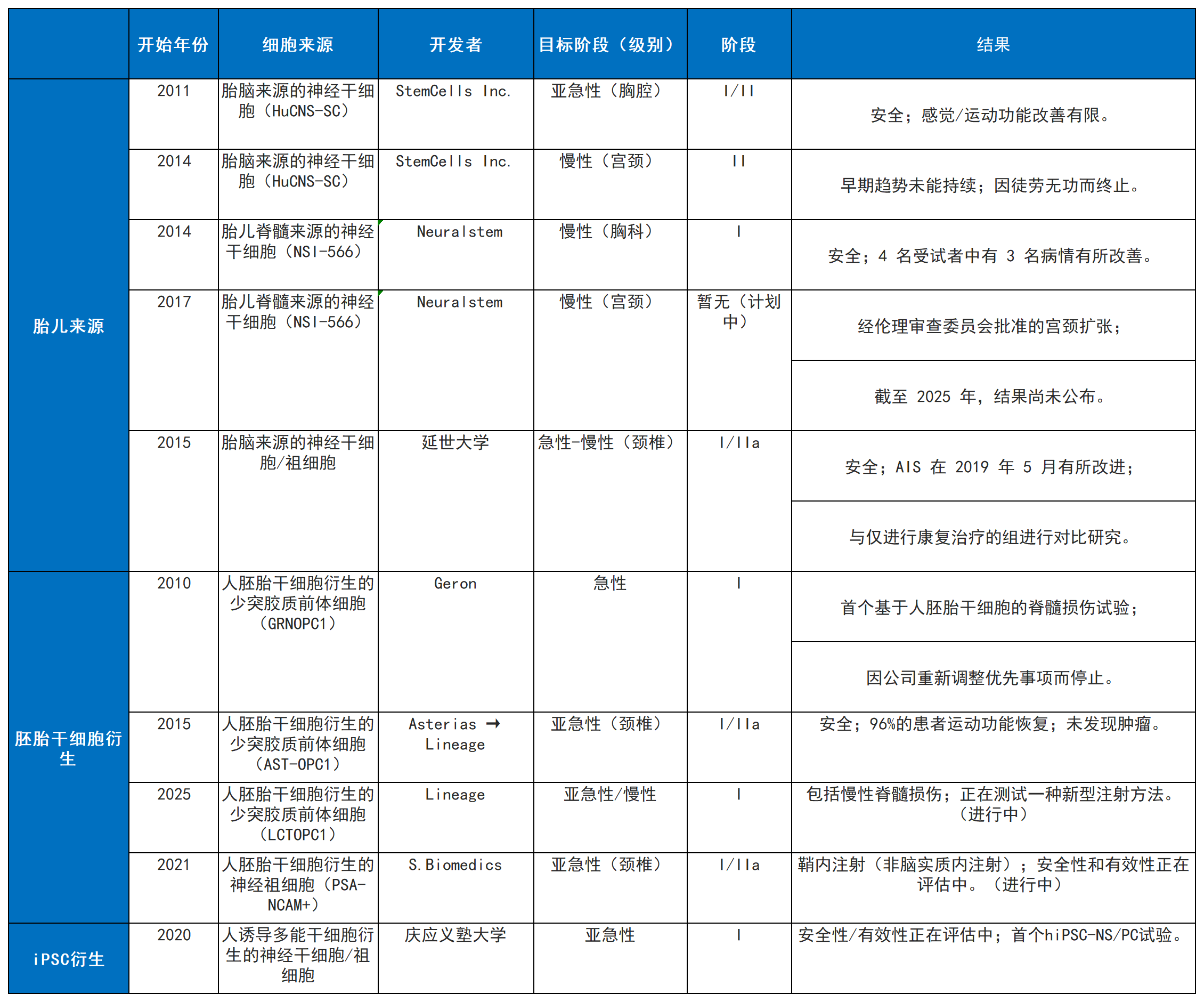
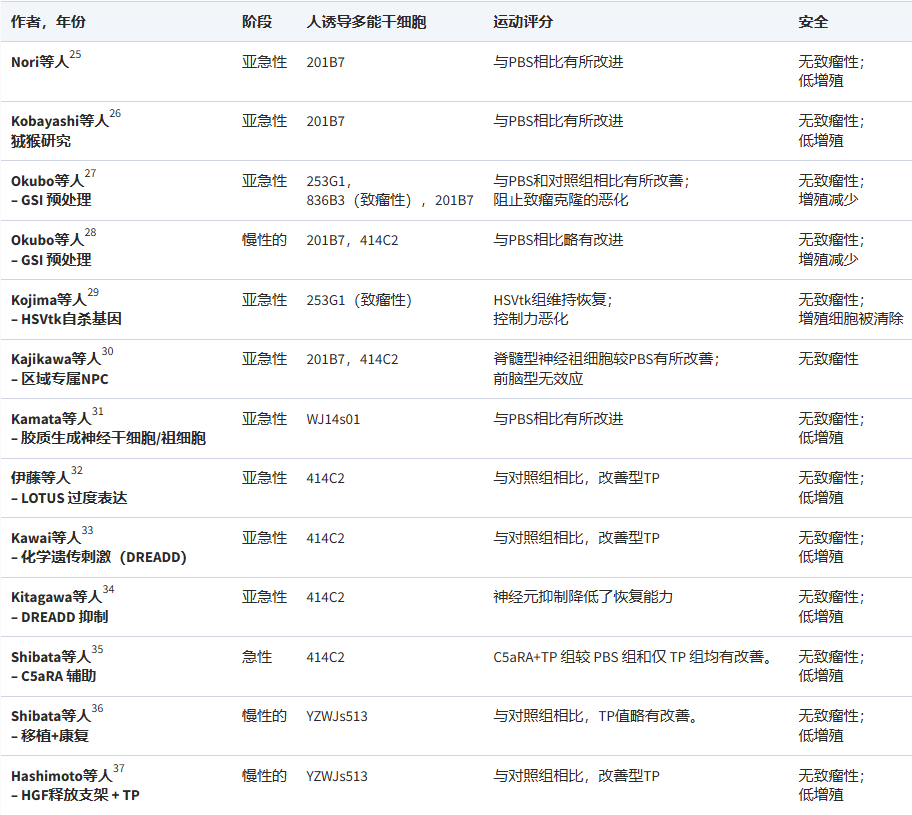
迄今为止报道的NS/PC和OPC移植治疗SCI的主要临床试验已按细胞来源分类(表1)。
hiPSC-NS/PCs移植治疗脊髓损伤的作用机制
利用hiPSC-NS/PCs进行移植疗法被认为是脊髓损伤(SCI)的一种很有前景的基础治疗方法。我们的研究表明,移植的hiPSC-NS/PCs能够存活,并可能有助于改善受损脊髓的功能和保护其组织,且在啮齿动物和非人灵长类动物SCI模型中均未观察到肿瘤形成(表2)。其治疗机制主要归因于以下三个方面。
hiPSC-NS/PCs移植治疗脊髓损伤的核心机制之一,是通过直接分化为功能性神经元并重建受损的神经回路来实现功能恢复。移植的细胞能够分化成各类神经元,并延伸长距离轴突,与宿主的上下行神经通路形成突触连接。
关键的功能性证据来自化学遗传学(如DREADD)和光遗传学操控研究,这些实验证实,人为抑制移植神经元的活动会导致已恢复的运动功能暂时丧失,而激活其活动则可增强突触形成、防止组织萎缩并进一步改善运动功能。这表明移植物来源的神经元已成功整合到宿主的中枢神经系统网络中,并主动驱动了行为学的改善。
其次,hiPSC-NS/PCs可通过分化为少突胶质细胞,促进脱髓鞘轴突的再髓鞘化,从而恢复神经信号传导速度与保真度。通过定向分化技术,可以制备出具有强烈胶质分化倾向的细胞系,使其在移植后分化为成熟少突胶质细胞的效率大幅提升。
这些新生的少突胶质细胞能够对宿主残留的轴突进行有效的重新包裹,这不仅有助于电生理传导的恢复,还能促进白质结构的保留,为运动功能恢复提供了重要的结构基础。临床前研究证实,这一过程能带来显著的功能改善,且未观察到致瘤性。
第三,移植的hiPSC-NS/PCs还通过强大的旁分泌作用,发挥神经保护和调节损伤微环境的功能。即使细胞尚未完全分化,它们也能持续分泌多种神经营养因子(如BDNF、GDNF、NT-3)和细胞因子。这些因子具有减轻继发性损伤、抑制有害炎症、减少胶质瘢痕过度形成以及支持宿主神经元与轴突存活的多重益处。RNA测序分析表明,这种分泌谱会根据损伤环境动态调整,显示出高度的环境响应性和治疗适应性,从而为神经修复创造一个更有利的局部环境。
综上所述,hiPSC-NS/PCs的治疗作用并非依赖于单一机制,而是上述“细胞替代”、“髓鞘再生”和“营养支持”三大核心机制的协同与整合。它们共同致力于从结构重建、功能连接和微环境调控多个层面修复受损的脊髓。未来研究的关键方向之一,正是通过优化细胞产品或联合治疗策略,来协同增强这些内源性修复机制,以期在更广泛的损伤类型和时期中取得最优疗效。
治疗时机与联合策略:聚焦脊髓损伤亚急性期
最大化hiPSC-NS/PCs疗效的关键因素之一是干预时机。急性期剧烈的炎症反应和慢性期稳固的抑制性瘢痕环境,均不利于移植细胞的存活与整合。而亚急性期(损伤后数天至数周)提供了一个相对平衡的“治疗窗口”,此时急性炎症开始消退,抑制性环境尚未完全固化,更利于移植物定植与功能发挥。这一理念已指导了如庆应义塾大学临床试验(jRCTa031190228)等转化研究的设计。
为进一步提升亚急性期治疗效果,联合策略日益受到重视。特别是,在2020年,一项近期临床前研究在急性期给予重组人HGF,随后在亚急性期移植hiPSC来源的神经干细胞/祖细胞(hiPSC-NS/PCs)。
与单独治疗相比,这种序贯治疗方案提高了移植细胞的存活率,促进了髓鞘再生和神经元再生,并带来了更好的运动功能恢复。这些发现表明,在这种情况下,HGF可能作为一种预处理策略,为亚急性期的后续移植创造更有利的微环境。

此外,对hiPSC-NS/PCs进行基因工程改造,使其过表达突触组织蛋白CPTX,从而主动促进移植神经元与宿主回路间功能性突触的形成。这些多模式联合疗法代表了未来优化疗效的重要趋势。
hiPSC-NS/PCs治疗的安全性控制
安全性与致瘤风险是hiPSC疗法临床转化的核心关切。控制系统性风险需要多管齐下:
首先,是源头控制与分子干预。优先选用经过全面验证的低风险细胞系,并利用表观遗传学特征(如抑癌基因甲基化状态)进行筛选。在移植前,可采用γ-分泌酶抑制剂(GSI)等对细胞进行短期预处理,通过抑制Notch信号通路来促进其向神经元分化、降低增殖潜能,从而从根源上减少致瘤风险。
其次,是实施全流程严格质控。建立涵盖细胞生产全链条的质量控制体系至关重要,包括利用流式细胞术确保未分化标志物(如OCT4)呈阴性、评估核型稳定性、以及验证其定向分化为神经元和胶质细胞的能力与比例。这套标准化流程是保证细胞产品一致性与安全性的操作基石。
通过综合运用上述策略,可层层规避风险。未来,建立长期的移植后监测体系,将是持续评估安全性、赢得临床信任的关键。
面向慢性脊髓损伤的挑战与临床转化瓶颈
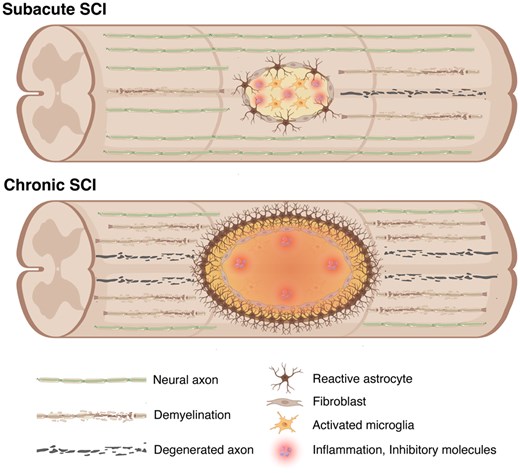
尽管利用hiPSC-NS/PCs移植的治疗策略在脊髓损伤的急性期和亚急性期取得了进展,但慢性脊髓损伤(约占所有脊髓损伤病例的95%)的有效治疗方法仍未得到充分开发,构成了一项重大的临床挑战。在亚急性期,损伤微环境相对宽松,有利于移植物的存活、整合和安全性;而在慢性期,瘢痕、空洞和脱髓鞘会形成抑制性环境,限制功能恢复,并可能影响移植物的生物学行为(图2)。
临床前研究表明,在亚急性期进行移植可显著提高功能恢复,而慢性期移植则受到抑制性微环境的限制。
为了应对这一临床需求,美国已启动了使用胎儿脑或脊髓来源的神经干细胞/祖细胞(NS/PCs)的临床试验。然而,胎儿组织来源的细胞存在伦理问题且供应有限。因此,人诱导多能干细胞来源的神经干细胞/祖细胞(hiPSC-NS/PCs)作为一种有前景的替代细胞来源脱颖而出,它不仅供应稳定,而且伦理限制也更少。
尽管如此,迄今为止的临床前研究尚未证实单独使用神经干细胞/祖细胞移植治疗脊髓损伤慢性期具有足够的疗效,这凸显了开发更有效、更可持续的治疗策略的必要性。
此外,临床转化还面临一系列实际挑战:
其一,模型与临床脱节。多数临床前研究采用胸椎损伤模型,但临床上颈椎损伤占主导,二者在神经解剖复杂性与功能评估上差异巨大,加之物种差异,削弱了临床前数据的预测价值。
其二,临床试验实施困难。包括患者功能评估受多种因素干扰、客观生物标志物缺乏、尤其是慢性期患者招募困难等。
其三,产业化壁垒高。细胞产品的标准化、规模化生产、严格的批次间质控、复杂的冷链物流以及高昂的研发成本,构成了疗法普及的最终障碍。目前,采用“现成”的HLA匹配异体hiPSC细胞库被视作比个体化自体疗法更可行的转化路径。
结论
综上所述,基于hiPSC-NS/PCs的细胞疗法为脊髓损伤的修复带来了革命性希望,其多机制协同的治疗作用在临床前研究中得到证实,并已初步步入临床验证阶段。当前的研究焦点正从亚急性期延伸至更具普遍性的慢性期损伤,同时积极探索联合治疗策略以优化疗效。
然而,要实现广泛临床应用,仍必须成功应对长期安全性验证、客观疗效评价体系建立、临床相关模型开发以及产业化供应链构建等多重挑战。持续而严谨的基础与临床研究,是支撑这一极具前景的再生疗法最终惠及广大患者的科学基石。
主要参考资料:[1]:Ryo Ogaki, Narihito Nagoshi, Hideyuki Okano, Masaya Nakamura, Human induced pluripotent stem cell-derived neural stem/progenitor cell therapy for spinal cord injury: preclinical advances and translational perspectives, Stem Cells Translational Medicine, Volume 15, Issue 1, January 2026, szaf073, https://doi.org/10.1093/stcltm/szaf073
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信