小儿脑性瘫痪(Cerebral Palsy,CP ),简称脑瘫。是一组由出生前或分娩过程中脑损伤引发的非进行性中枢神经系统障碍,主要表现为运动功能障碍、肌肉张力异常及协调能力受损,常伴随智力缺陷、癫痫、行为异常、视听语言障碍等多系统并发症,是全球儿童常见致残性疾病之一。
在全球范围内,脑瘫的发病率大约为每1000名儿童中有2到3人被确诊患有这种疾病。然而,不同地区的具体患病率有所差异,例如在中国,《中国实用儿科临床杂志》上一项针对12个省市的研究显示,中国脑瘫的发病率为2.48%,而在1-6岁的儿童中,患病率为2.46%。
该疾病不仅造成患儿终身护理需求(需24小时看护、长期康复训练及持续医疗支出),还可能因部分患儿在出生后数周死亡或寿命缩短至8-9岁而加剧家庭经济与心理压力。
脑瘫这种疾病的治疗是很复杂的,通常都是以对症康复为主,帮助患儿改善运动功能,比如说进行物理疗法、康复训练、药物治疗和手术治疗等,但是治疗的效果都不是很理想。但近年来,间充质干细胞移植治疗在神经系统疾病取得了令人鼓舞的进展,许多针对脑瘫的临床研究项目也取得了阶段性成果。
接下来本文结合近年临床研究及案例,系统阐述间充质干细胞治疗脑瘫核心机制以及临床疗效证据。

间充质干细胞治疗脑瘫疗效如何?249例患者告诉你答案
一、间充质干细胞:生物医学的 “多面手”
间充质干细胞(MSC)是一类具有自我更新和多向分化潜能的成体干细胞,广泛存在于骨髓、脂肪、脐带、胎盘等多种组织中 。正是由于其来源广泛、易于获取和体外扩增的特性,使其成为干细胞研究和临床应用的热点。在治疗脑瘫的过程中,间充质干细胞发挥着 “多重角色”。
- 从分化能力来看,间充质干细胞具备向神经细胞分化的潜力。当将其移植到受损的脑组织后,在特定的微环境诱导下,间充质干细胞能够分化为神经元、神经胶质细胞等,补充因损伤而缺失的神经细胞,修复受损的神经通路。
- 此外,间充质干细胞强大的免疫调节和抗炎能力也在脑瘫治疗中发挥关键作用。脑瘫患者脑部受损后,局部会发生炎症反应,炎症因子的持续释放会进一步加重神经细胞的损伤。而间充质干细胞能够通过分泌多种细胞因子,如转化生长因子 -β(TGF-β)、白细胞介素 – 10(IL-10)等,调节免疫细胞的功能,抑制炎症反应,减轻脑部组织的二次损伤,为神经修复创造有利的微环境。
- 同时,间充质干细胞还具有旁分泌作用。它可以分泌大量的生物活性分子,包括神经营养因子(如脑源性神经营养因子 BDNF、神经生长因子 NGF)、血管内皮生长因子(VEGF)等。这些因子能够促进内源性神经干细胞的增殖和分化,刺激神经细胞的存活、生长和突触形成,同时还能促进脑部血管的新生,改善脑部的血液循环,为受损神经组织提供充足的营养和氧气,加速神经功能的恢复。
二、临床疗效:多维度功能改善
2.1 脐带间充质干细胞治疗脑瘫患者
2020年,南方医科大学附属东莞市人民医院在《Stem Cells International》上发表了一篇关于《人类间充质干细胞移植治疗脑瘫的证据:随机对照试验的荟萃分析》的研究成果。

本分析纳入4项研究,共189名受试者,研究均采用脐带间充质干细胞(hUC-MSC)治疗。结果显示:
1.粗大运动功能(GMFM)评分:治疗组在3个月、6个月和12个月时均显著高于对照组,整体加权效应值达1.10,表明hMSC治疗对脑瘫患儿粗大运动功能有持续改善作用。(见图1)
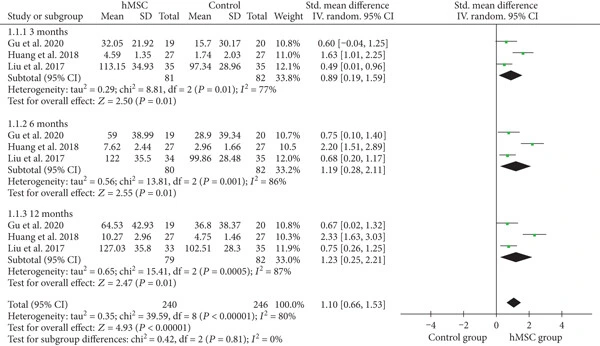
2.综合功能评估(CFA):2项RCT研究的CFA评分分析同样显示:治疗组3个月和6个月时CFA评分均显著优于对照组,加权效应值为1.30,提示hMSC治疗对整体功能恢复具有积极作用。(见图2)
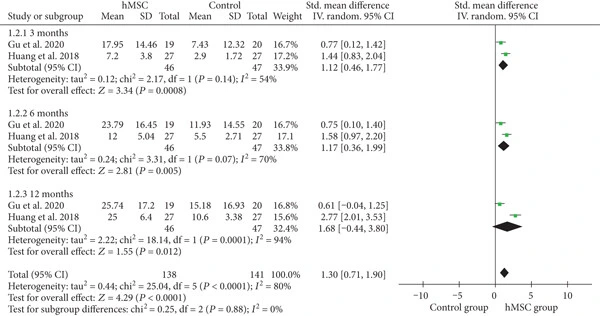
安全性评估:不良事件(AE)的meta分析表明治疗组与对照组无显著差异。
综上所述,脐带间充质干细胞疗法在改善脑瘫患儿运动功能(GMFM/CFA评分)方面效果显著且安全性良好,为临床应用提供了可靠依据。
2.2 脐带间充质干细胞治疗脑瘫儿童安全性和有效性的进一步证据
同年,根据《干细胞研究与治疗》报道,我国研究团队开展的研究,通过随机、双盲、安慰剂对照试验为人脐带间充质干细胞治疗脑瘫的安全性和有效性进一步提供证据。

本次研究工纳入了40例脑瘫患者,其中1名患者在未接受任何治疗的情况下撤回知情同意并失访。因此,39名患者完成了所有研究评估。最后一名患者的最后一次访视于2018年2月完成。研究发现:
ADL(日常生活能力)评分和CFA(精细动作功能)评分在3个月随访时hUC-MSC组较对照组改善更显著。(见图3)
断层扫描/计算机断层扫描评估脑代谢活动:发现相比于对照组,间充质干细胞治疗组中五分之三的患者在3个月中观察到葡萄糖标准摄取值显著增加,较基线提升超过50%。这表明脑糖代谢的改善可能在间充质干细胞移植诱导的功能改善中起到重要作用。

综上所述,hUC-MSC治疗可显著改善脑瘫患者的功能障碍,并揭示其作用机制可能与脑代谢活性的增强相关,为干细胞治疗脑瘫提供了新的治疗方向和循证依据。
2.3 脂肪间充质干细胞移植治疗五例脑瘫儿童疗效观察
2022年3月1日,赣南干细胞临床研究中心牵头在国际期刊《美国转化医学杂志》上发表了一篇关于《脂肪间充质干细胞移植治疗脑瘫五例疗效观察:病例报告》的研究成果。

共5名脑瘫患者在常规体格检查后,每14天静脉输注一次脂肪间充质干细胞(ADMSC),3次输注为1个疗程。同时进行常规康复训练,并随访6个月至1年。
治疗后,儿童粗大运动功能量表(GMFM-88)、脑瘫儿童综合功能评估量表和精细运动功能量表(FMFM)的评分均得到改善。1名既往有结核性胸膜炎病史的受试者在治疗期间复发,但经过适当的医疗干预后症状消失。其余4名受试者的常规血液参数均正常。(见图4、5)


综上所述,研究表明静脉注射ADMSCs后,脑瘫儿童的运动功能和言语功能得到改善,尤其是重度脑瘫儿童。没有观察到明显的安全性问题。
2.4 骨髓间充质干细胞多次注射治疗脑瘫患者的疗效
2025年,伊朗德黑兰科研人员在国际期刊《神经修复学杂志》上发表了一篇关于《反复鞘内注射自体骨髓间充质干细胞治疗痉挛性脑瘫:单组安全性和初步疗效临床试验》的临床研究结果。

本研究对16名2至12岁痉挛型脑性瘫痪(CP)患儿进行了一项前瞻性、单组、开放标签的I期临床试验。患者接受4次鞘内MSC注射,每次间隔一个月。研究结果发现:
1.运动功能改善(GMFCS分级):
12个月随访中,50%(8/16)患者GMFCS分级提升。
具体而言,GMFCS II 级患者比例从6.2%上升至18.75%,III 级患者比例从12.5%上升至18.75%。GMFCS V级患者比例从62.5%下降至43.75%。总体比例变化具有统计学意义,表明参与者的运动功能得到了显著改善。所有IV级和III级患者以及30%的V级患者的GMFCS分级均有所改善。(见图6)

2.粗大运动功能(GMFM-88评分):
12个月后总分显著提高,各领域均改善。平均从47.01±21.45提高至54.69±22.62。
具体来说,躺着从70.47提升到81.37;坐着从56.77提升到67.92;爬行/站立/行走,分别提升7.6%、6.7%、3.8%。这些结果表明,干预后运动能力有统计学上显著的提高。(见图7)

3.平衡与痉挛控制(BBS&MAS)
治疗后12个月,BBS评分从平均值6.75提高至9.88,表明参与者的平衡能力和稳定性得到了增强。通过MAS评估,肌肉痉挛明显减少,平均评分从2.25降至1.62,表明肌肉紧张度降低,运动控制改善。(见图8)

4.功能独立性(FIM/FAM)
使用FIM/FAM评估功能独立性。运动分量表得分从38.63提高至47.44,提示运动独立性有所提高。认知分量表得分也显著提高,从57.06提高至70.88,提示干细胞治疗后认知功能有所改善。(见图8)
综上所述,这些结果表明,MSC疗法可改善功能结局和生活质量,并且反复鞘内注射自体MSC是安全的,能够显著改善痉挛型脑性瘫痪患儿的运动功能、平衡能力和痉挛状态。
三、间充质干细胞治疗脑瘫疗效总结
综上所述,间充质干细胞(MSCs)治疗脑瘫在运动功能、平衡能力、痉挛控制及认知功能等方面均展现出显著疗效,且安全性良好。
脐带间充质干细胞(hUC-MSC)的荟萃分析显示,治疗组在粗大运动功能(GMFM)和综合功能评估(CFA)评分上持续优于对照组,且脑代谢活性增强;
脂肪间充质干细胞(ADMSC)治疗则显著改善重度脑瘫儿童的运动与言语功能,未见明显不良反应;
伊朗团队的I期临床试验进一步证实,反复鞘内注射自体骨髓MSC可显著提升痉挛型脑瘫患儿的GMFCS分级、平衡能力(BBS评分)及肌肉痉挛控制(MAS评分),同时认知功能独立性(FIM/FAM)亦显著提高。
这些研究共同表明,不同来源的MSCs均能有效促进脑瘫患者的功能恢复,为临床治疗提供了多样化的选择与循证支持。
四、挑战与未来方向
个体化治疗方案:需根据脑瘫类型(如痉挛型、共济失调型)和损伤部位选择最佳细胞来源(脐带、胎盘)及输注途径(鞘内、静脉)。
长期安全性评估:需建立10年以上随访机制,监测迟发性风险(如免疫耐受性变化)。
技术优化:
- 基因编辑:增强MSCs的归巢能力或神经营养因子分泌。
- 外泌体疗法:MSCs分泌的外泌体携带修复因子,可减少细胞移植风险
结语
间充质干细胞治疗脑瘫展现出显著的临床潜力,通过神经修复、免疫调节和血管新生等多机制改善运动功能与生活质量。现有数据支持其安全性与有效性,但需进一步通过大规模随机对照试验验证长期疗效。未来,随着工程化外泌体与基因编辑技术的突破,MSCs有望成为脑瘫精准治疗的核心手段,为全球数百万患儿带来康复希望。
相关阅读:脐带、脂肪、骨髓和胎盘:哪种来源的间充质干细胞更适合治疗脑瘫?
参考资料:
Xie, Baocheng, Chen, Minyi, Hu, Runkai, Han, Weichao, Ding, Shaobo, Therapeutic Evidence of Human Mesenchymal Stem Cell Transplantation for Cerebral Palsy: A Meta-Analysis of Randomized Controlled Trials, Stem Cells International, 2020, 5701920, 10 pages, 2020. https://doi.org/10.1155/2020/5701920
Gu, J., Huang, L., Zhang, C. et al. Therapeutic evidence of umbilical cord-derived mesenchymal stem cell transplantation for cerebral palsy: a randomized, controlled trial. Stem Cell Res Ther 11, 43 (2020). https://doi.org/10.1186/s13287-019-1545-x
Hu, K., Wang, R. ., Xiao, B. ., Xiao, B. ., Gu, Y. ., Liu, F. ., … Wen, Y. . (2022). Effect of adipose-derived mesenchymal stem cell transplantation in five patients with cerebral palsy: A case report. American Journal of Translational Medicine, 6(1), 33–40. Retrieved from https://journals.publicknowledgeproject.org/default3/index.php/ajtm/article/view/2253
Mohammadhosein Akhlaghpasand, Maede Hosseinpoor, Bardia Hajikarimloo, Atieh Hajarizadeh, Maryam Golmohammadi, Roozbeh Tavanaei, Ida Mohammadi, Nastaran Ansari Noghlebari, Niloofar MohammadEbrahim, Alireza Zali, Saeed Oraee-Yazdani,Repeated Intrathecal Injections of Autologous Bone Marrow-Derived Mesenchymal Stem Cells for Spastic Cerebral Palsy: Single-Arm Safety and Preliminary Efficacy Clinical Trial,Journal of Neurorestoratology,2025,100207,ISSN 2324-2426,https://doi.org/10.1016/j.jnrt.2025.100207.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信