对于1型糖尿病患者来说,依赖胰岛素注射几乎是日常生活的一部分,但这种局面或许正在被改写。近几年,全球有数十家研究机构和企业尝试借助干细胞技术“重启”胰岛β细胞的功能。
2025年,《Cell》《Nature Biotechnology》《New England Journal of Medicine》等国际权威期刊先后发表了相关研究,结果都指向一个趋势:干细胞疗法在1型糖尿病的治疗中展现出了前所未有的潜力。
像Vertex制药公司VX-880疗法的最新2期试验显示,83%的重症患者在单次输注后完全停用外源性胰岛素;中国团队的自体来源化学重编程胰岛移植患者实现部分患者在移植后3个月内停用胰岛素。
这些数字背后是一个正在形成的共识:干细胞治疗正从实验室走向临床。接下来,本文将系统梳理2025年干细胞疗法的最新临床证据与关键障碍,深入解析这项“治愈希望” 技术其距离真正走进常规临床应用,还有多远。

2025干细胞治疗1型糖尿病最新进展:距离临床还有多远?
1型糖尿病困境与治疗局限
1型糖尿病是一种自身免疫性疾病,免疫系统错误攻击并破坏胰岛β细胞,导致胰岛素绝对缺乏。患者必须终身依赖外源性胰岛素治疗,日常管理包括每日4-7次指尖血糖检测和精确的胰岛素剂量调整。即使采用强化胰岛素治疗,患者仍面临血糖波动和严重低血糖风险,以及远期微血管和大血管并发症威胁。
现有治疗手段无法根治疾病,只能控制症状,患者期待一种能够解决根本问题的治疗方法。这些局限催生了干细胞疗法的发展,利用干细胞的自我更新和分化潜能,创造替代性胰岛素生成细胞,从根本上恢复患者的生理性血糖调节能力。
干细胞治疗1型糖尿病的三大作用机制
干细胞治疗1型糖尿病主要通过以下三大机制发挥作用:
1.细胞替代是最直接的策略:利用干细胞分化出的胰岛β细胞,来取代已经被破坏的细胞,从而恢复体内的胰岛素分泌功能。
2.免疫调节作用针对1型糖尿病的自身免疫病因:像间充质干细胞这类细胞,能够在一定程度上“安抚”异常活跃的免疫系统,保护仍存活的胰岛β细胞不再遭到持续破坏。
3.旁分泌效应也不可忽视:干细胞还能释放多种生物活性分子,帮助改善胰岛周围的微环境。它们既能促进血管新生,增强局部供血,也能减轻炎症反应,从而提高移植细胞的存活率和功能稳定性。
2025年干细胞治疗1型糖尿病患者最新临床进展
1.国内首个“干细胞再生胰岛”疗法获批,多名1型糖尿病患者移植后3个月内停用胰岛素
2024年5月7日,上海长征医院殷浩教授团队联合中国科学院程新教授团队在《细胞·发现》(Cell Discovery)发表重磅研究,通过自体干细胞再生胰岛移植,成功治愈一名患病25年的Ⅱ型糖尿病患者。[1]
时隔一年,2025年4月18日,殷浩教授团队再传捷报:其与中科院分子细胞科学卓越创新中心合作开发的“异体人再生胰岛注射液(E-islet 01)”,正式获得国家药品监督管理局(NMPA)临床试验默示许可。[2]
这是全球第二个、中国首个获批临床试验的通用型再生胰岛疗法,标志着我国在糖尿病再生医学领域实现了从“跟跑”到“领跑”的跨越。并且殷浩与合作团队先后利用自体和异体再生胰岛移植,成功治愈多例1型糖尿病患者!

殷浩教授介绍,E-islet 01是利用细胞重编程和定向分化等前沿技术将健康供体来源的血液细胞转化为内胚层干细胞,再以内胚层干细胞为原材料定向制备的再生胰岛,其具备与健康胰岛一致的结构和功能,能够通过实时感知血糖变化精准分泌包括胰岛素、胰高血糖素、生长抑素等一系列内分泌激素,从而维持血糖稳态。
长征医院的临床研究(IIT)表明,E-islet 01经微创操作输注到患者肝门静脉内,可实现胰岛功能衰竭糖尿病(Ⅰ型和严重Ⅱ型)患者的治愈。
2.人胚干细胞衍生胰岛细胞疗法突破:83%重症糖尿病患者完全停用胰岛素
6月20日,福泰制药(Vertex)在美国糖尿病协会(ADA)科学年会上震撼发布FORWARD-101临床试验的1/2/3期的最新研究结果,并更新了1/2期试验的最新临床数据,相关结果发表在国际期刊《新英格兰医学杂志》上。[3]
该研究聚焦于zimislecel(原名VX-880),一种基于干细胞的完全分化胰岛细胞疗法,旨在治疗伴有低血糖意识障碍和严重低血糖事件(SHE)的1型糖尿病(T1D)患者。

在FORWARD-101最新临床试验中,12名接受单次全剂量Zimislecel输注的患者接受了至少1年的随访,结果显示:
所有12名参与者均表现出内源性胰岛素分泌(通过C肽评估)的恢复,严重低血糖事件的消失,以及血糖控制达标(HbA1c<7%,TIR>70%)。
该疗法显著减少了所有患者的外源胰岛素的使用量,平均每位患者都减少了92%,并且在83%(10例)患者中完全消除了外源胰岛素的使用需求。
与VX-880使用相关的不良事件与典型的胰岛输注和现有免疫抑制药物方案一致,未在任何受试者中观察到额外的不良症状。
试验结果表明,Zimislecel在1型糖尿病治疗中展现出革命性潜力:不仅在1年内显著减少甚至停用外源胰岛素(平均减少92%),同时血糖稳定、低血糖风险消失。10人完全摆脱胰岛素注射,安全性良好,不良反应与常规治疗相当。这一突破为糖尿病患者提供了“摆脱每日注射”的新希望,未来或成为治疗的重要选择。
详情请浏览:突破性干细胞疗法Zimislecel:83%重症糖尿病患者停用胰岛素超一年
3.京都大学完成日本首例iPS细胞移植治疗:初期安全性良好
2025年4月14日,日本京都大学医学部附属医院发布了一则重磅消息– iPS细胞疗法在糖尿病治疗领域取得突破性进展,有望减轻糖尿病患者每日注射胰岛素的负担。
该院宣布成功完成日本首例干细胞再生胰岛组织移植手术,首位接受治疗的1型糖尿病患者术后观察显示良好临床反应,近期将进行第二例移植,这标志着人类在攻克糖尿病征程中迈出关键一步。

这项突破性研究植根于2007年山中伸弥教授开创的iPS细胞技术,该技术荣获2012年诺贝尔生理学或医学奖。
这项成果源自2007年由山中伸弥教授开创的iPS细胞技术,该技术曾在2012年获得诺贝尔生理学或医学奖。研究团队利用健康供者的诱导多能干细胞分化出具备胰岛素分泌功能的“胰岛细胞”,再将其制成片状,移植到患者体内,以期重建其胰岛功能。
京都大学大学院医学研究科的矢部大介教授矢部大介教授在新闻发布会上透露:“首例患者术后已顺利度过关键观察期,未发生重大问题,安全性评估最多将持续5年。若后续进展顺利,2030年前有望实现该技术的临床应用。”
相关阅读:2025年干细胞治疗1型糖尿病最新临床进展,治愈已触手可及(截至8月)
关键障碍:临床转化面临的挑战
尽管临床前景光明,但干细胞疗法要成为常规临床选择还需跨越多重障碍。
1.免疫排斥问题是首要挑战:无论是异体还是自体来源,移植细胞都面临免疫攻击。异体细胞需终身免疫抑制剂,增加感染和肿瘤风险;自体细胞虽避免了异体排斥,但仍面临自身免疫再度攻击。这些问题都是要解决的。
2.量产和质量控制是产业化难点:GMP级细胞生产要求高,成本昂贵,当前治疗成本是胰岛素终身费用的数倍。
3.伦理和监管框架仍需完善:特别是对于胚胎干细胞来源的产品,以及基因编辑技术的应用。
干细胞疗法的安全性:不良事件与风险管控
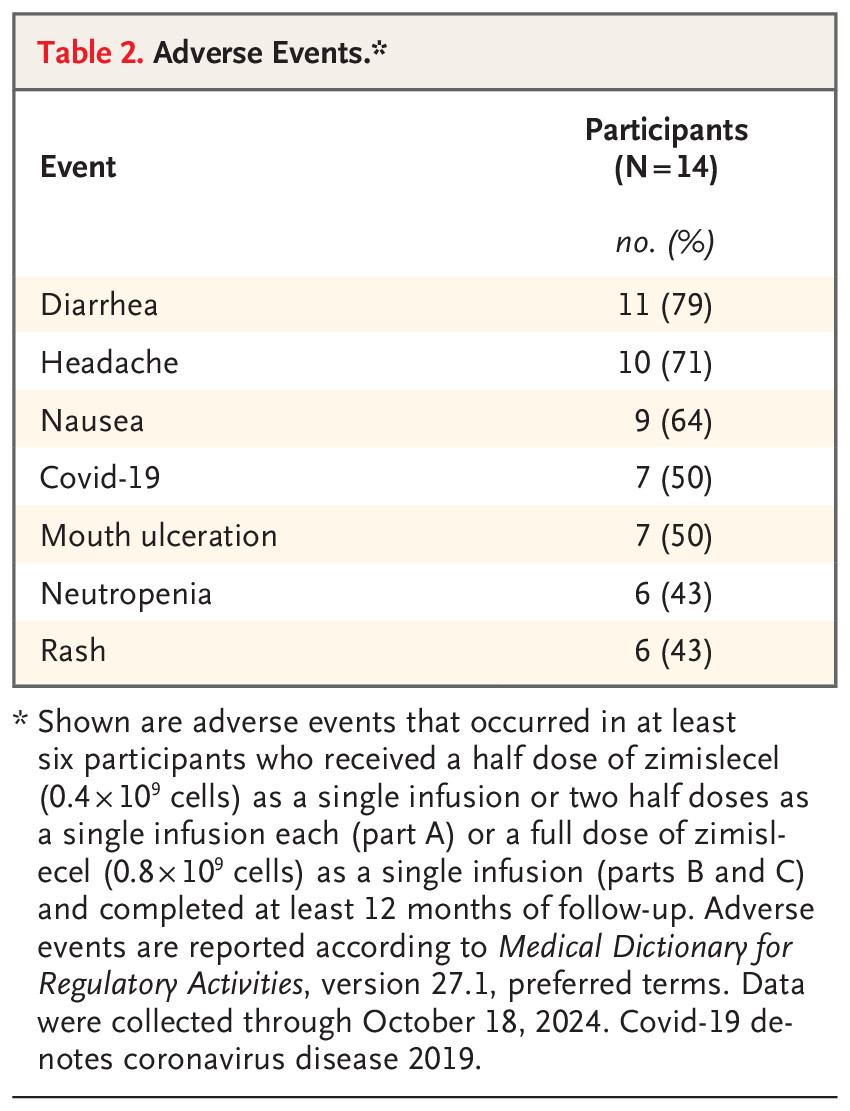
整体来看,干细胞治疗1型糖尿病的安全性表现令人放心。以福泰制药(Vertex)开展的FORWARD-101临床试验为例:在完成至少12个月随访的14名参与者中,大部分不良事件都是轻度或中度,未出现严重不良反应。[3]
最常见的不良事件包括腹泻、头痛、恶心、口腔溃疡、中性粒细胞减少以及皮疹。研究团队评估认为,这些不良反应普遍较轻,通常在干细胞输注后约6天内出现,并在30天内自行缓解。(见下图)
未来展望:临床落地时间表预测
基于当前进展,干细胞治疗1型糖尿病的时间表已经初步清晰。2025年福泰制药的全球首款针对1型糖尿病的干细胞疗法3期临床即将完成,预计明年申报上市。如果获批,该药物将有望使欧美等地区因现有治疗手段受限而反复出现严重低血糖事件的患者受益
未来1-2年内,我们可能会看到有条件批准的干细胞产品上市,适用于最需要的患者群体。
3-5年内,随着技术优化和免疫方案改进,适应症可能会扩大,更多患者能够从中受益。
5-10年后,基因编辑技术可能推动“通用型”干细胞产品的出现,进一步降低免疫排斥风险和治疗成本。
意义:患者角度的风险-收益评估
从患者视角看,干细胞治疗带来了前所未有的希望,但也需理性看待。
治疗效益:重塑糖尿病管理的未来
对于1型糖尿病(T1D)患者而言,干细胞治疗如同一束曙光,有望彻底改变疾病管理模式。其核心优势在于功能性治愈的可能性:
- 胰岛素独立:通过干细胞分化为功能性β细胞,患者可能摆脱每日胰岛素注射的繁琐,实现自主调节血糖的能力。
- 血糖稳定控制:干细胞疗法可模拟生理性的胰岛素分泌模式,显著降低血糖波动,减少夜间低血糖事件的发生率。
- 并发症预防:长期稳定的血糖控制能延缓或逆转糖尿病相关并发症(如视网膜病变、肾病),提升患者生存质量。
- 免疫耐受重建:部分疗法通过调节自身免疫系统,可能减少对胰岛β细胞的持续攻击,为长期疗效提供保障。
风险与挑战:理性看待科学边界
尽管前景广阔,但患者仍需清醒认识当前的技术局限性:
- 个体差异显著:疗效可能因患者年龄、病程、免疫状态等因素而异,无法保证“普适性”。
- 免疫排斥风险:异体干细胞移植需依赖免疫抑制剂,可能增加感染或肿瘤风险;自体干细胞疗法成本高昂且技术复杂。
- 经济负担沉重:目前单次治疗费用可达数万元,远超普通家庭承受范围,及需医保或政策支持。
患者行动建议:把握机遇,规避风险
参与临床试验:优先选择经正规审批的临床试验,在专业团队指导下体验前沿疗法。
关注监管动态:密切跟踪FDA或NMPA的审批进展,等待成熟疗法上市后再评估可行性。
权衡风险-收益:与医生充分沟通,结合自身病情(如严重低血糖史、并发症程度)制定个性化干细胞决策。
警惕非正规宣传:拒绝“包治百病”的干细胞噱头,谨防非法机构以“祖细胞疗法”为名行诈骗之实。
结语:希望与挑战并存的 “黎明前”
干细胞治疗1型糖尿病已经取得了从“0到1”的革命性突破,首次在临床上实现了让1型糖尿病患者“脱离胰岛素”的梦想。当前的研究正从“证明概念”转向“优化方案”,聚焦于提升安全性、耐久性和可及性。
虽然前路仍有挑战,但毋庸置疑,干细胞技术正引领我们走向一个彻底改写糖尿病治疗史的新时代,为数百万患者点燃了治愈的曙光。
相关阅读:
新研究有望终结胰岛素注射!《糖尿病杂志》:干细胞治疗1型糖尿病迎来转机
参考资料:
[1]Wu, J., Li, T., Guo, M. et al. Treating a type 2 diabetic patient with impaired pancreatic islet function by personalized endoderm stem cell-derived islet tissue. Cell Discov 10, 45 (2024). https://doi.org/10.1038/s41421-024-00662-3
[2]https://www.thepaper.cn/newsDetail_forward_30703516
[3]https://www.nejm.org/doi/full/10.1056/NEJMoa2506549
[4]https://www.nikkei.com/article/DGXZQOUF142ZG0U5A410C2000000/
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信