2025年已接近尾声。回顾这一年,中国在干细胞治疗中风(脑卒中)领域取得了多项重要进展。无论是基础研究、临床试验数据,还是政策与监管环境,都在持续推进,干细胞疗法正从实验阶段加速向实际临床应用迈进。
过去,人们普遍认为中风后脑组织损伤难以修复,但最新研究显示,干细胞治疗在促进神经功能恢复、改善运动能力、减少后遗症等方面表现出积极效果,为患者带来了新的希望。
本文将梳理2025年我国干细胞治疗中风的基础研究成果、临床研究进展和政策动向三个方面,为医疗专业人士、中风患者及家属提供一份清晰、可信的年度进展总结。

2025中国干细胞治疗中风走到哪一步了?从基础研究到临床政策的全面梳理
一、基础研究进展:机制更清晰、技术路径更丰富
2025年的基础研究,正从“证明干细胞有效”迈向“阐明为何及如何更有效”的深水区。核心突破集中在两大方向:一是开发出更安全、高效的“无细胞”治疗新策略;二是实现了对移植干细胞在体内的“可视化”全程追踪,为临床转化提供了关键工具。
1.1 “无细胞治疗”策略的崛起:从替代到精准调控
传统干细胞移植面临存活率低、潜在风险等挑战。今年,研究者们另辟蹊径,提取干细胞中的核心功能成分(如线粒体、外泌体),制成“纳米级生物制剂”,实现了更精准的靶向修复。
修复能量工厂,重启血管新生:重庆医科大学与陆军军医大学联合团队创新性地构建了RGD肽修饰的间充质干细胞源线粒体囊泡(RGD-mitoEVMs)。该囊泡能像“特快专递”一样,将健康的线粒体精准递送至中风后受损的脑血管内皮细胞内部。[1]
研究首次阐明,这一过程能重编程细胞内的谷胱甘肽代谢,激活关键信号通路,从而将病变区域的血管尖端细胞转化率提升2.1倍,新生血管密度增加68%,最终显著减小脑损伤并改善功能。

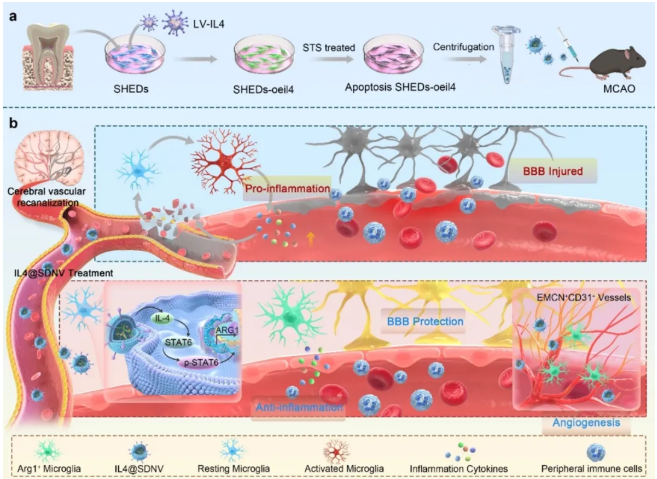
重编程免疫细胞,实现神经血管双保护:空军军医大学高昌俊教授团队研发了富含IL-4的人牙髓干细胞纳米囊泡(IL4@SDNV)。[2]
该囊泡能靶向渗透血脑屏障,被大脑固有的免疫细胞——小胶质细胞高效吞噬。通过将其从“破坏性”极化为“修复性”表型,同时解决了炎症控制和微血管再生两大难题,使脑血流灌注量提升超过144%。
尤为重要的是,该方法不依赖于传统的溶栓取栓时间窗,为错过黄金治疗期的患者提供了新希望。
1.2 可视化追踪:打开干细胞体内修复真相
干细胞移植后去哪儿了?存活了多久?变成了什么?这些曾是制约临床转化的关键疑问。2025年,我国科学家利用前沿分子影像技术,首次清晰回答了这些问题。
浙江大学张宏团队与复旦大学田梅团队合作,利用CRISPR/Cas9基因编辑技术,构建了携带三重融合报告基因的人神经前体细胞(hNPCs)。结合多模态影像技术,他们实现了对移植细胞长达48周的在体、动态、可视化监测。[3]
监测结果显示,移植的神经前体细胞不仅在中风区域长期存活,更在约11周后,超过80%分化为成熟的皮层神经元,并与宿主大脑建立了大量具有功能的兴奋性与抑制性突触连接,完成了全脑尺度上的神经环路重建。这直接证明了干细胞疗法通过“神经元替代”实现根本性修复的可行性。

二、临床研究进展:多点突破,证据日益坚实
在扎实的基础研究支撑下,2025年我国干细胞治疗中风的临床转化也迈出了历史性步伐,从慢性期康复延伸至最具挑战的急性期治疗,研究证据链日趋完整。
2.1 填补急性期治疗空白:国家首个备案临床研究启动
2025年9月,大连医科大学附属第一医院的刘晶教授团队开展的“脐带间充质干细胞治疗急性缺血性脑卒中的临床研究”项目成为国家卫生健康委与国家药监局联合备案体系下首个干细胞治疗急性缺血性脑卒中的临床研究。[4]
该研究选取脐带间充质干细胞(UC-MSC)作为治疗对象,利用其低免疫原性和良好的神经保护特性,评估其对急性缺血性脑卒中患者的安全性及疗效。
项目的开展不仅推动了国内干细胞治疗中风的研究体系建设,也为未来更大规模的多中心临床试验奠定了基础。同时,通过该研究,科研团队积累了细胞制备、剂量选择和注射途径等关键技术参数,为干细胞疗法的标准化、可重复性和临床推广提供了科学依据。

2.2 干细胞新药获国际权威认可:首款iPSC衍生神经前体细胞获FDA快速通道资格
2025年12月2日,我国霍德生物宣布,公司自主研发的国际首款人前脑神经前体细胞注射液(hNPC01)获得了美国食品药品监督管理局(FDA)授予的快速通道资格(Fast Track Designation, FTD),用于治疗缺血性脑卒中导致的长期运动功能障碍。[5]
这一认定意味着该疗法在神经修复领域的临床潜力与创新价值,首次得到国际权威监管机构的高度认可,并将加速其临床研发与上市进程。
FDA快速通道资格主要授予具有创新性、能够解决重大未满足医疗需求的治疗手段。获得该资格后,hNPC01将在临床设计指导、滚动提交上市申请、优先审评以及同情用药(Expanded Access)等方面享受政策加速,有望更快惠及患者。
hNPC01基于iPSC定向分化技术开发,用于促进神经细胞替代和神经环路重建。临床I期试验结果显示:
- 23例缺血性脑卒中偏瘫长期后遗症患者均表现出良好安全性;
- 12个月随访运动功能显著改善,平均上肢FMA-UE提升可达11.3–13.7分;
- 92%的患者达到临床显著改善标准,并观察到下肢与语言能力提升;
- 近70%患者残疾等级(mRS)改善,且改善趋势持续至18个月。
与目前全球唯一获批的VNS神经调控治疗相比,hNPC01在运动功能改善幅度与综合获益方面显示更明显优势。
霍德生物表示,将借由快速通道优势推进国际多中心确证临床试验,并计划拓展至脑出血、脑外伤、脑瘫等更多神经损伤适应症,为长期缺乏有效修复手段的群体提供新选择。
2.3 关键临床证据发布:多分期干预价值被系统验证
2025年10月8日,大连医科大学附属第一医院干细胞临床研究中心牵头在国际期刊《Journal of Translational Medicine》上发表了一篇名为《干细胞疗法治疗缺血性卒中的临床试验和先进磁共振成像技术:现状与展望》的研究成果。[6]
研究共发现68项注册研究,其中26项已完成并发表。此外,通过PubMed纳入18篇已发表的英文临床试验文章,最终汇总44项已发表的干细胞治疗IS的临床研究。数据涵盖研究设计、细胞类型、剂量、给药途径、给药时间及功能性结局。

研究结果表明:
1. 急性期(发病后一周内)
常用细胞类型:以骨髓单核细胞(BMMNCs) 为主,其他包括多能成体祖细胞(MAPCs)、脐带血干细胞等。
临床结果:干细胞治疗在急性期总体安全,并显示出一定的功能改善趋势。但疗效存在异质性,部分高质量研究表明,治疗时机和患者特征可能影响效果。
- 例如,一项早期研究(NCT00761982)显示,接受BMMNCs治疗的患者组有20%预后良好,而对照组为0。
- 大型临床试验(如MASTERS、TREASURE试验)发现,在卒中后更早(如36小时内)进行干预,或针对较年轻(如<64岁)、梗死体积较大(>50mL)的特定患者,可能观察到更明显的获益趋势。
- 疗效评估需要长期随访,因为干细胞的作用机制涉及神经修复,效果可能在后期更明显。
2. 亚急性期(发病后1周至6个月)
常用细胞类型:骨髓间充质干细胞(BMSCs) 和骨髓单核细胞(BMMNCs)。
临床结果:此阶段的治疗安全性得到了长期(长达5年)的验证。在功能改善方面,研究结果不一,但部分设计严谨的试验证实了其疗效。
- 例如,STARTING系列试验不仅证明了长期安全性,还发现治疗能改善患者的下肢运动功能。疗效与治疗时机(卒中发作至输注的时间) 和患者年龄密切相关。
- 其他几项随机对照试验也证实了BMSCs治疗可以改善临床结局。
3. 慢性期(发病6个月后)
常用细胞类型:更多使用创新型细胞,如神经干细胞系(CTX0E03)、改良的间充质干细胞(SB623)等。
临床结果:干细胞为慢性期患者的功能恢复提供了新的可能性。不同的给药途径可能影响疗效。
- 颅内注射:多项研究(如PISCES试验、Chen等人的RCT)表明,直接将细胞注射到脑内安全可行,并能改善神经功能或手臂运动功能。一项荟萃分析指出,与其他途径相比,颅内注射可能具有更优的临床疗效,但其侵入性也带来了相对更高的风险。
- 鞘内注射与静脉注射:鞘内注射在小型研究中显示出促进功能恢复的潜力;静脉注射的研究结果则不一致,疗效有待进一步证实。
4.关键疗效趋势与共识
安全性是广泛共识:绝大多数临床试验证实,干细胞治疗在不同阶段的卒中患者中都具有良好的安全性和耐受性,严重不良事件罕见。
疗效与治疗时机紧密相关:虽然各阶段都观察到疗效,但证据提示,在急性期,尤其是发病后极早期进行治疗,可能获得更理想的功能恢复。
作用机制决定疗效特点:干细胞疗法并非单纯的急性神经保护,其核心在于通过调节免疫微环境、促进神经再生与修复来发挥作用。因此,其疗效可能在长期随访中逐渐显现,这与其他传统疗法不同。
个体化治疗是未来方向:疗效在不同研究、不同患者中存在差异。未来需要根据患者的年龄、卒中严重程度、梗死特点及分期等因素,优化细胞类型、剂量、给药途径和治疗时机,实现个体化精准治疗。
相关阅读:2025年1-11月干细胞治疗中风最新进展:炎症抑制与神经再生的双重突破
三、 政策与监管环境:框架重塑,为创新提速
2025年,中国在生物医学创新领域的顶层设计实现了历史性跨越,为干细胞等前沿疗法的规范、高效发展扫清了最大的制度障碍。
3.1 里程碑法规出台,构建全链条管理体系
2025年10月,国务院正式公布 《生物医学新技术临床研究和临床转化应用管理条例》 (国务院令第818号),将于2026年5月1日起施行。这是我国首次在国家层面以行政法规形式,对包括干细胞治疗在内的生物医学新技术构建了覆盖研发、临床研究到临床应用的全链条管理制度。[7]
核心突破:该《条例》为生物医学新技术开辟了区别于传统药品和医疗器械的 “第三类”监管路径,明确了在完成临床研究后,可向卫生健康部门申请直接转化为临床应用,打通了从实验室到病床的“最后一公里”。
3.2 监管路径持续优化,鼓励产学研医协同
在国家卫健委对人大建议的答复中,进一步明确了当前的政策导向:[8]
支持多元主体参与:在原有医疗机构为主体的基础上,政策鼓励企业、高校、科研院所与具备资质的医疗机构合作,共同发起临床研究,促进产学研医深度融合。
完善技术评价体系:国家药监局已制定近二十项细胞治疗相关技术指导原则,并实施严格的全链条质量管理,每年对生产企业进行全覆盖检查,确保产品安全。
推动区域先行先试:在北京、上海、广东、海南等自贸试验区,允许开展外资企业参与的人体干细胞技术开发与应用试点,以推动国际合作与产业创新。
四、未来展望与挑战
展望2026年及未来,中国干细胞治疗中风领域在明确的法规框架和积极的临床数据驱动下,发展路径愈发清晰,但迈向广泛应用仍需克服诸多挑战。
未来趋势:
- 临床研究加速纵深:随着干细胞项目的推进,更多针对急性期和不同严重程度、不同亚型中风患者的精细化临床试验将展开。慢性期治疗的研究也将向更大规模、更长随访期的确证性临床试验(II/III期)迈进。
- 治疗策略智能化与联合化:基于纳米囊泡、外泌体等“无细胞”智能递送系统的研发将成热点。同时,干细胞治疗与康复训练、神经调控技术(如经颅磁刺激)等组成联合方案,以实现疗效最大化。
- 产业化进程提速:在《条例》的引导下,“产学研医”协同将更加紧密,干细胞制剂的标准化、自动化、规模化生产体系将加速建立,以降低未来治疗成本。
面临的主要挑战:干细胞治疗目前成本高昂。未来产品若获批,如何将其纳入国家医保体系,或通过商业保险、创新支付模式(如按疗效付费)提高可及性,是关乎社会公平与产业可持续发展的终极课题。
结语
2025年,是中国干细胞治疗中风领域从“积累”迈向“爆发”的关键转折年。从大连医科大学附属第一医院开创性地启动国家首个急性期备案临床研究,到科学家们在《ACS Nano》《Nature Communications》等顶刊上不断揭示修复大脑的精密机制,再到国务院颁布奠定行业基石的《生物医学新技术临床研究和临床转化应用管理条例》,无不彰显着中国在这一生命科学前沿领域的决心、智慧与速度。
虽然前路仍有科学的高峰需要攀登,有医学的难题等待破解,但一条从基础发现到临床验证,再到政策支持的完整创新链条已经铸就。对于每年数百万新增的脑卒中患者及其家庭而言,这意味着“受损大脑可能被修复”不再是一个遥远的科学幻想,而是一个正被清晰勾勒、稳步走近的临床现实。2025年的这些坚实进展,正是照亮这条康复新路的第一束强光。
参考资料:
[1]https://gwgl.cqmu.edu.cn/info/1252/7444.htm
[2]https://www.x-mol.com/news/935791
[3]https://pubs.rsna.org/doi/abs/10.1148/radiol.250305
[4]https://mp.weixin.qq.com/s/QVwnMHhTCOtwUdcoNh86Bg
[5]霍德生物
[6]Liu, J., Cheng, L., Ma, C. et al. Clinical trials and advanced MRI techniques with stem cell therapy for ischemic stroke: present and future perspectives. J Transl Med 23, 1069 (2025). https://doi.org/10.1186/s12967-025-07054-5
[7]中国政府网
[8]https://www.nhc.gov.cn/wjw/jiany/202508/c8badee009af4094afc67c4d3fec2ea7.shtml
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 扫码添加官方微信
扫码添加官方微信